成份
本品活性成份為:阿侖膦酸鈉
化學名稱:(4-氨基-1-羥基亞丁基)二膦酸單鈉鹽三水合物。
化學結構式:
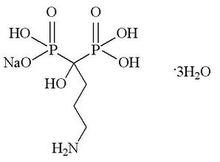 阿侖膦酸鈉腸溶片
阿侖膦酸鈉腸溶片分子式:CHNNaOP·3HO
分子量:325.12
性狀
本品為腸溶片,除去腸溶衣後顯白色或類白色。
適應症
1、適用於治療絕經後婦女的骨質疏鬆症,以預防髖部和脊柱骨折(椎骨壓縮性骨折)。
2、適用於治療男性骨質疏鬆症以增加骨量。
規格
按阿侖膦酸計 (1)10mg (2)70mg
用法用量
本品必須在每天第一次進食、喝飲料或套用其它藥物治療之前的至少半小時,用白水送服,因為其它飲料(包括礦泉水)、食物和一些藥物有可能會降低本品的吸收(見[藥物相互作用])。
本品為腸溶片,理論上可能會降低食道的不良反應,但為確保全全,推薦以下服藥方法:為儘快將藥物送至胃部,降低對食道的刺激,本品應在清晨用一滿杯白水送服,並且在服藥後至少30分鐘之內和當天第一次進食前,病人應避免躺臥。本品不應在就寢時和清早起床前服用,否則會增加發生食道不良反應的危險(見【注意事項】)。
如食物中攝入不足,所有骨質疏鬆患者都應補充鈣和維生素D(見[注意事項])。
老年患者或伴有輕至中度腎功能不全的患者(肌酐清除率35~60ml/min)不需要調整劑量。因缺乏相關用藥經驗,對於更嚴重的腎功能不全患者(肌酐清除率<35ml/min),不推薦使用本品。
絕經後婦女骨質疏鬆症的治療:
推薦劑量為:每周1次,1次1片70mg;或每天1次,1次1片10mg。
治療男性骨質疏鬆症以增加骨量:
推薦劑量為:每天1次,1次1片10mg。作為一種選擇,每周1次,1次1片70mg也可以考慮。
不良反應:
據國外文獻報導:
臨床研究
在臨床研究中,阿侖膦酸鈉一般耐受性良好。在一些長達5年的研究中,不良反應通常是輕微的,一般不需要停止治療。
治療絕經後婦女骨質疏鬆症
兩個(美國和多國)大型、實際上設計完全相同的為期三年、安慰劑對照、雙盲、多中心研究中,每天套用阿侖膦酸鈉10mg,結果顯示其總的安全性情況與安慰劑組相似。研究者所報告的在≥1%的毎天接受阿阿侖膦酸鈉10 mg的病人中,所發生的可能、很可能或一定和藥物相關且發生率高於安慰劑組的上消化道不良反應包括:(阿侖膦酸鈉6.6%,安慰劑4.8%)、消化不良(3.6%,3.5%)、食管潰瘍(1.5%,0.0%)、吞咽困難(1.0%,0.0%)和腹服(1.0%,0.8%)。
皮疹和紅斑很少發生。
另外,研究者所報告的在≥1%的每天接受阿侖瞵酸鈉10mg治療的病人,發生的可能、很可能或—定與藥物相關的,而且發生率高於安慰荊組的不良反應有:肌肉骨格疼痛(阿侖膦酸鈉4.1%,安慰劑2.5%)、便秘(3.1%,1.8%)、腹瀉(3.1%,l.8%)、脹氣(2.6%,0.5%)和頭痛( 2.6%,1.5%)。
在以上研究的2年延長期(治療4年和5年)中,阿侖膦酸鈉10mg/天的總體安全性狀況與有安慰劑對照的3年期間所觀察到的相似。另外,由於任何臨床不良反應而停用阿侖膦酸鈉每天10mg的患者比例也與該研究的前3年相似。
以下是研究者報告可能、很可能或一定與藥物有關的不良事件,其發生於為期一年臨床中任一組≥l%的病人中,或發生於為期三年臨床中≥1%的接受每天阿侖膦酸鈉10mg的病人且發生率高於安慰劑組。
治療男性骨質疏鬆症
茬一項為期兩年療程的雙盲、安慰劑對照、多中心的臨床研究中,146名每日服用阿侖瞵酸鈉10mg的男性患者的安全性資料與絕經後婦女的—致。
其他研究
一項十周的內窺鏡研究(包括男女牲共227人,平均年齡55歲)發現,阿侖瞵酸鈉每周一次70mg的治療組與安慰劑組在引起上消化道病變方面沒有差別。
另一項為期一年的研究(包括男女性335人,平均年齡50歲)發現,阿侖瞵酸鈉每周一次70mg的治療組與安慰劑組在總的安全性與耐受性方面相似,並且男女之間沒有差別。
治療糖皮質激素誘導的骨質疏鬆症
在兩個為期一年的安慰劑對照、雙盲、多中心臨床研究中,接受糖皮質激素治療的患者毎天服甩5mg或10mg阿侖瞵酸鈉的總的安全性和耐受性情況與安慰劑組相近。在接受阿侖瞵酸鈉5mg/天或10mg/天或安慰劑治療的想者發生被研究中認為可能、很可能或確定與藥物有關的≥1%不良反應列於下表。
研究中接受糖皮質激素治療的患者繼續治療的第二年(阿侖瞵酸鈉,n=147)的總的安全性和耐受性情況與第一年所觀察到的結果相似。
產品上市後經驗
阿侖瞵酸鈉上市套用後已報告的不良反應如下:
全身反應:過敏反應,包括蕁麻疹和罕見的血管性水腫。同其他二瞵酸鹽一樣,在開始服用阿侖瞵酸鈉時,會發生一過性的急性期的反應(肌痛、不適和罕見發燒)。在存在誘因條件時,會發生罕見的低鈣血症。
胃腸道反應:噁心、嘔吐、食管炎、食道糜爛、食道潰瘍、罕見食管狹窄或穿孔、口咽潰瘍;罕見胃和十二指腸潰瘍。某些較為嚴重並伴有併發症,儘管它們與藥物的因果關係尚未確定(見【注意事項】及【用法用量】)。在拔牙和/或局部感染癒合延遲時,會發生罕見的下頜局部骨壞死。
肌肉骨骼:骨、關節、和/或肌肉疼痛,罕見嚴重和/或致殘的情況。
皮膚:皮疹(偶伴有對光過敏),搔癢。罕見的嚴重皮膚反應,包括Stevens-Johnson綜合徵和毒性表皮壞死鬆懈。
特殊感覺:罕見眼色素層炎,罕見虹膜炎或虹膜外表層炎。
實驗室結果
在雙盲、多中心、安慰劑對照的臨床研究中,阿侖瞵酸納組分別有18%和10%的病人發生無症狀性、輕微且短暫的血清鈣和血清磷下降,安慰劑組中分別有12%和3%。但是血滿鈣<8.0mg/dL (2.0mmol/L)和血清磷≤2.0mg/dL (0.65mmol/l)的發生率,兩組情況相似。
禁忌:
導致食管排空延遲的食管異常,例如食管狹窄或弛緩不能。
不能站立或舉盲車少30分鐘者。
對本品任何成分過敏者。
低鈣血症(【注意事項】)。
注意事項:
和其它二磷酸鹽一樣,阿侖瞵酸鈉可能對上消化道黏膜產生局部刺激。
在服用阿侖膦酸鈉的病人中,已報告的食管不良反應有食管炎、食管潰瘍和食管糜爛,罕有食管狹窄或穿孔的報告。其中有些病例,因這些不良反應嚴重而需要住院治療。因此,醫生應該警惕可能發生食管反應的任何症狀和體徵,應指導病人如果出現吞咽困難、吞咽痛、胸骨後疼痛或新發胃灼熱或胃灼熱加重,停用本品並就醫。
本品為腸溶片,理論上可能會降低食道的不良反應,但為確保全全,仍需注意以下問題:在服用本品後躺臥、和/或不用一滿杯水送服藥、和/或出現提示食管刺激的症狀後仍繼續服藥的病人,發生嚴重食管不良反應的危險性較大。為了便於將本品送至胃部從而降低對食管的刺激,應指導病人用一滿杯水吞服藥物,並且在至少30分鐘內及在當天第一次進食之前不要躺臥。因此,提供病人詳盡的用藥指導,讓其充分理解是很重要的。(見【用法用量】)。
儘管在廣泛的臨床試驗中末觀察到胃和十二指腸潰瘍危險性的增加,上市後卻有極少量的報告,某些較為嚴重並伴有併發症。然而,它們與藥物的因果關係尚未確定。
因為阿侖膦酸鈉對上消化道黏膜有刺激性作用並有可能加重潛在的疾病,故應慎用於患有活動性上消化道疾病如吞咽困難、食管疾病、胃炎、十二指腸炎、潰瘍或最近有胃腸道病史(近1年內),如消化道潰瘍或活動性胃腸道出血或消化道手(除外幽門成形術)的病人。
本品應整片吞服,病人不應該咀嚼或吮吸藥片,以防口咽部潰瘍。應該特別指導病人在就寢前或清早起床前不要服用本品。應該告訴病人,若不遵醫囑就可能增加出現食管問題的危險性。應該告訴病人,如果發生食管疾病的症狀(如吞咽困難或疼痛、胸骨後疼痛或新發胃灼熱或胃灼熱加重),應該停用本品並請醫生診斷治療。
服用二膦酸鹽的病人會發生骨、關節和/或肌肉疼痛。在上市後經驗總結中,這些症狀嚴重和/或致殘的情況是罕見的(見不良反應,上市後經驗)。症狀發作的時間從開始治療後一天至幾個月不等。多數病人停藥後症狀緩解。當再服用同樣藥物或再服用另—種二膦酸鹽時,症狀會再次出現。
應當告訴每周服用一次一片70mg的病人,如果漏服了一次每周劑量,應當在記起後的早晨服用一次。不可以在同一天服用兩次,而應按其最初選擇的日期計畫,仍然每周服用一片。
肌酐清除率<35ml/min的病人,不推薦套用本品(見【用法用量】)。
除雌激素缺乏和老齡之外,造成骨質疏鬆的原因還應考慮糖皮質激素的使用。
在開始套用本品治療之前,必須先糾正低鈣血症(見禁忌)。
其它影響礦物質代謝的異常(例如維生素D缺乏),也應該得到有效治療。由於阿侖膦酸鈉可增加骨密度,因此可出現輕度的、無症狀的血鈣和磷酸鹽下降,特別是使用糖皮質激索治療的患者,可能他們的鈣吸收減少。因此,使用糖皮質激素的患者保證攝入足夠的鈣和維生素D是很重要的。
對於糖皮質激素治療的日劑量7.5mg強的松時,服用阿侖瞵酸鈉治療骨質疏鬆的利弊還未確定。開始治療之前,必須確定男女患者的荷爾蒙水平,並作適當調整。
採用同侖膦酸鈉和塘皮質激素聯合用藥時,在治療開始時必須測定骨密度值,並且在治療後的第6個月和第12個月再次測定。
阿侖膦酸鈉治療糖皮質激素誘導的骨質疏鬆症的效果顯示,患者的BMD值達到中等水平,低於健康年輕成人平均值1.2個標準差。
孕婦及哺乳期婦女用藥:
未在孕婦中做過研究,孕婦不宜使用。
未在哺乳期婦女中做過研究,不套用於這類病人。
兒童用藥:
未在兒童中做過研究,兒童不宜使用。
老年用藥:
在臨床研究中,未發現阿侖瞵酸鈉有年齡相關性的療效和安全性方面的差異,或遵醫囑。
藥物相互作用:
如果同時服用鈣補充製劑、抗酸藥物和其它口服藥物可能會干擾本品吸收。因此,病人在服用本品以後,必須等待至少半小時後,才可服用其他藥物。
預計無其它具有臨床意義的藥物相互作用。
兩項為期一或兩年的臨床研究對絕經後骨質疏鬆婦女同時套用激素替代治療(雌激素±孕教素)(靜脈同時經皮給藥或口服給藥)和阿侖磷酸鈉進行了評價。與單獨套用相比,聯合套用激素替代治療和阿侖膦酸鈉能更多地增加骨量,更多地降低骨轉換。在這些研究中,聯合治療與單獨治療在安全性和可耐受性方面是一致的。
特異性相互作用研究尚未進行。在治療男性和絕經後婦女的骨質疏鬆症的研究中,阿侖麟酸鈉已與各種常用處方藥同時使用,無明顯確定的臨床不良相互作用。
藥物過量:
目前尚沒有阿侖膦酸鈉過量用藥的資料。口服藥物過量可能會導致低鈣血症、低磷血症和上消化道不良事件,如胃部不適、胃灼熱、食管炎、胃炎或潰瘍。應給予牛奶或抗酸劑以結契約侖膦酸鈉。由於食管刺激的危險,不應該誘導嘔吐,病人應保持直立。
藥理毒理:
據國外文獻報導:
作用機制
動物研究發現阿侖膦酸鈉有下述作用方式。在細胞水平,阿侖膦酸鈉對骨吸收部位特別是破骨細胞作用的部位有親嗜性。正常情況下,破骨細胞粘附於骨表面但邊緣並不粗糙,而粗糙的邊緣則是骨吸收活躍的標誌。阿侖膦酸鈉不影響破骨細胞的聚集或粘附,但它確實能夠抑制破骨細胞的活性。小鼠體內進行的有關標記有放射性活性的[H]阿侖膦酸鈉在骨內作用部位的研究顯示,破骨細胞表面的攝入是成骨細胞表面的10倍。標記有放射活性的[H]阿侖麟酸鈉分別給予大鼠6天和小鼠49天后,檢查其骨組織發現,正常骨形成於阿侖膦酸鈉上面,後者與基質結合後不再具有藥理活性,因此阿侖膦酸鈉必須持續服用以抑制新形成的吸收表面的破骨細胞。狒狒和大鼠的組織形態測量學顯示,阿侖膦酸鈉能降低骨轉換(即,骨重建部位的數量),而且在這些重建部位,骨形成超過骨吸收,從而使骨量增加。
動物毒理
急性毒性
對雌性大鼠和小鼠來說,口服阿侖膦酸鈉的LD值分別為552mg/kg(3256mg/m)和966mg/kg(2898mg/m)(相當於人類口服劑量*27600和48300mg)。對雄性鼠,這些值要略高一些,分別為626mg/kg和1280mg/kg。而狗口服劑量達200mg/kg(4000mg/m仍未見致死作用(相當於人類口服劑量*10000mg)。
*以患者的體重為50公斤計。
慢性毒性
對大鼠和狗分別進行的長達1年和3年的重複劑量-毒性研究發現,阿侖膦酸鈉的相關變化有以下幾個方面:在內源性軟骨骨形成區保留了最初的松質骨;鹼性磷酸酶活性持續下降;血鈣和血磷的濃度一過性下降。這些都與阿侖膦酸鈉預期的藥理活性相關。對腎毒性最敏感的物種(如狗)出現腎毒性的劑量相當於人類至少套用100mg。大鼠需要更高的劑量才表現出這種腎毒性。胃腸毒性只出現在齧齒動物。這可能是由於對黏膜的直接作用,且僅發生在劑量超過2.5mg/kg/天時。
致癌作用
口服給予大鼠阿侖膦酸鈉每天3.75mg/kg觀察105周以及口服給予小鼠阿侖膦酸鈉lOmg/kg/天觀察92周,均未發現有致癌作用。
致突變作用
無論有無代謝活性,體外微生物致突變試驗未發現阿侖膦酸鈉有致突變作用。同樣,體外哺乳細胞致突變試驗、體外大鼠肝細胞鹼性洗脫試驗以及靜脈給予小鼠阿侖膦酸鈉每天25mg/kg(75mg/m)體內染色體畸變試驗也均未發現其有致突變作用。但是,中國倉鼠卵細胞的體外染色體畸變試驗發現:阿侖膦酸鈉濃度大於5mM時有弱細胞毒作用,這對人類來說無相關性。因為,體內的治療劑量不可能達到同樣濃度。而且,五項基因毒性研究中有四項都是純陰性結果,包括與人類致癌可能性最直接相關的研究(體內染色體畸變試驗和微生物致突變試驗)以及大鼠和小鼠體內的致癌研究陰性結果均表明阿侖膦酸鈉對人類沒有基因毒性或致癌的危險。
繁殖
口服給予大鼠阿侖膦酸鈉每天5mg/kg對兩性的生育和繁殖能力都沒有影響。這些研究中發現的唯一與藥物相關的影響是大鼠分娩困難。這與藥物介導的低鈣血症直接相關,這種影響可通過給大鼠補充鈣來預防。而且,每天1.25mg/kg的劑量沒有任何影響。
生長發育
有關生長發育的毒性研究中,給予大鼠阿侖膦酸鈉每天25mg/kg和給予兔子每天35mg/kg均未發現有不良影響。
藥代動力學:
據國外文獻報導
吸收
以靜脈劑量作參考,空腰及標準早餐前2小時給予阿侖膦酸鈉5~70mg,其平均口服生物利用度在女性為0.64%,在男性口服l0mg為0.6%,兩者相似。如果在標準早餐前1或1.5小時給藥,其生物利用度在兩性有類似下降(約40%)。骨質疏鬆硏究證明,在每天第一次進食或喝飲料前至少30分鐘給予阿侖膦酸鈉才發揮作用。
如果在標準早餐後2小時或2小時以上給藥,其生物利用度可以忽略不計。阿侖膦酸鈉與咖啡或桔汁同服可使其生物利用度下降約60%。
對健康者來說,口服給予潑尼松(20mg每天三次,連用5天)對阿侖膦酸鈉的口服生物利用度的影響沒有臨床意義(平均增加20~44%)。
分布
研究表明,靜脈給予大鼠阿侖膦酸鈉lmg/kg後,其瞬間分布於軟組織,但接著迅速再分布於骨組織或通過尿排泄。其在人體內的平均穩態分布容積,除了骨組織外至少為28L。口服給予治療劑量的阿侖膦酸鈉由於其在血漿內的濃度過低,難以進行檢驗分析(小於5ng/ml)。其血漿蛋白結合率約為78%。
代謝
還沒有證據表明阿侖膦酸鈉在動物或人體內代謝。
清除
一次性靜脈給予C標記的阿侖膦酸鈉發現,約50%的放射性活性在72小時內由尿排泄,糞便中沒有或只有很少的放射性活性。一次性靜脈給予10mg阿侖膦酸鈉後測定其腎清除率為71ml/min,全身清除率不超過200ml/min。靜脈給藥後6小時內其血漿濃度下降95%以上。其在人體內的終末半衰期估計大於10年,這提示阿侖膦酸鈉從骨骼中釋放。
病人特徵
臨床前研究表明此藥不在骨內沉積而迅速由尿排泄。在動物身上長期積累靜脈給藥35mg/kg沒有發現骨吸收飽和的證據。儘管還沒有臨床資料,但腎功能受損時,和動物研究的結果一樣,阿侖膦酸鈉通過腎的清除很可能會下降。因此,當腎功能受損時,阿侖膦酸鈉在體內的蓄積可能會增加(見[用法用量])。
貯藏
密閉保存。
包裝
鋁-鋁包裝。
10mg:6片/盒,7片/盒,10片/盒,12片/盒,14片/盒,30片/盒。
70mg:1片/盒,2片/盒,4片/盒。
有效期
24個月
執行標準
國家食品藥品監督管理局標準YBH06722009
