簡介
每年,法國有一萬人自願報名,充當製藥公司試驗新藥的“實驗田”。一旦體檢合格,他們就成了新藥上市前的最後一批試驗者。抽血、B超,沒完沒了的檢查,有時還伴著頭暈噁心等副作用。他們中的有些人,已經把這項工作當成自己補貼家用的一種途徑,戲稱自己是試驗新藥的職業“豚鼠人”。驅使他們從事這一行當的主要目的,是因為職業“豚鼠人”收入輕鬆,而且待遇不菲。沿革
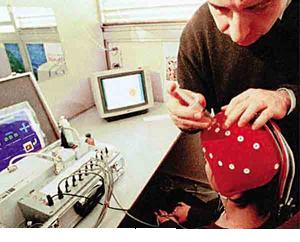 接受試驗的“豚鼠人”
接受試驗的“豚鼠人”現在我們都知道,新藥上市前,必須在人身上做臨床試驗。不過,這個制度一直到20世紀五六十年代發生了“反應停”事件後,才在全世界範圍內得以確立。“反應停”是當時聯邦德國推出的一種新藥,1957年上市,用來抑制孕婦妊娠期的噁心嘔吐和精神緊張。那時候,新藥上市前無需做臨床試驗,在動物身上試驗完畢後就可以銷售了。
1960年,歐洲的一位小兒科醫生連續接診了幾個畸形嬰兒,他們有的四肢奇短,有的甚至沒有胳膊,手直接長在軀體上,成了“海豹兒”。這位醫生髮現,這些畸形兒的母親無一例外在懷孕期間服用過“反應停”。在歐美各國、日本、澳大利亞和非洲,“海豹兒”也都大量出現。
1961年,“反應停”被各國禁用,但全世界已有約1.2萬嬰兒受害,其中5000多人痛苦地存活了下來。此事在西方引起了很大的震動,被稱為“20世紀最大的藥物災難”,生產“反應停”的藥廠也因聲名狼藉而倒閉。
不久後,國際醫學界達成共識:僅在動物身上試驗新藥是遠遠不夠的,任何新藥推出前,都必須在志願者身上進行臨床試驗,驗明這種藥有何副作用。
由於少數醫療機構在患者不知情的情況下偷偷進行人體試驗,1964年,國際醫學界通過了《赫爾辛基宣言》,要求“必須永遠尊重研究對象捍衛其尊嚴的權利”,這個宣言,是對1946年《紐倫堡公約》的強調。
從此之後,各國在臨床試驗方面的法規越來越健全,試藥行為逐漸規範了起來。
背景
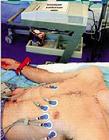 “豚鼠人”
“豚鼠人”“是藥三分毒”,試藥這一行充滿了風險。由於工作簡單、報酬很高,還是有很多人願意以身試藥。新藥通常先在小白鼠身上做試驗,而小白鼠又稱豚鼠,因此,試藥者常被戲稱為“豚鼠人”。
主要人群是社會弱勢群體,生活所迫,維持家用。其中還有部分的大學生,他們為了繼續學業,保證正常的學習生活開始紛紛加入“豚鼠人”的隊伍里。而後者由於年輕而健康也就成了最佳人選。
事件
“為了醫學研究,現招募18歲到45歲的志願者,男性要求無吸菸史,或日吸菸數量不超過五隻;女性年齡限制放寬到55歲,沒有接受過激素治療。體檢合格者視具體情況給予500到3100歐元的報酬。”在夏天,類似的小廣告終日出現在法國各類報紙的邊邊角角。炎熱的夏季是法國傳統的休假季節,也是製藥公司尋找“豚鼠人”的黃金季節。除去生活捉襟見肘的老百姓,還有許多大學生會被製藥公司的廣告吸引過來,健康而年輕的身體讓他們很容易通過體檢。
據法國一位已經連續6年報名充當志願者的18歲大學生描述:“當然,這種差使沒啥意思可言,但它可以讓我很快地賺到一大筆錢。一旦通過體檢住進醫院,那就意味著每天都有375元錢到手哇。而我所做的,只是認真閱讀注意事項,按照要求完成檢查。這些檢查大多被安排在清早或是中午,剩下的時間就沒人管你了。”事實上,沒有哪個“豚鼠人”膽敢忽視注意事項,契約上明明白白地規定,如果取樣時遲到,罰款40歐元;如果在禁菸期內忍不住噴雲吐霧,將被罰款150歐元。
製藥公司通過人體進行的新藥試驗,是藥品在動物身上試驗成功之後,獲得醫藥局批文進入市場之前的必經之路。製藥公司在獲得批文的過程中必須提供足夠的數據,在證明新藥療效的同時,保證它不會對人體產生毒副作用。
但不要以為“豚鼠人”的工作很輕鬆,只要吃藥就行,其實,這份活很遭罪。
 試藥
試藥生理
“豚鼠人”體檢合格後,除每天吃藥外,還要抽血,做B超,接受沒完沒了的各種檢查。其中做腦電圖檢查時,要把電針刺進頭皮里,最令“豚鼠人”望而生畏。此外,有些試驗要求“豚鼠人”先餓得前胸貼後背,有些則要先將胃填滿再吃藥。而新藥在“豚鼠人”身上產生頭暈、噁心等毒副作用,也是常見的事。心理
“豚鼠人”在心理上也很受折磨。法國的一個“豚鼠人”描述說:“化驗的屋子望過去好像一座大廠房,我們像軍人一樣秩序井然。‘豚鼠’們在一種奇怪的氣氛里排隊等待抽血,屋子裡很靜,大家都有一點緊張。‘豚鼠人’里年輕人居多,而那些給我們抽血的護士,年紀就要大許多。‘豚鼠人’誰都沒有自己的名字,靠號碼彼此區分,大家在這種流水線式的作業中覺得自己被當成動物或是機器來對待,一種屈辱感油然而生。而護士一刻不停地重複著相同的勞動,也被機械式的工作折磨得疲憊而煩躁,於是衝突就變得家常便飯起來。”其他形式
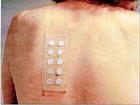 “豚鼠人”
“豚鼠人”一位經驗豐富的“豚鼠人”說:“我們的行話管這種活兒叫做‘膏藥’。十小塊化妝品樣品被粘在膠帶上,就像藥店裡的膏藥一樣,然後把它貼在後背靠上的位置。這差使沒什麼危險,只是要忍著點刺癢,有時還可能引起過敏。”對於在背上貼著這么一塊“膏藥”,既不能沾水,又不能讓太陽曬著。
試藥代辦機構
由於製藥公司對“豚鼠人”的需求量與日俱增,一種專門代理試藥的機構就應運而生了,這就是契約研究組織(ContractResearchOrganization,簡稱CRO)。 “豚鼠人”
“豚鼠人”CRO專門負責尋找試藥的醫院、招募“豚鼠人”、與相關政府部門打交道等業務。目前,世界上約有500家CRO,多數是美國公司,其中最大的10家,占了試藥市場50%以上的份額。美國的QuintilesTransnational是全球最大的CRO,業務遍及30多個國家。光是在印度,該公司就招募過6400名病人,在精神病、傳染病和腫瘤等領域進行試藥。
多數CRO配備有藥學專家、管理專家和技術人員,能守法地開展業務。也有一些CRO純粹是“公關公司”,靠遊說衛生管理部門、甚至向官員行賄來獲得臨床試驗批文,然後矇騙“豚鼠人”試藥。這種CRO中的敗類,已經屢屢鬧出過害人性命的醜聞。比如,印度泰米爾納德邦醫學院的一位教授就曾發現,一個CRO替醫院草擬並讓病人簽字的試藥協定上,關於藥物的副作用一字未提,而那些病人大多是文盲。
保護措施
 “豚鼠人”
“豚鼠人”20世紀90年代初,世界衛生組織參考了各國在試藥方面的管理規範後,制定了適用於各成員國的《藥品臨床試驗規範指導原則》,並向各國推薦。包括中國在內的很多國家,參照這一原則制定了相關法規。
美國的法律也有其可借鑑之處———“豚鼠人”的身體一旦出問題,甚至可以在與藥廠的官司中追溯自己20年前參加過的臨床試驗。因此在美國,藥廠要是在官司中輸給了“豚鼠人”,動輒就要賠幾千萬美元。
法國在這方面也做得很細緻。為了防止某些人變成職業“豚鼠人”,1988年,法國頒布法律,限定了每個“豚鼠人”每年從藥廠獲得的補償金數額。這個數額,現在相當於3800歐元(當時法國使用法郎)。也就是說,你每年參加試藥只準拿到這點錢,試藥次數再多也白搭。此外,“豚鼠人”每次試藥後都有一個“絕對禁止期”,在此期間,不得參加試藥。
為了防止“豚鼠人”違法試藥,法國衛生部專門替“豚鼠人”建立檔案,詳細記錄了每個“豚鼠人”參加過哪些臨床試驗等情況。
同時在法國,“健康產品衛生安全委員會”(Afssaps)就是保護“豚鼠人”健康安全的專門機構。安全委員會主席弗朗索瓦·沙皮伊說:“我們有一個諮詢委員會負責審核工作。首先,確認各公司所做的試驗確屬必要;其次,這種試驗不能有失人道。”只有向該委員會提出申請並獲得通過的試驗項目,才能招募志願者。無論化妝品還是新藥,試驗過程中讓某些“豚鼠人”感到頭痛、輕微噁心、乏力、眩暈,或是身上起點風疹塊,只要不是太嚴重,都不會影響到上市許可證的申請。但是,當這些反應在“豚鼠人”身上表現得很明顯,相關部門就不會頒發許可證。
據統計,法國製藥公司篩選出的20萬種試劑里,只有1000種最終可以獲得臨床試驗的資格(這時試驗對象還是實驗室里的各種動物)。然後,大約有70種試劑可以拿到“豚鼠人”身上進行試驗。最後,只有15種新藥可以獲得上市許可證。而在最終獲準上市的新藥里,一般只有6到8種在市場上有銷路。一家製藥公司實驗室的工作人員說:“一般講,一種新藥從開發到最終上市,中間要經過十餘年的時間。”一年又一年,“豚鼠人”就這樣為我們的健康用藥充當著先鋒。
