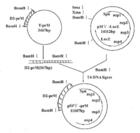
 苯硫酸酯酶
苯硫酸酯酶基本信息
苯硫酸酯酶由生物體內細胞產生的一種生物催化劑。由蛋白質組成(少數為RNA)。能在機體中十分溫和的條件下,高效率地催化各種生物化學反應,促進生物體的新陳代謝。生命活動中的消化、吸收、呼吸、運動和生殖都是酶促反應過程。酶是細胞賴以生存的基礎。細胞新陳代謝包括的所有化學反應幾乎都是在酶的催化下進行的。如哺乳動物的細胞就含有幾千種酶。它們或是溶解於細胞液中,或是與各種膜結構結合在一起,或是位於細胞內其他結構的特定位置上。這些酶統稱胞內酶;另外,還有一些在細胞內合成後再分泌至細胞外的酶──胞外酶。酶催化化學反應的能力叫酶活力(或稱酶活性)。酶活力可受多種因素的調節控制,從而使生物體能適應外界條件的變化,維持生命活動。沒有酶的參與,新陳代謝只能以極其緩慢的速度進行,生命活動就根本無法維持。例如食物必須在酶的作用下降解成小分子,才能透過腸壁,被組織吸收和利用。在胃裡有胃蛋白酶,在腸里有胰臟分泌的胰蛋白酶、胰凝乳蛋白酶、脂肪酶和澱粉酶等。又如食物的氧化是動物能量的來源,其氧化過程也是在一系列酶的催化下完成的。
特性
 苯硫酸酯酶
苯硫酸酯酶一般來說,動物體內的酶最適溫度在35到40攝氏度之間,植物體內的酶最適溫度在40-50攝氏度之間;細菌和真菌體內的酶最適溫度差別較大,有得酶最適溫度可高達70攝氏度。動物體內的酶最適PH大多在6.5-8.0之間,但也有例外,如胃蛋白酶的最適PH為1.5,植物體內的酶最適PH大多在4.5-6.5之間。
酶的這些性質使細胞內錯綜複雜的物質代謝過程能有條不紊地進行,使物質代謝與正常的生理機能互相適應.若因遺傳缺陷造成某個酶缺損,或其它原因造成酶的活性減弱,均可導致該酶催化的反應異常,使物質代謝紊亂,甚至發生疾病.因此酶與醫學的關係十分密切。
相關信息
 苯硫酸酯酶
苯硫酸酯酶圖說明這三個酶的底物結合部位均有一個袋形結構,糜蛋白酶該處能容納芳香基或非極性基;胰蛋白酶袋子底部稍有不同其中一個胺基酸殘基為天冬氨酸取代,使該處負電荷增強,故該處對帶正電荷的賴氨酸或精酸殘基結合有利;彈性蛋白酶口袋二側為纈氨酸和蘇氨酸殘基所取代,因此該處只能結合較小側鏈和不帶電荷的基團.說明酶的催化特異性與酶分子結構的緊密關係。
相關分類
 苯硫酸酯酶
苯硫酸酯酶1.氧化還原酶類(oxidoreductase)
促進底物的氧化或還原。
2.轉移酶類(transferases)
促進不同物質分子間某種化學基團的交換或轉移。
3.水解酶類(hydrolases )
促進水解反應。
4.裂解酶類(lyases)
催化從底物分子雙鍵上加基團或脫基團反應,即促進一種化合物分裂為兩種化合物,或由兩種化合物合成一種化合物。
5.異構酶類(isomerases)
促進同分異構體互相轉化,即催化底物分子內部的重排反應。
6.合成酶類(ligase)
促進兩分子化合物互相結合,同時ATP分子(或其它三磷酸核苷)中的高能磷酸鍵斷裂,即催化分子間締合反應。
按照國際生化協會公布的酶的統一分類原則,在上述六大類基礎上,在每一大類酶中又根據底物中被作用的基團或鍵的特點,分為若干亞類;為了更精確地表明底物或反應物的性質,每一個亞類再分為幾個組(亞亞類);每個組中直接包含若干個酶。
