絕熱過程
正文
熱力學系統同外界無熱交換的過程。在良好的絕熱材料隔絕的系統中進行的過程,或由於過程進行得很快,以致同外界沒有顯著熱量交換的過程都可近似地看作絕熱過程。例如聲波在空氣中的傳播,以及內燃機中氣體的壓縮過程等,都進行得很快,可當作絕熱過程處理。在絕熱的準靜態過程中,熱力學系統狀態參量之間存在著一定的關係,稱為絕熱過程方程。理想氣體的準靜態絕熱過程方程有以下三種形式:
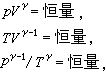
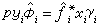
由熱力學第一定律可知,在絕熱過程(Q=0)中,能量轉換的特點是:系統內能的減少等於系統對外界所作的功,即-ΔU=A。理想氣體在準靜態絕熱過程中功的表達式為
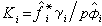
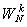
根據熱力學第二定律的數學表達式
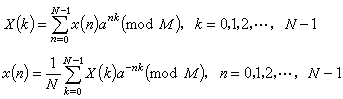 ,可見系統的熵在可逆過程中的增量 dS 等於系統所吸收的熱量婾Q同熱源的熱力學溫度T 之比。對於可逆的絕熱過程而言,
,可見系統的熵在可逆過程中的增量 dS 等於系統所吸收的熱量婾Q同熱源的熱力學溫度T 之比。對於可逆的絕熱過程而言,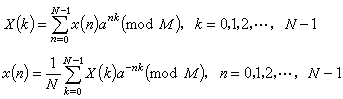 =0,即熵不變,所以可逆絕熱過程即等熵過程。
=0,即熵不變,所以可逆絕熱過程即等熵過程。
