發展歷史
1846年法國化學家J.J.Ebelmen用SiCl4與乙醇混合後生成四乙氧基矽烷(TEOS),發現在濕空氣中發生水解並形成了凝膠。
20世紀30年代W.Geffcken證實用金屬醇鹽的水解和凝膠化可以製備氧化物薄膜。
1971年德國H.Dislich報導了通過金屬醇鹽水解製備了SiO2-B2O-Al2O3-Na2O-K2O多組分玻璃。
1975年B.E.Yoldas和M.Yamane製得整塊陶瓷材料及多孔透明氧化鋁薄膜。
80年代以來,在玻璃、氧化物塗層、功能陶瓷粉料以及傳統方法難以製得的複合氧化物材料得到成功套用。
基本原理
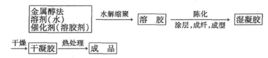
將酯類化合物或金屬醇鹽溶於有機溶劑中,形成均勻的溶液,然後加入其他組分,在一定溫度下反應形成凝膠,最後經乾燥處理製成產品。
化學過程
溶膠-凝膠法的化學過程首先是將原料分散在溶劑中,然後經過水解反應生成活性單體,活性單體進行聚合,開始成為溶膠,進而生成具有一定空間結構的凝膠,經過乾燥和熱處理製備出納米粒子和所需要材料。
其最基本的反應是:
(l) 水解反應:M(OR)n + xH2O → M (OH) x (OR) n-x + xROH
(2) 聚合反應:-M-OH + HO-M- → -M-O-M-+H2O
-M-OR + HO-M- → -M-O-M-+ROH
分類
溶膠-凝膠法按產生溶膠凝膠過程機制主要分成三種類型:
(1)傳統膠體型。通過控制溶液中金屬離子的沉澱過程,使形成的顆粒不團聚成大顆粒而沉澱得到穩定均勻的溶膠,再經過蒸發得到凝膠。
(2)無機聚合物型。通過可溶性聚合物在水中或有機相中的溶膠過程,使金屬離子均勻分散到其凝膠中。常用的聚合物有聚乙烯醇、硬脂酸等。
(3)絡合物型。通過絡合劑將金屬離子形成絡合物,再經過溶膠.凝膠過程成絡合物凝膠。
特點
溶膠--凝膠法與其它方法相比具有許多獨特的優點:
(1)由於溶膠--凝膠法中所用的原料首先被分散到溶劑中而形成低粘度的溶液,因此,就可以在很短的時間內獲得分子水平的均勻性,在形成凝膠時,反應物之間很可能是在分子水平上被均勻地混合;
(2)由於經過溶液反應步驟,那么就很容易均勻定量地摻入一些微量元素,實現分子水平上的均勻摻雜;
(3)與固相反應相比,化學反應將容易進行,而且僅需要較低的合成溫度,一般認為溶膠一凝膠體系中組分的擴散在納米範圍內,而固相反應時組分擴散是在微米範圍內,因此反應容易進行,溫度較低;
(4)選擇合適的條件可以製備各種新型材料。但是,溶膠一凝膠法也不可避免的存在一些問題,例如:原料金屬醇鹽成本較高;有機溶劑對人體有一定的危害性;整個溶膠一凝膠過程所需時間較長,常需要幾天或兒幾周;存在殘留小孔洞;存在殘留的碳;在乾燥過程中會逸出氣體及有機物,並產生收縮。
目前,有些問題已經得到解決,例如:在乾燥介質臨界溫度和臨界壓力的條件下進行乾燥可以避免物料在乾燥過程中的收縮和碎裂,從而保持物料原有的結構與狀態,防止初級納米粒子的團聚和凝聚;將前驅體由金屬醇鹽改為金屬無機鹽,有效的降低了原料的成本;檸檬酸一硝酸鹽法中利用自燃燒的方法可以減少反應時間和殘留的碳含量等等。
重要套用
金屬化合物經溶液、溶膠、凝膠而固化,再經低溫熱處理而生成納米粒子。其特點反應物種多,產物顆粒均一,過程易控制,適於氧化物和Ⅱ~Ⅵ族化合物的製備。
溶膠一凝膠法作為低溫或溫和條件下合成無機化合物或無機材料的重要方法,在軟化學合成中占有重要地位。在製備玻璃、陶瓷、薄膜、纖維、複合材料等方面獲得重要套用,更廣泛用於製備納米粒子。
具體套用領域:
①材料學:高性能粒子探測器,隔熱材料,聲阻抗耦合材料,電介質材料,有機-無機雜化材料,金屬陶瓷塗層耐蝕材料,納米級氧化物薄膜材料,橡膠工業
②催化劑方面:金屬氧化物催化劑,包容均相催化劑,
③色譜分析:製備色譜填料,製備開管柱和電色譜固定相,電分析,光分析