形態
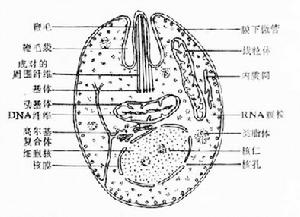 杜氏利什曼原蟲
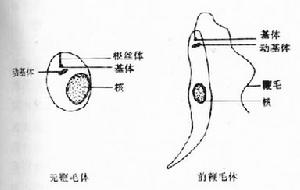
杜氏利什曼原蟲在透射電鏡下,蟲體由內外兩層表膜包被。每一層為一個單位膜。在內層表膜下有排列整齊的管狀纖維,稱為膜下微管(subpellicular microtubule)微管數目、直徑、間距等在種、株鑑定上有一定意義。蟲體前端的表膜向內凹陷,形成一袋狀腔,稱為鞭毛袋。內有一根很短的鞭毛(即光鏡下的根絲體)。基體為中空圓形。動基體為臘腸狀,其內有一束與長軸平行的纖絲,該纖絲由DNA組成。由於動基體在蟲體發育過程中可分出新的線粒體,因此,實際上它是一個大線粒體。其它線粒體呈泡狀或管狀,內有少數排列不整齊的板狀嵴。類脂體圓形或卵圓形。內質網不發達,呈管狀或泡狀。核一個,卵圓形,大小約1.5×1.0µm。核膜兩層可見核孔。核仁1-2個。
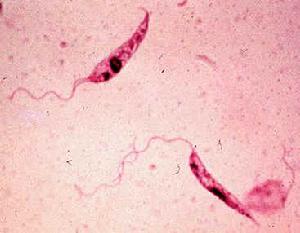
前鞭毛體(promastigote)寄生於白蛉消化道。成熟的蟲體呈梭形,大小為14.3~20µm×1.5-1.8µm,核位於蟲體中部,動基體在前部。基體在動基體之前,由此發現一鞭毛游離於蟲體外。前鞭毛體運動活潑,鞭毛不停地擺動。在培養基內常以蟲體前端聚集成團,排列成菊花狀。有時也可見到粗短形前鞭毛體,這與發育程度不同有關。
生活史
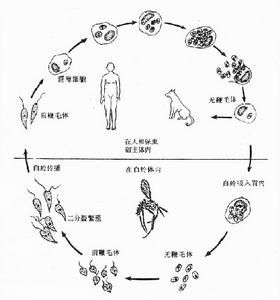 杜氏利什曼原蟲生活史
杜氏利什曼原蟲生活史1.在白蛉體內發育 當雌性白蛉(傳播媒介)叮刺病人或被感染的動物時,血液或皮膚內含無鞭毛體的巨噬細胞被吸入胃內,經24小時,無鞭毛體發育為早期前鞭毛體。此時蟲體呈卵圓形,鞭毛也已開始伸出體外。48小時後發育為短粗的前鞭毛體或梭形前鞭毛體。體形從卵圓形逐漸變為寬梭形或長度超過寬度3倍的梭形,此時鞭毛也由短變長。至第3、4天出現大量成熟前鞭毛體,長11.3-15.9µm(有時可達20µm),活動力明顯加強,並以縱二分裂法繁殖,分裂時,基體、動基體及核首先分裂,然後蟲體自前向後逐漸一分為二個子體。原來的鞭毛留在一個基體上,另一個基體重新生出一根鞭毛。在數量急增的同時,逐漸向白蛉前胃、食道和咽部移動。一周后具感染力的前鞭毛體大量聚集在口腔及喙。當白蛉叮刺健康人時,前鞭毛體即隨白蛉唾液進入人體。
2.在人體內發育 感染有前鞭毛體的雌性白蛉叮吸人體或哺乳動物時,前鞭毛體即可隨白蛉分泌的唾液進入其體內。一部分前鞭毛體被多形核白細胞吞噬消滅,一部分則進入巨噬細胞。前鞭毛體進入巨噬細胞後逐漸變圓,失去其鞭毛的體外部分,向無鞭毛體期轉化。同時巨噬細胞內形成納蟲空泡(parasitophorous vacuole)。此時巨噬細胞的溶酶體與之融合,使蟲體處於溶酶體的包圍之中。無鞭毛體在巨噬細胞的納蟲空泡內不但可以存活,而且進行分裂繁殖,最終導致巨噬細胞破裂。游離的無鞭毛體又進入其它巨噬細胞,重複上述增殖過程。
利什曼原蟲侵入巨噬細胞的機制
體外試驗研究結果表明,利什曼原蟲首先粘附於巨噬細胞。再進入該細胞內。粘附的途徑大體可分為兩種:一種為配體-受體途徑,一種為前鞭毛體吸附的抗體和補體與巨噬細胞表面的Fc或C3b受體結合途徑。在調整(modulation)或封閉這些受體後可大大減少前鞭毛體與巨噬細胞的結合。還有試驗表明,原蟲質膜中的分子量63KD糖蛋白(GP63)能與巨噬細胞表面結合,發揮吸附作用。粘附後原蟲隨巨噬細胞的吞噬活動而進入細胞,而非前鞭毛體主動入侵巨噬細胞。
前鞭毛體轉化為無鞭毛體的機制及兩者的差異
利什曼原蟲前鞭毛體轉化為無鞭毛體的機制目前尚未完全闡明。一般認為可能與微小環境的改變如pH、溫度等以及原蟲所需營養物質和宿主對原蟲產生的特異性等因素有關。實驗證明,前鞭毛體以27℃為宜,無鞭毛體則需要35℃環境。它們的抗原性也有明顯差異,各有不同的期特異抗原區帶。此外,微管蛋白(tubulin)也有較大差異。而生化方面的差異主要表現在量的不同。
機體對利什曼原蟲的殺傷
利什曼原蟲在巨噬細胞內寄生和繁殖,其抗原可在巨噬細胞表面表達。宿主對利什曼原蟲的免疫應答屬細胞免疫,效應細胞為激活的巨噬細胞。通過細胞內產生的活性氧殺傷無鞭毛體。含有無鞭毛體的巨噬細胞壞死可清除蟲體。近年來有研究表明,抗體在宿主殺傷利什曼原蟲的過程中也起了作用。
致病性
 杜氏利什曼原蟲
杜氏利什曼原蟲由於血小板減少,患者常發生鼻衄、牙齦出血等症狀。蛋白尿及血尿的出現,可能由於患者發生腎小球澱粉樣變性以及腎小球內有免疫複合物的沉積所致。
患黑熱病時出現免疫缺陷,易並發各種感染疾病,是造成黑熱病患者死亡的主要原因。患者治癒後這種易並發感染的現象消失。可見杜氏利什曼原蟲感染不但伴隨有特異性細胞免疫反應的抑制,還可能導致機體對除了該原蟲以外的其它抗原產生細胞免疫和體液免疫反應的能力降低,即非特異性抑制。例如患者對傷寒甲、乙菌苗的免疫應答顯著下降。免疫力低下的原因,可能與原蟲繁殖快速,產生的抗原過多,機體處於免疫無反應(anergy)狀態有關。
患者經特效藥物治療後,痊癒率較高,一般不會再次感染,可獲得終生免疫。
在中國黑熱病有下列特殊臨床表現:
皮膚型黑熱病:大多分布於平原地區。據資料統皮膚損害與內臟同時並發者,占58.0%;一部分病人(32.3%)發生在內臟病消失多年之後;還有少數(9.7%)既無內臟感染,又無黑熱病病史的原發病人。皮膚損傷除少數為褪色型外,多數為結節型。結節呈大小不等的肉芽腫,或呈暗色丘疹狀,常見於面部及頸部,在結節內可查到無鞭毛體。皮膚型黑熱病易與瘤型麻風診斷混淆。此型黑熱病更常見於印度、蘇丹。
淋巴結型黑熱病:此型患者的特徵是無黑熱病病史,局部淋巴結腫大,大小不一,位較表淺,無壓痛,無紅腫,嗜酸性粒細胞增多。淋巴結活檢可在類上皮細胞內查見無鞭毛體。
導致病症
 杜氏利什曼原蟲
杜氏利什曼原蟲根據傳染來源的不同,黑熱病在流行病學上可大致分為三種不同的類型,即人源型、犬源型和自然疫源型;分別以印度、地中海盆地和中亞細亞荒漠內的黑熱病為典型代表。中國由於幅員遼闊,黑熱病的流行範圍又廣,包括平原、山丘和荒漠等三種不同類型的地區,因此這三種不同類型的黑熱病在國內都能見到。它們在流行歷史,寄生蟲與宿主的關係以及免疫等方面,有著明顯的差別,在流行病學上也各有其特點。
實驗診斷
1.病原檢查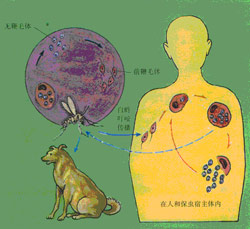 杜氏利什曼原蟲生活史
杜氏利什曼原蟲生活史⑴穿刺檢查:
1)塗片法:以骨髓穿刺物作塗片、染色,鏡檢。此法最為常用,原蟲檢出率為80%-90%。淋巴結穿刺應選取表淺、腫大者,檢出率為46%-87%。也可做淋巴結活檢。脾穿刺檢出率較高,可達90.6%-99.3%,但不安全,少用。
2)培養法:將上述穿刺物接種於NNN培養基,置22-25℃溫箱內。經一周,若培養物中查見活動活潑的前鞭毛體,則判為陽性結果。操作及培養過程應嚴格注意無菌。
3)動物接種法:穿刺物接種於易感動物(如地鼠、BALB/c小鼠等),1-2個月後取肝、脾作印片或塗片,瑞氏染液染色,鏡檢。
⑵皮膚活組織檢查:
在皮膚結節處用消毒針頭刺破皮膚,取少許組織液,或用手術刀亂取少許組織作塗片,染色,鏡檢。
2.免疫診斷法
⑴檢測血清抗體:如酶聯免疫吸附試驗(ELISA)、間接血凝試驗(IHA)、對流免疫電泳(CIE)、間接螢光試驗(IF)、直接凝集試驗等,陽性率高,假陽性率也較高。近年來,用分子生物學方法獲得純抗原,降低了假陽性率。
⑵檢測血清循環抗原:單克隆抗體抗原斑點試驗(McAb-AST)用於診斷黑熱病,陽性率高,敏感性、特異性、重複性均較好,僅需微量血清即可,還可用於療效評價。
3.分子生物學方法
近年來,用聚合酶鏈反應(PCR)及DNA探針技術檢測黑熱病取得較好的效果,敏感性、特異性高,但操作較複雜,目前未能普遍推廣。
培養方法
(一)前鞭毛體培養1.培養基主要有NNN(3N)培養基和USMARU培養基。
NNN培養基可以分固體部分和液體部分。固體部分:1.4g瓊脂、0.6g氯化鈉加入90ml雙蒸水,加熱溶解,每4ml或1.5ml分裝入12ml或6ml培養管中,121℃15min滅菌,而後加入去纖維素的兔血至15%含量,混合併放成斜面,4℃保存。液體部分為少量的滅菌雙蒸水,還可加入青黴素和鏈黴素。培養溫度在20-27℃左右。USMARU培養基是將Bacto血瓊脂4g溶於雙蒸水中,以後製法如NNN培養基。
2.操作步驟取皮膚或組織、骨髓的活檢標本加入培養管中,20~25℃培養。每2-3天取極少量培養液觀察是否有前鞭毛體,一旦發現有前鞭毛體則應立即取數滴培養液轉入新鮮培養基中。
另有培養基根據昆蟲血淋巴液的成份加胎牛血清配製而成。蟲體在此培養基中生長良好,但價格昂貴。
有許多株的利什曼原蟲還可以成功地培養在一些哺乳動物細胞培養液的混合液中,例如MEM、RPMI1640或199培養基。
(二)無鞭毛體培養
利什曼原蟲的無鞭毛體寄生在哺乳動物的單核吞噬細胞內,也可以體外培養在這類細胞內,例如可在巨噬細胞培養株J774G8內培養或在直接從外周血分離的巨噬細胞內培養。前者巨噬細胞分裂,且蟲體大量增殖,但有時會混有前鞭毛體。後者則適用於短期的實驗,雖然蟲體自身增殖,但巨噬細胞並不分裂。無鞭毛體還可以生長在無細胞的培養基中。這種無鞭毛體可以被巨噬細胞迅速吞噬,並在細胞內分裂,可轉化為前鞭毛體。一般培養溫度為33℃,每96小時轉種一次。
防治方法
中國在黑熱病防治工作成績卓著,由於在廣大流行區採取查治病人,殺滅病犬和消滅白蛉的綜合措施,到1958~1960年先後達到了基本消滅的要求。患病人數由1951年的53萬人,至1990年降為360。但為了進一步鞏固現有的防治成果,儘快在全國範圍內達到控制及消滅黑熱病之目的,尚應積極開展黑熱病的防治工作。治療病人 注射低毒高效的葡萄糖酸銻納,療效可達97.4%。抗銻病人採用戊脘脒(pentamidine)、二脒替(stilbamidine)、羥眯替(hydroxystilbamidineisothionate)。經多種藥物治療無效而脾高度腫大且有脾功能亢進者,可考慮脾切除。
控制病犬 對病犬進行捕殺。但對丘陵山區犬類的管理確有一定困難,需尋找有效措施加以控制。
滅蛉、防蛉 在平原地區採用殺蟲劑室內和畜舍滯留噴灑殺滅中華白蛉。在山區、丘陵及荒漠地區對野棲型或偏野棲型白蛉,採取防蛉、驅蛉措施,以減少或避免白蛉的叮刺。
至於自然疫源型流行區的疫源地分布和保蟲宿主等問題仍有待查清,其防治對策也需研究。
