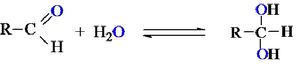性質
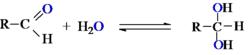 醛與水加成生成同碳二醇(不穩定)
醛與水加成生成同碳二醇(不穩定)同碳二醇極不穩定,非常容易脫水變成醛或酮。可以理解為H2O是弱的親核試劑,因此H2O對羰基加成的反應,平衡常數比較小,傾向於醛酮一方。
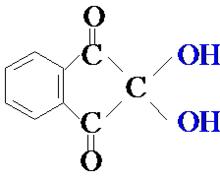 水合茚三酮
水合茚三酮由於O原子電負性大、半徑小,因此其電荷密度相當大,當兩個-OH連在一個C上時,電荷密度太大,使得體系在熱力學上不穩定。然而,當醛酮的羰基碳原子上連有吸電子基團時則穩定存在,如圖所示(水合茚三酮)。
這是因為強吸電子基團增強了羰基的親電活性,使羰基變得極為活潑,能夠與水發生加成反應並生成穩定產物偕二醇。
又如:
1、三氯乙醛被水加成:ClCCHO+HO→ClCCH(OH)(安眠藥)
2、甲醛被水加成:HCHO+HO→HCCH(OH),轉化率100%
3、乙醛被水加成:CHCHO+HO→CH3CH(OH),轉化率58%
由於乙醛的羰基碳與甲基這一給電子基團相連,羰基親電活性被削弱,且位阻增大,因此反應性相對甲醛來說較弱。甲醛則因其高羰基活性和極低位阻而具有極高的反應性。
再如:HCOOH(甲酸)+HO→HC(OH)(原甲酸)
相似化合物
類似地,當一個碳原子上連線了兩個或多個這樣的吸電子基團(-Cl,-Br,-OH和-NH)且其一基團含H時,該結構在熱力學上都是不穩定的,容易發生1,2-消除反應。
如:
1.RR'CClOH→RR'C=O + HCl
2.RR'COHNH→RR'C=NH + HO