分類
在一個水分子中2個氫原子和1個氧原子就是通過化學鍵結合成水分子。由於原子核帶正電,電子帶負電,所以我們可以說,所有的化學鍵都是由兩個或多個原子核對電子同時吸引的結果所形成。化學鍵有3種類型 ,即離子鍵、共價鍵、金屬鍵(氫鍵不是化學鍵,它是分子間力的一種)。
內容
離子鍵
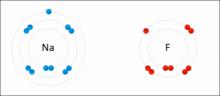 原子相互得失電子,形成離子鍵的過程
原子相互得失電子,形成離子鍵的過程帶相反電荷離子之間的互相作用叫做離子鍵(Ionic Bond),成鍵的本質是陰陽離子間的靜電作用。兩個原子間的電負性相差極大時,一般是金屬與非金屬。例如氯和鈉以離子鍵結合成氯化鈉。電負性大的氯會從電負性小的鈉搶走一個電子,以符合八隅體。之後氯會以-1價的方式存在,而鈉則以+1價的方式存在,兩者再以庫侖靜電力因正負相吸而結合在一起,因此也有人說離子鍵是金屬與非金屬結合用的鍵結方式。而離子鍵可以延伸,所以並無分子結構。
離子鍵亦有強弱之分。其強弱影響該離子化合物的熔點、沸點和溶解性等性質。離子鍵越強,其熔點越高。離子半徑越小或所帶電荷越多,陰、陽離子間的作用就越強。例如鈉離子的微粒半徑比鉀離子的微粒半徑小,則氯化鈉NaCl中的離子鍵較氯化鉀KCl中的離子鍵強,所以氯化鈉的熔點比氯化鉀的高。
定義:離子鍵是由正負離子之間通過靜電作用而形成的,正負離子為球形或者近似球形,電荷球形對稱分布,那么離子鍵就可以在各個方向上發生靜電作用,因此是沒有方向性的。
離子鍵概念:帶相反電荷離子之間的相互作用稱為離子鍵。
成鍵微粒:陰離子、陽離子。
成鍵本質:靜電作用。靜電作用包括陰、陽離子間的靜電吸引作用和電子與電子之間、原子核與原子核之間的靜電排斥作用。(一吸,兩斥)
成鍵原因:①原子相互得失電子形成穩定的陰、陽離子。②離子間吸引與排斥處於平衡狀態。③體系的總能量降低。
存在範圍:離子鍵存在於大多數強鹼、鹽及金屬氧化物中。
 化學鍵
化學鍵一個離子可以同時與多個帶相反電荷的離子互相吸引成鍵,雖然在離子晶體中,一個離子只能與幾個帶相反電荷的離子直接作用(如NaCl中Na+可以與6個Cl-直接作用),但是這是由於空間因素造成的。在距離較遠的地方,同樣有比較弱的作用存在,因此是沒有飽和性的。化學鍵的概念是在總結長期實踐經驗的基礎上建立和發展起來的,用來概括觀察到的大量化學事實,特別是用來說明原子為何以一定的比例結合成具有確定幾何形狀的、相對穩定和相對獨立的、性質與其組成原子完全不同的分子。開始時,人們在相互結合的兩個原子之間畫一根短線作為化學鍵的符號 ;電子發現以後 ,1916年G.N.路易斯提出通過填滿電子穩定殼層形成離子和離子鍵或者通過兩個原子共有一對電子形成共價鍵的概念,建立化學鍵的電子理論。
量子理論建立以後,1927年 W.H.海特勒和F.W.倫敦通過氫分子的量子力學處理,說明了氫分子穩定存在的原因 ,原則上闡明了化學鍵的本質。通過以後許多人 ,特別是L.C.鮑林和R.S.馬利肯的工作,化學鍵的理論解釋已日趨完善。
化學鍵在本質上是電性的,原子在形成分子時,外層電子發生了重新分布(轉移、共用、偏移等),從而產生了正、負電性間的強烈作用力。但這種電性作用的方式和程度有所不同,所以又可將化學鍵分為離子鍵、共價鍵和金屬鍵等。離子鍵是原子得失電子後生成的陰陽離子之間靠靜電作用而形成的化學鍵。離子鍵的本質是靜電作用。由於靜電引力沒有方向性,陰陽離子之間的作用可在任何方向上,離子鍵沒有方向性。只要條件允許,陽離子周圍可以儘可能多的吸引陰離子,反之亦然,離子鍵沒有飽和性。不同的陰離子和陽離子的半徑、電性不同,所形成的晶體空間點陣並不相同。
共價鍵
1.共價鍵(Covalent Bond)是原子間通過共用電子對(電子云重疊)而形成的相互作用。形成重疊電子云的電子在所有成鍵的原子周圍運動。一個原子有幾個未成對電子,便可以和幾個自旋方向相反的電子配對成鍵,共價鍵飽和性的產生是由於電子云重疊(電子配對)時仍然遵循泡利不相容原理。電子云重疊只能在一定的方向上發生重疊,而不能隨意發生重疊。共價鍵方向性的產生是由於形成共價鍵時,電子云重疊的區域越大,形成的共價鍵越穩定,所以,形成共價鍵時總是沿著電子云重疊程度最大的方向形成(這就是最大重疊原理)。共價鍵有飽和性和方向性。
2.原子通過共用電子對形成共價鍵後,體系總能量降低。
共價鍵的形成是成鍵電子的原子軌道發生重疊,並且要使共價鍵穩定,必須重疊部分最大。由於除了s軌道之外,其他軌道都有一定伸展方向,因此成鍵時除了s-s的σ鍵(如H2)在任何方向都能最大重疊外,其他軌道所成的鍵都只有沿著一定方向才能達到最大重疊。 共價鍵的分類
共價鍵有不同的分類方法。
(1) 按共用電子對的數目分,有單鍵(Cl—Cl)、雙鍵(C=C)、三鍵(N≡N,C≡C)等。
(2) 按共用電子對是否偏移分類,有極性鍵(H—Cl)和非極性鍵(Cl—Cl)。
(3) 按提供電子對的方式分類,有正常的共價鍵和配位鍵(共用電子對由一方提供,另一方提供空軌道。
如銨根離子中的N—H鍵中有一個屬於配位鍵)。
 化學鍵
化學鍵(4) 按電子云重疊方式分,有σ鍵(電子云沿鍵軸方向,以“頭碰頭”方式成鍵。如C—C。)和π鍵(電子云沿鍵軸兩側方向,以“肩並肩”方向成鍵。如C=C中鍵能較小的鍵.C=C中有一個σ鍵與一個π鍵。)等
3.舊理論:共價鍵形成的條件是原子中必須有成單電子,自旋方向必須相反,由於一個原子的一個成單電子只能與另一個成單電子配對,因此共價鍵有飽和性。如H原子與Cl原子形成HCl分子後,不能再與另外一個Cl形成HCl2了。
4.新理論:共價鍵形成時,成鍵電子所在的原子軌道發生重疊並分裂,成鍵電子填入能量較低的軌道即成鍵軌道。如果還有其他的原子參與成鍵的話,其所提供的電子將會填入能量較高的反鍵軌道,形成的分子也將不穩定。 像HCl這樣的共用電子對形成分子的化合物叫做共價化合物。
化合物分類
 原子之間依靠化學鍵組成有機小分子
原子之間依靠化學鍵組成有機小分子1.離子化合物:由陽離子和陰離子構成的化合物。
大部分鹽(包括所有銨鹽),強鹼,大部分金屬氧化物,金屬氫化物。 活潑的金屬元素與活潑非金屬元素形成的化合物中不一定都是以離子鍵結合的,如AICI3、FeCl3、BeCl2等不是通過離子鍵結合的。非金屬元素之間也可形成離子化合物,如銨鹽都是離子化合物。
2.共價化合物:主要以共價鍵結合形成的化合物,叫做共價化合物。
非金屬氧化物,酸,弱鹼,少部分鹽,非金屬氫化物。
3.在離子化合物中一定含有離子鍵,可能含有共價鍵。在共價化合物中一定不存在離子鍵。
金屬鍵
1.概述:化學鍵的一種,主要在金屬中存在。由自由電子及排列成晶格狀的金屬離子之間的靜電吸引力組合而成。由於電子的自由運動,金屬鍵沒有固定的方向,因而是非極性鍵。金屬鍵有金屬的很多特性。例如一般金屬的熔點、沸點隨金屬鍵的強度而升高。其強弱通常與金屬離子半徑成逆相關,與金屬內部自由電子密度成正相關(便可粗略看成與原子外圍電子數成正相關)。
2.改性共價鍵理論:在金屬晶體中,自由電子作穿梭運動,它不專屬於某個金屬離子而為整個金屬晶體所共有。這些自由電子與全部金屬離子相互作用,從而形成某種結合,這種作用稱為金屬鍵。由於金屬只有少數價電子能用於成鍵,金屬在形成晶體時,傾向於構成極為緊密的結構,使每個原子都有儘可能多的相鄰原子(金屬晶體一般都具有高配位數和緊密堆積結構),這樣,電子能級可以得到儘可能多的重疊,從而形成金屬鍵。上述假設模型叫做金屬的自由電子模型,稱為改性共價鍵理論。這一理論是1900年德魯德(drude)等人為解釋金屬的導電、導熱性能所提出的一種假設。這種理論先後經過洛倫茨(Lorentz,1904)和佐默費爾德(Sommerfeld,1928)等人的改進和發展,對金屬的許多重要性質都給予了一定的解釋。但是,由於金屬的自由電子模型過於簡單化,不能解釋金屬晶體為什麼有結合力,也不能解釋金屬晶體為什麼有導體、絕緣體和半導體之分。隨著科學和生產的發展,主要是量子理論的發展,建立了能帶理論。
定域鍵
只存在於兩個原子之間的共價鍵。只包含定域鍵的多原子分子可以看成是由相對獨立的兩個原子之間的化學鍵把原子連線起來形成的,這是忽略了相鄰化學鍵的影響,而把描述雙原子分子中化學鍵的方法用到多原子分子的定域鍵上。如乙烯中有一個C-C和四個C-H σ鍵、一個C-C π鍵。定域鍵具有比較恆定的鍵性質。例如一定類型定域鍵的鍵長、鍵偶極矩、鍵極化度、鍵力常數、鍵能等在不同分子中近似保持不變。因此,分子的有關廣延性質可近似表示為相應的鍵性質之和。定域鍵的這種特點在化學中得到廣泛的套用,例如從鍵能計算分子的原子化能近似值。這種模型較好地反映了由鍵上電子云所確定的分子性質如鍵能、鍵長、鍵角、鍵偶極、鍵極化度等。 這種圍繞兩個原子的分子軌道成為 定域軌道。
極性鍵
 化學鍵
化學鍵在化合物分子中,不同種原子形成的共價鍵,由於兩個原子吸引電子的能力不同,共用電子對必然偏向吸引電子能力較強的原子一方,因而吸引電子能力較弱的原子一方相對的顯正電性。這樣的共價鍵叫做極性共價鍵,簡稱極性鍵。
舉例:HCl分子中的H-Cl鍵屬於極性鍵
有一個簡單的判斷極性鍵與非極性鍵的方法,比較形成該化合物中各原子的原子量,一般來說,相對原子質量越大的原子吸引電子能力更強。但是要注意,有極性鍵構成的化合物,不一定是極性化合物,例如甲烷,它就是有極性鍵的非極性分子(原因是正負電荷中心重合)。
非極性鍵
由同種元素的原子間形成的共價鍵,叫做非極性共價鍵。同種原子吸引共用電子對的能力相等,成鍵電子對勻稱地分布在兩核之間,不偏向任何一個原子,成鍵的原子都不顯電性。非極性鍵可存在於單質分子中(如H2中H—H鍵、O2中O=O鍵、N2中N≡N鍵),也可以存在於化合物分子中(如C2H2中的C—C鍵)。非極性鍵的鍵偶極矩為0。以非極性鍵結合形成的分子都是非極性分子。存在於非極性分子中的鍵並非都是非極性鍵,如果一個多原子分子在空間結構上的正電荷幾何中心和負電荷幾何中心重合,那么即使它由極性鍵組成,那么它也是非極性分子。由非極性鍵結合形成的晶體可以是原子晶體,也可以是混合型晶體或分子晶體。例如,碳單質有三類同素異形體:依靠C—C非極性鍵可以形成正四面體骨架型金剛石(原子晶體)、層型石墨(混合型晶體),也可以形成球型碳分子富勒烯C60(分子晶體)。
舉例:Cl2分子中的Cl-Cl鍵屬於非極性鍵
配位鍵
又稱配位共價鍵,是一種特殊的共價鍵。當共價鍵中共用的電子對是由其中一原子獨自供應時,就稱 配位鍵。配位鍵形成後,就與一般共價鍵無異。成鍵的兩原子間共享的兩個電子不是由兩原子各提供一個,而是來自一個原子。例如氨和三氟化硼可以形成配位化合物:圖片式中→表示配位鍵。在F和B之間的一對電子來自N原子上的孤對電子。
泡利原理
 化學鍵
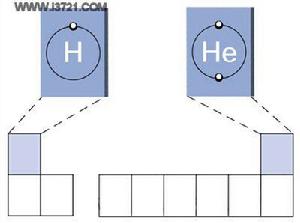
化學鍵泡利原理髮現:高分辨光譜事實揭示核外電子除空間運動外,還存在著一種奇特的量子化運動,人們稱其為自旋運動,用自旋磁量子數( spin m.q.n)表示。這個原理由泡利首先提出。
泡利不相容原理內容:每個軌道最多可以容納兩個自旋相反的電子,常用“↑↓”來表示。
原子核也可以存在淨自旋。由於熱平衡,通常這些原子核都是隨機朝向的。但對於一些特定元素,例如氙-129,一部分核自旋也是可能被極化的,這個狀態被叫做超極化,在核磁共振成像中有很重要的套用。
洪特規則
洪特規則內容:當電子排布在同一能級的不同軌道時,基態原子中的電子總是優先單獨占據一個軌道,且自旋狀態相同。這個規則由洪特首先提出,稱為洪特規則。
基態原子的電子排布遵循能量最低原理、泡利原理和洪特規則。用構造原理得到的電子排布式給出了基態原子核外電子在能層和能級中的排布,而電子排布圖還給出了電子在原子軌道中的排布。另外,我們通常所說的電子排布指的是基態原子的電子排布。
對於同一個電子亞層,當電子排布處於
全滿(s^2.p^6.d^10.f^14)
半滿(s^1.p^3.d^5.f^7)
全空(s^0、p^0、d^0、f^0)
時比較穩定。
第二,第五主族的第一電離能大于于之相鄰的主族
鍵合距離
鍵合距離是指兩個或以上的原子核之間形成化學鍵所必需的最短距離。