百科名片
中心性漿液性脈絡膜視網膜病變簡稱“中漿”,該病累及脈絡膜和視網膜,目前較為通用的名稱為中心性漿液性脈絡膜視網膜病變。中漿患者中A型行為特徵者比較常見,發病前常伴有應激情況發生,如精神緊張、過度勞累等,此時患者血液中兒茶酚胺和皮質醇水平升高。患者常表現為輕度視力下降,視物變形、變小並伴色覺改變;中心或旁中心暗點;對比敏感度降低;由於黃斑區漿液性脫離導致患者遠視性屈光改變等。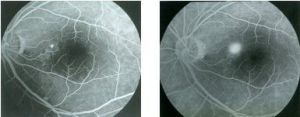 中心性漿液性脈絡膜視網膜病變
中心性漿液性脈絡膜視網膜病變西醫學名:中心性漿液性脈絡膜視網膜病變
主要症狀:輕度視力下降,視物變形、變小並伴色覺改變,中心或旁中心暗點,對比敏感度降低等
主要病因:A型行為特徵,抽菸,酗酒,自身免疫病,高血壓,腎上腺腫瘤等
疾病簡介
中心性漿液性脈絡膜視網膜病變(簡稱“中漿”)最初由vonGraefe報告,直至1965年有了螢光素眼底血管造影(FFA)技術以後,Maumenee才肯定了中漿是視網膜色素上皮(RPE)屏障功能受損導致漿液性RPE和(或)神經視網膜脫離;1967年gass對該病發病機制和臨床特徵進行了經典描述,並將該病稱為特發性中心性漿液性脈絡膜病變。由於該病累及脈絡膜和視網膜,目前較為通用的名稱為中心性漿液性脈絡膜視網膜病變。中漿患者中,A型行為特徵者比較常見,發病前常伴有應激情況發生,此時患者血液中兒茶酚胺和皮質醇水平升高。在動物實驗中,反覆注射去甲腎上腺素和糖皮質激素即能誘發類似中漿的臨床表現。其它高危因素還包括抽菸、酗酒、套用抗生素和抗組胺藥物、自身免疫病、高血壓、腎上腺腫瘤等。多數中漿患者急性發病後4~6個月自行好轉,視力多可恢復正常,所以,被認為是一種自限性疾病。但部分患者視物變形、對比敏感度下降、色覺異常等視功能改變可持續存在。少數患者病程遷延持續6個月以上。病變區域瀰漫性RPE失代償者,則定義為慢性中漿。這部分患者病變多較嚴重,常伴有永久性視力下降。長期遷延不愈可繼發脈絡膜新生血管(CNV),甚至導致永久視力喪失。中漿患者首次發病後,約30%~50%可再次復發。10%患者可復發3次以上。
疾病分類
急性中漿
病程6個月以內,具有典型中漿表現,眼底黃斑區視網膜半透明泡狀隆起,中心凹光反射消失,漿液脫離區內或毗鄰可伴有水泡樣RPE脫離。FFA表現為一個或多個RPE水平的螢光素滲漏,隨造影過程表現為墨漬或冒煙狀滲漏擴大。慢性中漿
中漿患者病程遷延6個月以上,眼底表現為瀰漫性視網膜色素上皮層失代償,FFA常無明確滲漏點,而OCT檢查有明確漿液性脫離,此時稱為慢性中漿(Chroniccentralserouschorioretinopathy,CSCR)。慢性中漿長年遷延不愈可繼發脈絡膜新生血管(chorodalneovascularization,CNV),甚至導致永久視力喪失。大泡性視網膜脫離
中漿患者如果接受了不適當或由於全身疾病必須使用的糖皮質激素治療,導致漿液性脫離加重,表現為下方視網膜滲出性大泡性脫離,此為重症中漿的表現,可伴有RPE撕裂與永久視力喪失。發病原因
中漿患者中A型行為特徵者比較常見,發病前常伴有應激情況發生,如精神緊張、過度勞累等,此時患者血液中兒茶酚胺和皮質醇水平升高[2]。在動物實驗中,反覆注射去甲腎上腺素和糖皮質激素即能誘發類似中漿的臨床表現。其它高危因素還包括抽菸、酗酒、套用抗生素和抗組胺藥物、自身免疫病、高血壓、腎上腺腫瘤等。發病機制
既往對中漿發病機制的認識主要來源於FFA檢查結果。由於FFA檢查可發現明確的RPE滲漏點,故認為中漿原發病變位於RPE層。但導致RPE屏障功能受損以及漿液性RPE和(或)神經視網膜脫離的深層次原因並不清楚。吲哚青綠脈絡膜血管造影(ICGA)用於中漿的臨床研究後發現,中漿患者病灶對應處脈絡膜血管通透性過高,導致脈絡膜組織內靜水壓過高,引發局部RPE脫離,進而機械性破壞RPE屏障,液體滲漏進入神經視網膜下,導致視網膜神經上皮脫離。病理生理
有關皮質類固醇激素和兒茶酚胺在中漿發病中的作用尚不完全清楚。推測腎上腺素導致脈絡膜血管收縮與血流改變,皮質類固醇激素升高能增加毛細血管脆性和通透性,進而導致脈絡膜循環失調。皮質類固醇激素還可以直接損傷RPE細胞或其間的緊密連線,延緩受損RPE細胞的修復過程。實驗動物模型顯示,升高的皮質類固醇激素和兒茶酚胺水平能擾亂脈絡膜毛細血管血流的自身調節。臨床表現
男性比女性更容易患病,約占全部患者的80%,發病年齡多在30-50之間,20%-40%的患者發病累及雙側眼。患者輕度視力下降,視物變形、變小並伴色覺改變;中心或旁中心暗點;對比敏感度降低;由於黃斑區漿液性脫離導致患者遠視性屈光改變。
眼底檢查,黃斑或黃斑區外卵圓形或圓形視網膜神經上皮層脫離,脫離的視網膜呈半透泡狀隆起,隆起的邊緣可見反光暈,中心凹光反射消失,脫離區視網膜下可有黃白色點狀沉著物,對應螢光素血管造影滲漏點部位常可見脫色素黃色小點,神經上皮脫離區內或毗鄰可伴有水泡樣RPE脫離,病程較久者可伴色素紊亂或RPE萎縮區。少數患者表現為單純漿液性色素上皮脫離,並可以長期存在。
偶有患者在漿液性脫離區見到淺灰色混濁,組織病理學研究發現視網膜下或/和RPE下有纖維素存在,隨著濃度的增加,纖維素分子聚合,形成卵黃色或灰色混濁,此為伴有纖維素滲出的中漿,在PDT治療後隨著RPE滲漏終止該滲出迅速消退。
一些患者病程遷延6個月以上,眼底表現為瀰漫性視網膜色素上皮層失代償,FFA常無明確滲漏點,而OCT檢查有明確漿液性脫離,此時稱為慢性中漿(Chroniccentralserouschorioretinopathy,CSCR)。慢性中漿長年遷延不愈可繼發脈絡膜新生血管(chorodalneovascularization,CNV),甚至導致永久視力喪失。
一些患者由於接受了不適當或由於全身疾病必須使用的糖皮質激素治療,導致漿液性脫離加重,表現為下方視網膜滲出性大泡性脫離,此為重症中漿的表現,可伴有RPE撕裂與永久視力喪失。
診斷鑑別
特殊檢查
1.螢光素眼底血管造影(FFA):中漿典型的FFA表現是一個或多個RPE水平的螢光素滲漏,隨造影過程表現為墨漬或冒煙狀滲漏擴大,造影晚期在視網膜脫離區形成淡淡的盤狀高螢光。慢性中漿患者可不表現為典型的螢光素滲漏點,代之以後極部視網膜瀰漫的RPE脫色素或色素沉著引起的窗樣透見螢光或色素遮蔽螢光,在此基礎上有些患者合併存在RPE滲漏點。對於大泡性視網膜脫離恢復後的患者,可見到由後極向下的帶狀透見螢光區,此為RPE萎縮所致。大多數中漿患者合併漿液性RPE脫離,FFA表現為造影后期界限清楚、形態大小不變、染色均勻的高螢光池。中漿患者螢光素眼底血管造影2.中漿的吲哚青綠血管造影(ICGA):在造影早期和中期可見脈絡膜血管擴張滲漏所致的高螢光區。這些高螢光區的範圍常毗鄰或包含FFA滲漏點位置。
中漿患者吲哚青綠脈絡膜血管造影3.光相干斷層掃描(OCT):OCT能定性、定量檢測視網膜和RPE的漿液性脫離並追蹤視網膜下液消退過程,為臨床病程提供了客觀的檢測方法。
中漿患者相干光斷層掃描4.視野:急性期中心視野存在相對或絕對中心暗點,尤其是Amsler表檢查暗點更明確,且有視物變形,恢復期後中心視野可以正常。但是對於病程長的病例,或反覆多次發作病例,中心視野可能存在相對的暗點。
診斷要點
1.患者有典型臨床表現,急性期輕度視力下降,視物變形、變小並伴色覺改變;慢性中漿患者可有中度甚至重度視力下降伴視物變形、變小、色覺異常等改變。眼底檢查可見黃斑區典型視網膜神經上皮伴或不伴視網膜色素上皮脫離。2.FFA檢查可見典型RPE滲漏點,慢性中漿表現為後極部RPE失代償所致的瀰漫性透見螢光或伴有RPE滲漏點。
3.ICGA檢查可見病灶區域脈絡膜血管擴張滲漏所致的高螢光。
4.OCT檢查顯示後極部漿液性視網膜脫離或伴有漿液性RPE脫離。
鑑別診斷
根據臨床症狀、典型的眼底表現和FFA、ICGA可以做出診斷。但須與下列眼底疾病鑑別。1.脈絡膜腫物。無論是良性或惡性,無論位於後極部或周邊部腫物,均可能合併漿液性黃斑脫離,最多見於脈絡膜血管瘤。對這些病例,套用間接檢眼鏡檢查、FFA、ICGA以及眼超聲檢查,可以明確診斷。
2.先天性視乳頭小凹(congenitalopticpit):該病為先天性視神經發育異常,常在合併黃斑區漿液性脫離導致視力下降或視物變形時被發現,容易與中漿混淆。鑑別要點為(1)視神經乳頭有典型的小凹狀缺損;多位於視乳頭顳側邊緣;(2)FFA顯示小凹處早期低螢光,晚期高螢光不退,黃斑脫離區無RPE滲漏點;(3)OCT檢查顯示黃斑脫離與視乳頭小凹相交通。
3.下方裂孔或較小裂孔的孔源性視網膜脫離:孔源性視網膜脫離剛剛波及黃斑區時可類似中漿症狀,散瞳詳細檢查眼底不難明確診斷。
4.黃斑部脈絡膜新生血管(choroidalneovascularization簡稱CNV):包括濕性老年黃斑變性以及特發性脈絡膜新生血管等一大類疾病。典型CNV病灶黃斑區灰黃色滲出伴出血,與“中漿”易於鑑別。當CNV很小合併黃斑漿液脫離且不伴出血時與“中漿”不易鑑別,這一類病例要靠FFA以及ICGA鑑別。
5.後葡萄膜炎如原田氏病,在疾病早期可以引起黃斑區漿液性視網膜淺脫離,但該病還同時合併玻璃體炎、視盤充血、全身病變、內界膜紊亂以及對抗炎治療敏感,通過仔細詢問病史、檢查眼前節和後節及FFA,可以作出正確診斷。
6.息肉狀脈絡膜血管病變(Polypoidalchoroidalvasculopathy,PCV):典型PCV的臨床診斷比較容易,眼底黃斑區視網膜下濃密出血,ICGA顯示脈絡膜異常血管網以及脈絡膜毛細血管末端囊樣擴張。但孤立靜止的的PCV表現可類似於中漿,這些不典型的PCV病例可表現為孤立的RPE脫離或者神經上皮脫離,甚至表現為中漿樣的RPE滲漏點。此時,ICGA在鑑別診斷上將起到決定性作用,中漿患者ICGA表現為脈絡膜血管的擴張和滲漏,而PCV時ICGA表現為脈絡膜毛細血管末端囊樣擴張。甚至有一些病例,年輕時曾患中漿,年老時呈現典型的PCV表現,提示中漿和PCV可能存在某種內在聯繫。
疾病治療
基於中漿屬於自限性疾病這一認識,很多眼科醫生奉行的中漿治療策略是採用保守療法。一種情況是不給予任何治療,對疾病採取聽之任之的態度;另外一種情況是給予患者維生素C、維生素B1、路丁、地巴唑、肌酐等“安慰劑”治療。由於中漿的自限性,這些治療似乎也能使患者獲得滿意的“療效”。對於保守治療,多數患者於患病4~6個月後自行好轉,但仍有5%的患者遷延不愈或病情加重導致視力嚴重受損。此外,中漿比較常用的治療手段是雷射光凝治療。既往對中漿發病機制的認識主要來源於FFA檢查結果。由於FFA檢查可發現明確的RPE滲漏點,故認為中漿原發病變位於RPE層。但導致RPE屏障功能受損以及漿液性RPE和(或)神經視網膜脫離的深層次原因並不清楚。而中漿雷射光凝治療的理論依據是建立在FFA檢查發現的RPE滲漏點基礎之上,採用雷射光凝治療是通過雷射的熱效應凝固RPE滲漏點從而達到治療目的。但臨床實踐表明,雷射光凝治療可以封閉RPE滲漏點,加快漿液性RPE脫離的吸收,縮短病程,有利於視力恢復;但長期觀察發現,雷射光凝治療並未顯示可以提高患者遠期療效或減少復發率。
吲哚青綠脈絡膜血管造影(ICGA)用於中漿的臨床研究後發現,中漿患者病灶對應處脈絡膜血管通透性過高,導致脈絡膜組織內靜水壓過高,引發局部RPE脫離,進而機械性破壞RPE屏障,液體滲漏進入神經視網膜下,導致視網膜神經上皮脫離。這就進一步加深了對中漿病理基礎的本質的認識。所以,目前的觀點是,中漿發病是由於脈絡膜毛細血管擴張和滲漏所致,而雷射光凝不能解決脈絡膜毛細血管的擴張和滲漏,因此治療後仍有不少患者復發。除此之外,對於中心凹下或黃斑無血管區以內的滲漏點顯然不適合雷射治療;對於採用雷射治療的患者,還可能引起旁中心暗點甚至損傷Bruch膜導致CNV形成。近年來國內外文獻報導採用PDT治療中漿獲得成功,其機制為PDT導致脈絡膜毛細血管網栓塞,從而阻止了由於脈絡膜毛細血管通透性增加導致的滲漏。
採用PDT治療中漿最初主要是針對繼發於慢性中漿的CNV。對於這一類患者,採用治療滲出型AMD的PDT治療參數取得了較好的療效。Yannuzzi和CardilloPiccolino等最先採用吲哚青綠(ICG)介導的PDT治療未合併CNV的慢性中漿,治療後患者視力平均上升0.5到1行,FFA檢查顯示滲漏消失,黃斑區滲出吸收;隨訪約6個月均未出現復發。表明PDT治療慢性中漿有較好的效果。BattagliaParodiM等則首先報導了採用以注射用維替泊芬介導的PDT治療慢性中漿取得成功。Ober等報導了採用PDT治療急性中漿的臨床觀察,隨訪6個月視力平均從20/80上升至20/40,沒有出現治療相關的併發症。Chan等報導使用半量藥物的PDT治療急性中漿的前瞻、隨機、雙盲、安慰劑對照的臨床研究。注射用維替泊芬劑量採用常規劑量的一半,藥物注射時間為8min,注射完畢2min開始雷射照射。治療後1年的結果顯示,治療組94.9%患眼黃斑區視網膜下滲漏消退,而對照組僅有57.9%視網膜下液消失;治療組100.0%視力穩定或提高,而對照組僅有78.9%的患者視力穩定或提高。
研究發現,採用注射用維替泊芬的PDT治療可以導致脈絡膜血管改變,例如使擴張和充血的脈絡膜血管口徑恢復正常,同時減少血管外滲漏。但值得深入思考的問題是,PDT治療中漿和治療CNV是遵循同樣的機制嗎?眾所周知,注射用維替泊芬治療CNV的理論基礎是作為增生活躍組織的CNV內皮細胞上有較多低密度脂蛋白(LDL)受體,LDL作為載體運送注射用維替泊芬與CNV內皮細胞結合,再與雷射發生光動力反應,其結果是光動力反應產物活性氧自由基攻擊CNV內皮細胞導致脈絡膜的新生血管閉鎖。因此,很容易想到,中漿患者病變區域擴張的脈絡膜血管是否也可以與LDL結合,其結合能力是否與CNV相同?Barcelona等的研究回答了這一問題。該研究檢測了正常人和增生性疾病患者眼脈絡膜毛細血管的LDL受體,發現正常人眼脈絡膜毛細血管有較弱的LDL受體表達,而增生前期糖尿病視網膜病變和增生性鐮狀細胞視網膜病變則有較強的LDL受體表達。Schlötzer-Schrehardt等更是直接證明了人眼正常脈絡膜視網膜經PDT治療後發生生理性脈絡膜毛細血管閉鎖而未累及深層脈絡膜血管。
PDT治療中漿的成功,引起了眼科醫生的關注。尤其是Chan等採用半劑量注射用維替泊芬PDT成功治療中漿,啟發人們思考傳統的治療CNV的PDT治療方案可能並不適用於中漿的治療,其中的內涵即包括了PDT治療中漿的安全性,也包括減低藥物劑量可能會降低患者的經濟負擔。目前國內注射用維替泊芬全劑量藥價每支為16000元,半量藥價仍高達8000元,使臨床推廣套用受到極大限制。如能找到治療中漿的最低安全有效劑量,則能進一步降低治療成本,使更多患者受益。
基於以上思考,筆者於2007年開始觀察採用不同劑量注射用維替泊芬治療中漿的療效,採用PDT治療急性中漿患者15例15隻眼,按就診順序,患者1至7分別採用PDT治療CNV的注射用維替泊芬常規劑量的70%、60%、50%、40%、30%、20%、10%。在發現臨界有效劑量為20%~30%時,重複驗證20%和30%劑量。結果顯示,30%常規劑量為最低有效劑量,進而對其餘患者均採用30%常規劑量加以驗證。以上治療除了注射用維替泊芬劑量外,其餘治療參數與治療CNV相同。雷射照射的光斑大小根據ICGA檢查所顯示的脈絡膜毛細血管擴張區域確定,雷射光斑需覆蓋滲漏點所在的脈絡膜毛細血管擴張區。採用70%常規劑量治療的1例患者治療後黃斑區完全平復,FFA檢查滲漏消退,但隨診至1個月時PDT治療區發生CNV,予眼內注射抗血管內皮生長因子單克隆抗體bevacizumab(avastin)1.25mg後新生血管退行。其餘採用30%~60%常規劑量的患者FFA檢查所見螢光滲漏與ICGA檢查所見的脈絡膜血管滲漏完全消退,光相干斷層掃描(OCT)檢查黃斑區視網膜下液在治療後1~3周內逐漸吸收,視力均不同程度提高。2例採用10%、20%常規劑量無效者再次治療採用30%劑量有效。除70%常規劑量外,其餘劑量患者隨診期間未發生其它併發症。表明PDT治療急性中漿時注射用維替泊芬的最低安全有效劑量大約為常規治療CNV劑量的30%,採用此劑量治療急性中漿安全有效,可縮短患者病程,同時減輕患者的經濟負擔。這一研究結果發表於2009年RETINA雜誌。
雖然部分中漿的臨床過程具有一定的自限性,但較長的病程仍將產生不可逆的視功能損傷,如有安全有效的治療方法,仍建議對其進行積極治療;對比以往的藥物和雷射光凝治療,降低藥物劑量的PDT治療中漿安全、有效,值得進一步探索和推廣。這是我們目前對中漿治療的基本觀點。
中漿的其他治療還包括減少患者應激因素,停止使用糖皮質激素,降低血壓,減少血液中兒茶酚胺、糖皮質激素濃度等針對病因的治療。也有嘗試採用微脈衝雷射、經瞳孔溫熱療法、眼內注射抗血管內皮生長因子藥物等治療。但迄今這些方法並未獲得廣泛認可而成為臨床選擇的共識。[1-2]
