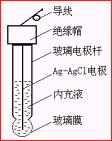
玻璃電極實驗過程
當玻璃膜與試液接觸時,由於外部試液與玻璃膜的外水化層,以及內參比溶液與玻璃膜的內水化層中,H+的濃度不同,H+就會從高濃度向低濃度擴散。擴散的結果,破壞了界面附近原來正負電荷分布的均勻性。於是,在兩相界面附近就形成雙電層結構,從而產生了相界電位(E外和E內)。玻璃電極的膜電位就等於二者之差,即E膜=E外-E內;可見,膜電位的產生不是由於電子的得失和轉移,而是離子交換和擴散的結果。
從理論上講,若內參比溶液和外參比溶液中,H+的濃度完全相同,則玻璃電極的膜電位應該為零,但實際上它並不等於零。
產生原因
這是由於膜內外兩個表面情況不一致(如組成不均勻、表面張力不同、水化程度不同等)而引起的。這時的膜電位稱為不對稱電位(用E不表示),其大小約為1mV~30mV。
解決方法
一般的玻璃電極,在剛浸入溶液中時,其不對稱電位較大,隨著浸泡時間的增加,不對稱電位要下降,最後達到恆定。