【通用名】Ivacaftor
2012年1月20日,Vertex製藥公司的Kalydeco(通用名:Ivacaftor)獲得美國食品藥品管理局(FDA)批准,用於治療囊性纖維化跨膜轉導調節器(CFTR)基因發生了特定的G551D突變的年齡≥6歲的罕見囊性纖維化(CF)患者。
適應證和用途
KALYDECO被分類為一種囊性纖維化跨膜電導調節器(CFTR)增效劑。KALYDECO適用於年齡6歲和以上在CFTR基因中有一種G551D突變囊性纖維化(CF)患者的治療。如患者的基因型未知,應使用FDA批准的CF突變試驗檢測G551D突變的存在。
使用限制
KALYDECO對在CFTR基因中F508del突變純合子CF患者無效和未曾研究CF其它患者群。
劑量和給藥方法
在成年和兒童年齡 6歲和以上中的給藥信息對成年和兒童患者年齡6歲和以上的推薦KALYDECO劑量是150 mg片口服每12小時(300 mg每天總量)與含脂肪食物。適當的含脂肪食物實例包括蛋,黃油,花生黃油,乳酪比薩,等。[見臨床藥理學(12.3)和患者諮詢資料(17.4)].
對有肝受損患者劑量調整對有中度肝受損患者KALYDECO的劑量應減低至150 mg每天1次(Child-Pugh類別B)。有嚴重肝受損患者(Child-Pugh類別C)應在KALYDECO劑量150 mg每天次或頻數更低謹慎使用[見特殊人群中使用 (8.6), 臨床藥理學(12.3),和患者諮詢資料(17.3)]。
對服用CYP3A抑制劑藥物患者的劑量調整當KALYDECO正在與強CYP3A抑制劑(如,酮康唑)共同給藥時劑量應減低至150 mg每周2次。當與中度CYP3A抑制劑共同給藥時(如,氟康唑)KALYDECO的劑量應減低至150 mg每天1次。應避免含柚子汁或塞維亞桔子食物[見藥物相互作用(7.1), 臨床藥理學(12.3),和患者諮詢資料(17.2)]。
劑型和規格
150 mg片。
禁忌證
不知道。
警告和注意事項
轉氨酶(ALT或AST) 升高有CF患者接受KALYDECO曾報導轉氨酶升高。建議在開始KALYDECO前,治療頭一年期間每3個月,和其後每年評估ALT和AST。發生轉氨酶水平增加患者應被嚴密監視直至異常解決。在有ALT或AST大於正常上限(ULN)的5倍患者中應中斷給藥。轉氨酶升高解決後, 考慮恢復KALYDECO給藥的獲益和風險[見不良反應(6)].
與CYP3A誘導劑同時使用KALYDECO與強CYP3A誘導劑,例如利福平使用,實質上減低ivacaftor的暴露,可能減低KALYDECO治療有效性。所以,建議KALYDECO不要與強CYP3A誘導劑(如,利福平, 聖約翰草)共同給藥[見藥物相互作用(7.2)和臨床藥理學(12.3)]。
不良反應
在說明書的其它章節更詳細討論下列不良反應:
(1)轉氨酶升高[見警告和注意事項(5.1)]
臨床試驗經驗
因為臨床試驗是在廣泛不同情況下進行的,臨床試驗觀察到不良反應率不能與另藥臨床試驗發生率直接比較而且可能不反映實踐中觀察到的發生率。
KALYDECO的總體安全性圖形是根據來自安慰劑-對照臨床試驗來自CFTR基因中有一種G551D突變或是對F508del突變純合子的353例有CF患者的合併數據。353例患者中,50%患者是女性和97%是高加索人;221例接受KALYDECO和132例接受安慰劑來自16至48周。用KALYDECO治療患者年齡是6和53歲間。
在這些試驗中,由於不良反應提前終止研究藥物患者比例對KALYDECO-治療患者是2%而對安慰劑-治療患者為5%。由研究中考慮嚴重的不良反應是否藥物-相關,在KALYDECO-治療患者發生更頻,包括腹痛,增加肝酶,和低血糖。.
總而言之,在353例有CF患者最常見不良反應是頭痛(17%),上呼吸道感染(16%),鼻充血(16%),噁心(10%),皮疹(10%),鼻炎(6%),頭暈(5%),關節痛(5%),和痰中細菌(5%)。
下面是根據兩項雙盲,安慰劑-對照48-周臨床試驗總共213例在CFTR基因中有一種G551D突變有CF患者年齡6至53歲和用KALYDECO 150 mg口服治療或安慰劑每天2次的不良反應的發生率。表1 顯示在兩項雙盲,安慰劑-對照試驗中在CFTR基因中有G551D突變有CF患者KALYDECO-治療發生 ≥8%還比安慰劑-治療患者發生率較高的不良反應。
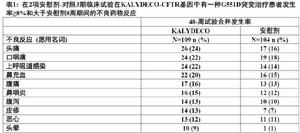 表1
表1感染和蟲染:鼻炎
調查研究:穀草轉氨酶升高,痰中細菌,血糖增加,肝酶增加
肌肉骨骼和結締組織疾病:關節痛,肌肉骨骼胸痛,肌痛
神經系統疾病:竇性頭痛
呼吸,胸和縱隔疾病:咽紅斑,胸痛,鼻竇充血,喘息
皮膚和皮下組織疾病:痤瘡
實驗室異常
轉氨酶升高:在四周期間, 安慰劑-對照臨床研究,在KALYDECO-治療患者中最高轉氨酶(ALT或AST)的發生率 >8,>5或>3 × ULN分別是2%,3%和6%而安慰劑-治療患者分別2%,2%和8%。2例患者(2%)用安慰劑和1例用KALYDECO患者(0.5 %)所有 >8 ×ULN永遠終止治療對升高的轉氨酶。2例用KALYDECO治療患者報導有肝轉氨酶升高嚴重的不良反應與之比較安慰劑無[見警告和注意事項(5.1)]。
藥物相互作用
其它藥物影響ivacaftor的潛能
CYP3A抑制劑Ivacaftor是一種敏感的CYP3A底物。與酮康唑,一種強CYP3A抑制劑共同給藥,顯著地增加ivacaftor暴露[用曲線下面積(AUC)測量]8.5-倍。所以,建議與強CYP3A抑制劑,例如酮康唑, 伊曲康唑[itraconazole], 泊沙康唑[posaconazole],伏立康唑[voriconazole],泰利黴素[telithromycin],和克拉黴素[clarithromycin]共同給藥時減低KALYDECO劑量至150 mg一周2次。
與氟康唑,一種CYP3A中度抑制劑共同給藥,增加ivacaftor暴露3-倍。所以, 建議同時服用中度CYP3A抑制劑患者,例如氟康唑和紅黴素[Erythromycin],減低KALYDECO劑量至150 mg每天1次。
KALYDECO與柚子汁,含一種或以上成分中度抑制CYP3A的共同給藥可能增加ivacaftor的暴露。所以,用KALYDECO治療時應避免含柚子汁或塞維亞桔子食物[見臨床藥理學(12.3)]。
與利福平,一種強CYP3A誘導劑共同給藥顯著減低ivacaftor暴露(AUC)約9-倍。所以,建議不與強CYP3A誘導劑,例如利福平、利福布汀[rifabutin]、苯巴比妥[Phenobarbital]、卡馬西平[carbamazepine]、苯妥英[phenytoin]、和聖約翰草共同給藥[見警告和注意事項(5.2)和臨床藥理學(12.3)].
Ivacaftor影響其它藥物的潛能
Ivacaftor及其M1代謝物有抑制CYP3A和P-gp的潛能。與咪達唑侖[midazolam],一個敏感的CYP3A底物共同給藥,增加咪達唑侖暴露1.5-倍,與CYP3A被ivacaftor的弱抑制作用。KALYDECO的給藥可能增加CYP3A/或P-gp底物藥物的全身暴露,可能增加或延長其治療效應和不良事件。所以,建議當KALYDECO與CYP3A和/或P-gp底物,例如地高辛[digoxin],環孢黴素[cyclosporine],和他克莫司[Tacrolimus]共同給藥謹慎[見臨床藥理學(12.3)]。
特殊人群中使用
妊娠致畸效應: 妊娠類別B。在妊娠婦女中沒有KALYDECO的適當和良好-對照研究。在大鼠中在約為最大推薦人用(MRHD)(根據vacaftor及其代謝物AUC之和在母體劑量200 mg/kg/day)的6倍,Ivacaftor無致畸胎性。在兔中在MRHD(基於母體劑量100 mg/kg/day,分別對ivacaftor AUC)的約12倍,Ivacafto無致畸胎性。妊娠大鼠和兔中觀察到ivacafto胎盤轉運。因為動物生殖研究並非總能預測人反應,妊娠期間只有明確需求才應使用KALYDECO。
哺乳母親Ivacaftor排泄至哺乳雌性大鼠乳汁中。Ivacaftor很可能排泄至人乳汁。沒有人研究ivacaftor對哺乳嬰兒的影響。當給予哺乳婦女KALYDECO應謹慎。
兒童使用在6至7歲CFTR基因中有G551D突變CF患者的2項安慰劑-對照臨床試驗曾顯示KALYDECO的安全性和療效。試驗1評價161例12歲或以上有CF患者和試驗2評價52例6至11歲有CF患者[見臨床研究(14.1)]。
尚未確定KALYDECO在年齡6歲更小CF患者的安全性和療效。
CF很大程度是一種兒童和年輕成人的疾病。KALYDECO的臨床試驗沒有包括足夠數65歲和以上患者以確定他們是否與較年輕患者反應不同。
肝受損對輕度肝受損患者(Child-Pugh類別A)無需調整劑量。中度肝受損患者(Child-Pugh類別B)建議減低劑量至150 mg每天1次。未曾在嚴重肝受損患者進行研究(Child-Pugh類別C)但預計暴露較高於中度肝受損患者。所以,嚴重肝受損患者中權衡治療風險和獲益後慎用劑量150 mg每天1次或頻數更低[見藥代動力學(12.3)]。
腎受損未曾在輕度,中度,或嚴重腎受損或末期腎病患者中研究KALYDECO。對輕至中度腎受損患者無需調整劑量;然而,建議嚴重腎受損患者(肌酐清除率小於或等於30 mL/min)或腎病末期患者中慎用KALYDECO。
對在CFTR基因中F508del突變純合子CF患者來自CFTR基因中F508del突變純合子CF患者中一項雙盲,安慰劑-對照試驗的療效結果顯示歷時16周KALYDECO治療與安慰劑比較,一秒鐘用力呼氣量(FEV1)無統計上顯著差別[見臨床研究(14.2)]。所以,對CFTR基因中F508del突變純合子患者中不應使用KALYDECO。
藥物過量
沒有用KALYDECO過量的報告。
在一項臨床研究使用最高單次劑量是800 mg在一種溶液劑無任何治療-相關不良事件。
最高重複劑量是450 mg(片劑)每12小時1次共4.5天(9劑)在一項試驗在健康受試者中評價KALYDECO對ECGs影響。與安慰劑比較報導的不良事件包括頭暈和腹瀉。
對KALYDECO過量無可供利用特異性抗毒藥。用KALYDECO過量的治療由一般支持措施組成包括監視生命體徵和患者臨床狀態的觀察。
一般描述
KALYDECO 片中活性成分是ivacaftor有下面化學名:N-(2,4-di-tert-butyl-5-hydroxyphenyl)-1,4-dihydro-4oxoquinoline-3-carboxamide. 其分子式是C24H28N2O3和分子量392.49。結構式如下:
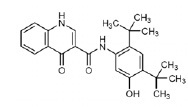 Kalydeco結構式
Kalydeco結構式臨床藥理學
作用機制Ivacaftor是CFTR蛋白的一種增效劑。CFTR蛋白是在許多器官內上皮細胞表面存在的一種氯離子通道。Ivacaftor有利於增加氯離子運輸通過增強G551D-CFTR蛋白的通道開放機率(或門控選通[gating])。
在體外,ivacaftor增加CFTR-介導的穿越上皮電流[transepithelial current, IT)在表達G551D-CFTR蛋白嚙齒類細胞中加入一種環腺苷酸(cAMP)激動劑EC50為100 ± 47 nM後;然而,在缺乏cAMP激動劑時ivacaftor不增加IT。在表達G551D-CFTR蛋白的人支氣管上皮細胞中加入一種有EC50為236 nM的cAMP激動劑後Ivacaftor也增加IT。在單通道膜片鉗實驗中用來自齧齒動物表達G551D-CFTR蛋白膜片鉗Ivacaftor增加G551D-CFTR蛋白開放機率與加入PKA和ATP相比為10-倍。
汗氯化物評價
在CFTR基因中有G551D突變患者臨床試驗中,KALYDECO導致汗中氯化物濃度統計上顯著減低。在兩項隨機化,雙盲,安慰劑-對照臨床試驗中(一項在12歲和以上患者和另一項患者6-11歲),汗中氯化物從基線至24周中位變化分別是-48 mmol/L(95% CI -51,-45)和-54 mmol/L(95% CI -62,-47)。這些變化持續至48周。汗中氯化物水平減低和肺功能(FEV1)中改善間無直接相關。
ECG評價
在72例健康受試者一項隨機化,安慰劑-和陽性-對照(莫西沙星[moxifloxacin]400 mg)四階段交叉至QT研究中評價多劑量ivacaftor 150 mg和450 mg每天2次對QTc間期的影響。在一項研究顯示檢測小效應能力,根據Fridericia的校正法(QTcF)基線-校正QTc對最大安慰劑校正的,單側95%可信區間的上限是低於監管關注閾值10 ms。
健康成年志願者和CF患者間 ivacaftor的藥代動力學相似。
健康志願者在飽腹狀態口服給予單次150 mg劑量後,峰血漿濃度時間(Tmax)發生在約4小時,和均數(±SD) AUC和Cmax分別為10600(5260) ng*hr/mL和768(233) ng/mL。
每2小時給藥,在第3至5天達到ivacaftor的穩態血漿濃度,與積蓄比值範圍2.2至2.9。
吸收
當與含脂肪食物給予ivacaftor暴露增加約2-至4-倍。所以, KALYDECO應與含脂肪食物給藥。含脂肪食物實例包括蛋,黃油,花生黃油,和乳酪比薩。在飽腹狀態tmax中位數(範圍)是約4.0(3.0; 6.0)小時。
分布
約99%的Ivacaftor結合至血漿蛋白,主要至α1-酸性糖蛋白和白蛋白。Ivacaftor不結合至人紅細胞。
健康受試者和CF患者在飽腹狀態單劑量275 mg KALYDECO後ivacaftor的平均表觀分布容積(Vz/F)相似。健康志願者在飽腹狀態口服給予150 mg每12小時共7天后,平均(±SD)表觀分布容積為353(122) L。
代謝
Ivacaftor在人中被廣泛地代謝。在體外和臨床研究表明ivacaftor主要是被CYP3A代謝。M1和M6是ivacaftor在人中的兩個主要代謝物。M1的效力約ivacaftor的1/6和被認為有藥理學活性。M6低於ivacaftor效力的1/50而不認為有藥理學活性。
消除
口服給藥後,大部分ivacaftor(87.8%)在糞中代謝轉化後被消除。主要代謝物M1和M6約占總劑量的65%有22%以M1被消除和43%為M6。以未變化母藥ivacaftor在尿中排泄量可忽略不計。單劑量後表觀末端半衰期是約12小時。健康受試者和CF患者中ivacaftor的平均表觀清除率(CL/F)相似。健康受試者150 mg劑量CL/F(SD)為17.3(8.4)L/hr。
特殊人群
肝受損
中度受損肝功能(Child-Pugh類型B,評分7至9)患者與人口統計指標匹配的健康受試者比較有相似的ivacaftor Cmax,但ivacaftor AUC0-∞增加約2-倍。所以,建議對有中度肝受損患者減低KALYDECO劑量150 mg每天1次。未曾研究輕度肝受損(Child-Pugh類別A)對ivacaftor的藥代動力學的影響,但ivacaftor的AUC0-∞增加預計小於2-倍。所以,對輕度肝受損患者無需調整劑量。未曾研究嚴重肝受損(Child-Pugh類別C,評分10-15)對ivacaftor藥代動力學的影響。不知道在這些患者中暴露增加的大小但預計大大高於中度肝受損患者觀察值。當獲益預計勝過風險,嚴重肝受損患者中KALYDECO應謹慎每天1次或更不頻繁使用劑量150 mg給藥。
腎受損
尚未在輕度、中度或嚴重腎受損患者(肌酐清除率小於或等於30 mL/min)或腎病末期患者中研究KALYDECO。對輕度和中度腎受損患者無需調整劑量因為在尿中ivacaftor及其代謝物消除可忽略不計(在一項人PK研究尿中僅回收6.6%總放射性);然而,當嚴重腎受損或腎病終末期患者給予KALYDECO建議謹慎。
性別
用來自KALYDECO臨床研究數據群體藥代動力學評價性別對KALYDECO藥代動力學的影響。無需根據性別調整劑量。
藥物相互作用
用KALYDECO和很可能共同給藥或藥代動力學相互作用研究中常被用作探針的藥物的其它藥物進行藥物相互作用研究 [見藥物相互作用(7)].
下面展示根據臨床研究或潛在藥物相互作用用KALYDECO的給藥建議:
Ivacaftor影響其它藥物的潛能
在體外研究顯示ivacaftor是一種CYP3A的弱抑制劑和抑制P-gp的潛能。在治療濃度時,和也可能抑制CYP2C8和cyp2c9同工酶。代謝物M1,但不是M6,也有抑制抑制CYP3A和P-gp潛能。Ivacaftor,M1,和M6不是CYP同工酶的誘導劑。在圖1顯示給予KALYDECO後對共同給藥藥物的給藥建議:
 圖1
圖1其它藥物影響Ivacaftor的潛能
在體外研究顯示ivacaftor和代謝物M1是CYP3A酶的底物(即,CYP3A4和CYP3A5)。在圖2中顯示KALYDECO與CYP3A抑制劑或誘導劑共同給藥的給藥建議:
 圖2
圖2注釋:對KALYDECO無誘導劑或抑制劑用作為參比品共同給藥得到數據。垂直線分別在0.8,1.0和1.25。
非臨床毒理學
癌發生,突變發生,和生育能力受損
在小鼠和大鼠中進行3年研究評估KALYDECO的致癌性潛能。在ivacaftor口服劑量至200 mg/kg/day和50 mg/kg/day,分別(根據ivacaftor及其代謝物AUC之和約分別等於MRHD的3至5倍時),小鼠和大鼠中未觀察到致瘤性證據。
Ivacaftor對以下分析中的遺傳毒性是陰性:為細菌基因突變的Ames試驗, 在體外在中國倉鼠卵巢細胞染色體畸變分析,和體內小鼠微核試驗。
Ivacaftor損傷生育能力和生殖性能指標,在雄性和雌性大鼠中在200 mg/kg/day時(根據ivacaftor及其代謝物AUC之和分別約為MRHD的5和6倍)。觀察到在雌性中在200 mg/kg/day增加長期動情周期。在大鼠中當母獸給藥前和早期妊娠期間200 mg/kg/day(根據ivacaftor及其代謝物AUC之和的MRHD約6倍)Ivacaftor還增加有全部非生存胚胎雌性數和減少黃體數,植入數,和活存胚胎數。在雄性和雌性大鼠中在200 mg/kg/day時,這些生育能力和生殖行為受損是歸因於嚴重毒性。在≤100 mg/kg/day(根據ivacaftor及其代謝物AUC之和MRHD的約3倍)未觀察到對雄性或雌性生育能力和生殖性能指標的影響。
臨床研究
在CFTR基因有一個G551D突變的患者中試驗劑量範圍:
對劑量範圍臨床方案主要包括一項雙盲,安慰劑-對照,交叉試驗在39例成年(平均年齡31歲)高加索人有CF患者有預測的FEV1 ≥ 40%。20例患者在基線時有中位預測的FEV1 56%(範圍:42%至109%)接受KALYDECO 25,75,150 mg或安慰劑每12小時共14天和19例患者在基線時有中位預測的FEV1 69%(範圍:40%至122%)接受KALYDECO 150,250 mg或安慰劑每12小時共28天。150 mg每12小時劑量的選擇主要根據肺功能輕微的[nominal]改善(給藥前FEV1)和藥效動力學參數的變化(汗氯化物和鼻潛力差別)。每天2次給藥方案主要是根據表觀末端血漿半衰期約12小時。對6至11歲兒童是根據觀察到達到與成年患者觀察到可比的藥代動力學。
療效:
在CFTR基因有一個G551D突變的CF患者中在兩項隨機化,雙盲,安慰劑-對照臨床試驗在213例臨床上穩定有CF患者(109例接受KALYDECO 150 mg每天2次)中評價KALYDECO的療效。來自這些試驗所有合格患者被滾動進入一項開放延伸研究。
試驗1評價161例有CF患者年齡12歲或以上(平均年齡26歲)有基線預測的FEV1 40-90%間[平均預測的FEV1 64%(範圍:32%至98%)]。試驗2評價52例患者為6至11歲(平均年齡9歲)有基線預測的FEV1 40-105%間[平均預測的FEV1 84%(範圍:44%至134%)]。在篩選時排除從痰中分離出有持久洋蔥伯克霍爾德菌([Burkholderia cenocepacia], dolosa,或分支桿菌屬[Mycobacterium] abcessus患者和那些有異常肝功能被定義為3或以上肝功能檢驗 (ALT,AST,AP,GGT,總膽紅素) ≥正常上限3倍患者。
在兩項試驗中患者被1:1隨機化至接受或150 mg KALYDECO或安慰劑每12小時與含脂肪食物共48周除了被處方CF治療(如,妥布黴素[tobramycin],阿法鏈道酶[dornase alfa])。不允許使用吸入高滲鹽水。
在兩項研究中主要療效終點是肺功能改善當用給藥前預測的FEV1直至治療第24周從基線平均絕對變化百分率。
在兩項研究中,用KALYDECO治療導致FEV1顯著改善。在試驗1中對從基線至24周預測的FEV1平均絕對變化百分率KALYDECO和安慰劑間治療差別是10.6百分點(P < 0.0001)和在試驗2中12.5百分點(P < 0.0001)(圖3)。這些變化持續至48周。觀察到預測的FEV1百分率改善不管年齡,疾病嚴重程度,性別,和地理區域。
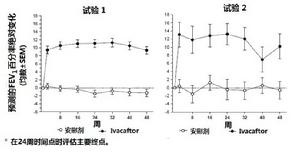 圖3
圖3其它療效變數包括汗中氯化物從基線至第24周絕對變化[在臨床藥理學討論(12.2)],直至第48周首次肺加重的時間(僅試驗1),從基線至第48周體重絕對變化,和囊性纖維化症狀改善包括相關呼吸症狀例如咳嗽,痰產生,和呼吸困難。對本研究的目的,肺加重被定義為抗生素治療中變化(IV,吸入,或口服)當12項預先指定sino-肺體徵/症狀有4或更多的結果。用KALYDECO治療患者顯示肺加重的風險,CF症狀(僅在試驗1),和體重增重統計上顯著改善(表2)。在患者<20歲中體重數據,當對年齡和性別用體重指數歸一化表示時,與重量從基線絕對變化一致。
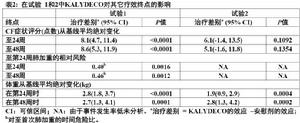 表2
表2試驗3是在140例年齡12歲和以上是在CFTR基因中對F508del突變純合子和有預測的FEV1 ≥40%有CF患者中一項16-周隨機化,雙盲,安慰劑-對照,平行-組試驗。患者被4:1隨機化接受KALYDECO 150 mg (n=112) 每12小時或安慰劑(n=28)除了他們處方的CF治療。被納入患者平均年齡為23歲和平均基線預測的FEV1是79%(範圍40%至129%)。因為在試驗1和2中,排除在篩選時從痰分離持久洋蔥伯克霍爾德菌([Burkholderia cenocepacia],dolosa,或分支桿菌屬[Mycobacterium] abcessus和那些有異常肝功能被定義為3或更多肝功能檢驗(ALT,AST,AP,GGT,總膽紅素) ≥正常上限3倍的患者。不允許使用吸入高滲鹽水。
當用從基線至16周預測的FEV1百分率平均絕對變化測定主要終點肺功能改善。在CFTR基因中對F508del突變純合子CF患者中用KALYDECO治療相對於安慰劑導致FEV1無改善[從基線至16周預測的FEV1百分率平均絕對變化對患者KALYDECO和安慰劑-治療組是分別1.5%和-0.2%(p = 0.15)]。用KALYDECO治療患者與安慰劑比較對第二位終點間差別無意義(CF症狀變化,體重變化,或汗中氯化物濃度變化)。
如何供應/貯存和處置
KALYDECOTM (ivacaftor)是以淡綠色,膜包衣,膠囊形含150 mg ivacaftor片供應。每片一側印有字元“V 150”和另一側平坦,和被包裝如下:
56-計數盒(含4個獨立泡卡每卡14片) NDC 51167-200-01和60-計數瓶NDC 51167-200-02
貯存在20-25?C (68-77?F);外出時允許15-30?C (59-86?F) [見美國藥典控制室溫]。
購買須知
美國是醫藥分開的國家,藥房全部實行嚴格的處方藥與非處方藥分類管理。對處方藥的銷售,必須憑美國醫生(電子/紙質)處方。如今國內患者可以依託科技,通過好醫友國際醫療平台實現遠程的病歷互動,由美國醫生根據患者病情開具電子處方,以正規渠道在好醫友美國藥房購買到處方藥。
患者諮詢資料
轉氨酶(ALT或AST)升高和監視告知患者用KALYDECO治療患者中曾發生肝檢驗升高。開始用KALYDECO前和治療頭一年時每3個月和其後每年進行肝功能檢驗[見警告和注意事項(5.1)]。
與CYP3A誘導劑和抑制劑藥物相互作用要求患者告訴你他們所用全部藥物包括任何草藥補品或維生素。建議KALYDECO不要與強CYP3A誘導劑(如,利福平, 聖約翰草)共同給藥,因為它們減低KALYDECO的治療有效性。當與強CYP3A抑制劑,例如酮康唑共同給藥時建議減低KALYDECO劑量至150 mg一周2次。當與中度CYP3A抑制劑,例如氟康唑共同給藥時建議減低劑量至150 mg 每天1次。應避免含柚子汁或Seville橘子食物[見藥物相互作用(7.1, 7.2)和臨床藥理學(12.3)]。
有肝受損患者中使用詢問和/或評估患者是否有肝受損。中度受損肝功能患者中減低KALYDECO劑量(Child-Pugh類別B,評分7 至9)至每天1次150 mg。未曾在嚴重肝受損患者中研究KALYDECO (Child-Pugh類別C,評分10-15);然而,預計暴露大大高於中度肝受損患者觀察值。當預計獲益大於風險,嚴重肝受損患者應慎用KALYDECO劑量每天1次150 mg或頻數更低。建議輕度肝受損患者無需調整劑量(Child-Pugh類別A,評分5-6)[見臨床藥理學(12.3)].
與含脂肪食物服用告知患者當與脂肪食物服用KALYDECO機體吸收最佳。典型CF膳食將滿足此要求。實例包括蛋、黃油、花生黃油、乳酪比薩等。