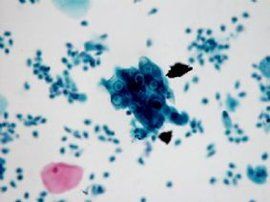
生物學特性
形態培養
 C型肝炎病毒
C型肝炎病毒HCV病毒體呈球形,直徑小於80nm(在肝細胞中為36~40nm,在血液中為36-62nm ),為單股正鏈RNA病毒,在核衣殼外包繞含脂質的囊膜,囊膜上有刺突。HCV僅有Huh7, Huh7.5, Huh7.5.1三種體外細胞培養系統,黑猩猩可感染HCV,但症狀較輕。
基因結構
HCV-RNA大約有9500-10000bp組成,5′和3′非編碼區(NCR)分別有319-341bp,和27-55bp,含有幾個順向和反向重複序列,可能與基因複製有關。在5′非編碼區下游緊接一開放的閱讀框(ORF),其中基因組排列順序為5'-C-E1-E2-p7-NS2-NS3-NS4-NS5-3',能編碼一長度大約為3014個胺基酸的多聚蛋白前體,後者可經宿主細胞和病毒自身蛋白酶作用後,裂解成10種病毒蛋白,包括三種結構蛋白,即分子量19KD的核衣殼蛋白(或稱核心蛋白,Core)和兩種糖蛋白(分子量為33KD的E1蛋白,分子量72Kd的E2蛋白),p7編碼一種膜內在蛋白,其功能可能是一種離子通道。非結構蛋白部分則包括NS2,NS3, NS4A,NS5A和NS5B,非結構蛋白對比病毒的生活周期非常重要。NS2和NS3具有蛋白酶活性,參與病毒多聚蛋白前體的切割。此外,NS3蛋白還具有螺鏇酶活性,參與解鏇HCV-RNA分子,以協助RNA複製,NS4的功能尚不清楚。NS5A是一種磷酸蛋白,可以與多種宿主細胞蛋白相互作用,對於病毒的複製起重要作用。而NS5B則具有RNA依賴的RNA聚合酶活性,參與HCV基因組複製。
變異性
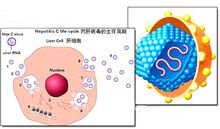 C型肝炎病毒
C型肝炎病毒HCV具有顯著異源性和高度可變性,對已知全部基因組序列的HCV株進行分析比較其核苷酸和胺基酸序列存在較大差異。並表現HCV基因組各部位的變異程度不相一致,如5′-CR最保守,同源性在92-100%,而3′NCR區變異程度較高,在HCV的編碼基因中,C區最保守、非結構(NS)區次之,編碼囊膜蛋白E2/NS1可變性最高稱為高可變區。
基因分型
HCV基因分型還無統一標準,因用於基因分型的部位和採用的技術方法不同,出現了各種基因分型結果,但各種基因型分類方法之間有一定的對應關係。
表26-2 HCV基因型各種分型之間的對應關係現知歐美國家多數HCV-Ⅰ型感染,而亞洲國家以Ⅱ型為主,Ⅲ型次之。Okomoto報告日本慢性C型肝炎患者和健康獻血員主要為Ⅱ型感染,分別占59.3%和82.4%,而血友病人約50%為Ⅰ型感染,原因是套用輸入美國進口凝因子Ⅷ。Wang氏報告我國北京慢性C型肝炎患者86.2%為Ⅱ型感染,Ⅲ型感染為13.8%。而新疆病人Ⅲ型感染卻占50%,說明不同型HCV具有一定的地區和人群分布特徵。此外不同基因型感染引起臨床過程和干擾素治療反應亦表現不同,如Ⅲ型感染臨床症狀較重,有引起嚴懲肝病傾向:Ⅱ型(Simmonds 1b)感染對干擾素治療不敏感效果差,Ⅲ型感染(Simononds 2a)用干擾素治療效果好。
感染的自然史
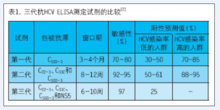 C型肝炎病毒
C型肝炎病毒大部分患者在感染的急性期無明顯症狀,伴有高水平的病毒血症和ALT升高。HCV急性感染後HCV RNA早於抗-HCV出現於血液中。HCV RNA最早可於暴露後2周檢出,HCV 核心抗原可在HCV RNA出現後1~2d檢出,而抗-HCV直到8~12周才能檢出,也就是說,在HCV感染髮生後,有約8-12周的時間,僅能檢出HCV RNA,而抗-HCV為陰性,即抗-HCV檢測的“視窗期”,“視窗期”的長短與檢測試劑有關。抗-HCV不是保護性抗體,是HCV感染的標誌。15%~40%的HCV急性感染者可在6個月內清除感染,在感染清除的過程中,有可能HCV RNA水平很低不能檢出,僅抗-HCV陽性;而65%~80%的患者病毒持續6個月仍未被清除,稱為慢性HCV感染。一旦慢性C型肝炎發生,HCV RNA滴度開始穩定,自發痊癒的病例很少見。除非進行有效的抗病毒治療,否則HCVRNA很少發生自發清除。在臨床上,慢性C型肝炎的患者抗-HCV多為陽性(免疫抑制的患者,如HIV感染者、實體器官移植受者、低丙種球蛋白血症或者血液透析患者可出現抗-HCV陰性),HCV RNA可為陽性也可為陰性(經抗病毒治療,HCV RNA水平低)。
實驗室診斷
RIA或者ELISA
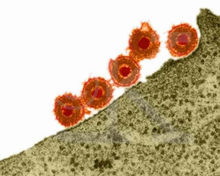 C肝病毒模式圖
C肝病毒模式圖即:放射免疫診斷(RIA)或酶聯免疫試驗(ELISA)檢測血清中抗HCV。
1989年,Kuo等建立了抗-C-100放射免疫試驗方法(RIA),隨後 Ortho公司又研製成功酶聯免疫試驗方法(ELISA)檢測抗-C-100。這兩種方法均用重組酵母表達的病毒抗原(C-100-3,為NS4編碼的蛋白,含363個胺基酸),經純化後包被微量塑膠板孔,然後加被檢血清,該病毒抗原即與被檢血清中抗-C-100結合,最後加同位素或酶標記的鼠抗人lgG單克隆抗體,加底物顯色判斷結果。
用上述酶聯免疫試驗法(ELISA)檢測抗-C-100有如下缺點:
1. 抗-C-100齣現較晚,約半數輸血後C型肝炎病人於輸血後4~6個月抗-C-100首次陽轉,因此,不宜作為急性C型肝炎的常規實驗室診斷;
2.抗-C-100不是中和抗體,也不是lgM抗體,而是lgG 抗體;
3.本法不夠靈敏,少數C型肝炎病人檢測不到抗-C-100;
4.有非特異性,一些自家免疫性慢性肝病患者可出現假陽性,因此,抗HCV陽性需作重組免疫印跡試驗(Recombinant Immune Blot Assay,RIBA,或稱 Western Blot)證實。
由於HCV核心抗體出現較早,因此,最近美國第二代酶聯免疫試驗法(ELISA)檢測抗HCV。該試劑盒採用HCVC區編碼蛋白C-22-3和非結構區NS3編碼蛋白C-33-3和C-100-3包被載體。用本法檢測抗HCV,其檢出率可提高25~30%,且檢出抗HDV的時間也可提早16~42天。
聚合酶鏈反應
(HCV cDNA/Polymerase Chain Reaction,RTPCR)測定肝和血清中HCV RNA。
本法是將HDV RNA逆轉錄為HCV DNA,選用高度保守的5′非編碼區引物擴增放大後作電泳觀察結果。本法較靈敏。由於肝和血清中HCV RNA出現較抗-HCV為早,一些HCV感染者抗HCV尚未陽轉時,其肝和血清中已可測到HDV RNA。HCV RNA陽性,說明病毒在體內複製;HCV RNA陰轉,說明病毒被清除。因此,RT-PCR可作為C型肝炎的早期診斷和獻血員篩查的出現指標,也可作為C型肝炎預後的一個指標。
檢測的意義
 C型肝炎病毒
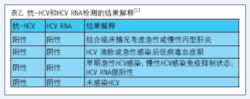
C型肝炎病毒抗-HCV和HCV RNA檢測結果可出現以下四種模式,需要進行認真分析以明確其診斷意義(見表2)。AASLD(the American Association for the Study of Liver Diseases)指南指出:
1、HCV RNA及抗-HCV均為陽性並伴近期ALT升高存在以下三種可能:①結合近期高危暴露史,考慮是否為急性HCV感染;②慢性HCV感染急性加重;③合併其他病原體導致急性肝炎的慢性HCV感染。
2、抗-HCV陽性而HCV RNA陰性提示:①HCV感染痊癒;②急性HCV感染後HCV RNA的清除期;③假陽性或假陰性結果;此時,建議4~6個月後再行HCV RNA檢測以明確診斷。
3、抗HCV陰性而HCV RNA陽性,提示為抗體產生之前的急性感染早期或免疫抑制患者慢性HCV感染,也有可能為HCV RNA假陽性結果,建議4~6個月後複查抗HCV和HCV RNA。
4、患者ALT升高而抗HCV及HCV RNA均為陰性,考慮可除外急性或慢性C型肝炎診斷。推薦4~6個月後複查抗-HCV。
需要說明是,抗-HCV和HCV RNA不能用於確定疾病的嚴重性,也不能用於預測疾病的預後和進展。
防治原則
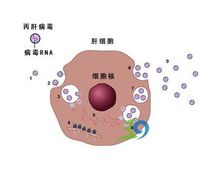 C型肝炎病毒入侵
C型肝炎病毒入侵C型肝炎的預防方法基本與B型肝炎的相同。目前,我國預防C型肝炎的重點應放在對獻血員的管理,加強消毒隔離制度,防止醫源性傳播。
國外報告,對獻血員進行抗HCV篩查,可排除85%具有HCV傳染性的獻血員,從而明顯降低輸血後C型肝炎的發病率。由於獻血員抗HCV陽性率與ALT水平和抗-HBc是否陽性有關,ALT(丙氨酸轉移酶)異常和抗HBc陽性者抗HCV陽性率明顯高於ALT正常和抗HBc陰性者(44%:0.5% ),因此,在目前尚無條件進行抗HCV篩查的地區,可對獻血員作ALT和抗HBc篩查。據報導,排除ALT異常的獻血員後,輸血後C型肝炎發病率可下降 47.4%;排除抗HBc陽性的獻血員後,輸血後C型肝炎發病率下降33%;如上述兩項指標異常的獻血員均被排除,則輸血後C型肝炎發病率可下降 61.2%。
最近,美國疾病控制中心報告,經皮膚感染C型肝炎病人血液者,於暴露後立即注射免疫蛋白(0.06ml/kg)可能有預防作用。
本病的最終控制將取決於疫苗預防。HCV分子克隆的成功,為本病的疫苗預防提供了可能性,未來的C型肝炎疫苗應包括各種不同重組的HCV毒株,或根據各地流行的HCV毒株來構建C型肝炎疫苗。
無論是急性C型肝炎,還是慢性C型肝炎,標準治療方案都是聚乙二醇干擾素(alfa-2a 或alfa-2b)聯合利巴韋林。這也是唯一有效治療C型肝炎的方案。聚乙二醇干擾素alfa由於一周一次給藥,給藥次數大大減少,方便了病人用藥,相對於普通干擾素的一周三次或隔日一次,聚乙二醇干擾素又稱為長效干擾素。兩種長效干擾素聯合利巴韋林的直接比較臨床試驗表明:12KD的聚乙二醇干擾素alfa-2b的復發率明顯低於40KD聚乙二醇干擾素alfa-2a,原因可能與抗病毒活性及分子大小引起的藥物分布有關。一般認為,聚乙二醇的分子量越大,抗病毒活性越低,12KD的聚乙二醇干擾素alfa-2b的活性明顯高於40KD的長效干擾素;而且,12KD的長效干擾素可以全身分布,不僅清除肝內的主要病毒,更可以清除淋巴結、腎臟、脾臟、腎上腺、唾液腺等肝外病毒,故停藥後的復發率較低。40KD大分子聚乙二醇干擾素由於分子過大,限於血管和肝內分布,對肝外的病毒清除不利。不僅加重肝臟負擔,排泄慢,而且由於不經過腎臟排泄,當發生不良反應時撤藥困難。一般認為,由於頭對頭比較的IDEAL試驗結果的公布,12KD聚乙二醇干擾素alfa-2b應做為治療C型肝炎的優先用藥。
感染的症狀
 C型肝炎病毒
C型肝炎病毒其一、C肝患者很大一部分沒有任何症狀,慢性C肝患者甚至可以在20年間沒有任何明顯症狀。
其二、C肝潛伏期一般為1.5-2個月,經過一段時間的潛伏期後,便出現肝炎的常見症狀,有疲乏、身體無力、食慾減退、部分可出現黃疸等症狀。
其三、C肝患者右上腹部感覺不舒服、噁心、嘔吐、食慾減退。
其四、少數C肝患者伴低熱,輕度肝腫大,有些患者可出現黃疸。
其五、少數C肝患者體重減輕、肌肉關節疼痛,睡眠不好。
其六、患者肝功能指標多為正常或輕度異常。
哪些因素容易引起C肝的傳播呢?
1、濫用藥物和注射毒品是目前引起C肝傳播的最主要的因素,主要是好多人共用一個注射器,被C肝病毒感染的機會就會大大增加,這類人要想徹底預防C肝傳染就必須戒毒或者使用個人的注射器或針頭。
2、輸血也是引起C肝傳播的重大因素之一,如果被輸入的血液沒有經過嚴格的篩查,輸血者感染C肝的就會就會大大增加,容易引起C肝傳染。
3、長期做透析的人也容易感染C肝病毒,主要是使用了沒有經過嚴格消毒的腎透析機而感染C肝病毒,屬於醫源性傳播的一種。
4、母嬰傳播是引起C肝傳播的重要因素之一,主要是感染了C肝病毒的母親在分娩過程中將C肝病毒傳染給孩子,這就需要母親在分娩前後採取有效的母嬰阻斷措施降低孩子感染病毒的機會。
5、不潔性交、公用某些私人物品(如牙刷或剃鬚刀等)也會造成C肝的傳播。
治癒
C型肝炎患者如果病毒核酸(HCV - RNA)陽性,說明病毒在持續複製,其肝功能難以穩定,患者多數情況下,血清轉氨酶(ALT)呈輕度或中度升高。這些患者應該進行抗病毒治療及保肝治療。經多年的臨床驗證,使用普通干擾素後,可有50%的患者獲得較好療效,即血清HCV - RNA陰轉,肝功能恢復正常。但停用干擾素後,10%~15%的患者出現病毒複製反彈,即HCV - RNA陽轉,肝功能再次異常。近幾年來,隨著長效干擾素聯合病毒唑的臨床套用,C肝患者的療效較以前提高了20%~30%,目前可達80%~90%。尤為可喜的是其反彈率明顯減少。長效干擾素套用劑量如前所述;病毒唑800~1200毫克/天,分3次口服。療程應在6~12個月。如能堅持12個月的療程,C肝病毒及肝功能出現反彈的幾率一般在5%以下。因此,有學者認為,長效干擾素聯合病毒唑的治療為徹底治癒C型肝炎帶來了光明的前景。
主要檢查項目
 C型肝炎病毒
C型肝炎病毒C型肝炎患者主要的檢查項目有以下方面:
1、肝功能檢查:直接判斷肝臟受損傷的情況,肝臟的受損、合成能力、代謝能力、儲備能力的了解等。
2、C肝病毒RNA檢測:C肝病毒RNA檢測是檢測血液中C肝病毒的實際存在情況,可在感染兩周內檢測到病毒。
3、C肝抗體檢測:C肝抗體檢測是用於診斷C肝的最重要手段,適用於高危人群的篩查,也可以用於C肝感染者的初次篩查。該項檢查是初步檢查C肝時,患者必須要做的基本檢查。C肝抗體是是否感染C肝病毒的指標,如果C肝抗體呈陽性,則說明患者很有可能感染了丙型病毒。
4、B超或肝穿刺檢查:這也是常見的C肝檢查項目,通過這兩項檢查可以判斷是否展為肝硬化,因為C肝發展為肝硬化幾率較高,所以需需要重視。其影像學檢查主要是進行B超檢查,通過B超檢測可以初步了解患者感染C肝病毒後,肝臟的實體形態,包括的肝臟的形態、回聲、大小等,經過該項檢查可以準確的診斷肝臟是否存在問題。
生活的注意
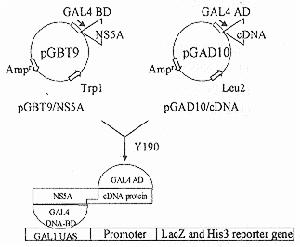 C型肝炎病毒
C型肝炎病毒C肝患者日常生活要注意以下幾個方面的問題:
1、預防傳染:家庭成員間不要共用衛生用具,女性C肝患者經期衛生棉應該處理後再扔掉,夫妻間性生活應採取防護措施,性生活儘量使用安全套。
2、避免有毒的化學物質:如少吃含色素和防腐劑過多的食品,不吃霉變的食物和已爛的姜。
3、注意合理的飲食:飲食要少食含脂肪、糖、色素、防腐劑過多的食品,以有效減輕肝臟負擔外,此外還應適當增加蛋白質和維生素的攝入量等。
4、合理作息:C肝患者要注意休息,補充睡眠,這樣會減少對自身肝臟的損害程度,有利於肝細胞的修復和再生,同時對患者病情的好轉也是很有用的。
5、保持良好的心情:C肝患者應該保持良好的心情,積極的面對疾病,樹立戰勝疾病的信心,切勿產生焦慮、煩躁的心情。