化合物簡介
基本信息
中文名稱:鹽酸帕洛諾司瓊
中文別名: 帕洛諾司瓊鹽酸鹽
英文名稱:palonosetron hydrochloride
英文別名:(3aS)-2-[(3S)-1-azabicyclo[2.2.2]octan-3-yl]-3a,4,5,6-tetrahydro-3H-benzo[de]isoquinolin-1-one,hydrochloride; Palonosetron Hydrochloride; Palonosetron hydrochloride;
CAS號:135729-62-3
分子式:CHClNO
分子量:332.86800
精確質量:332.16600
PSA:23.55000
LogP:3.33430
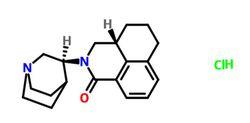 鹽酸帕洛諾司瓊
鹽酸帕洛諾司瓊結構式:
物化性質
外觀與性狀:白色固體
熔點:>290ºC
沸點:470.4ºC at 760 mmHg
閃點:209.5ºC
蒸汽壓:5.07E-09mmHg at 25°C
安全信息
信號詞:警告
危害聲明:H302
警示性聲明:P301 + P312 + P330
海關編碼:2933990090
藥理毒理
藥理作用
帕洛諾司瓊為親和力較強的5-HT3受體選擇性拮抗劑,對其它受體無親和力或親和力較低。5-HT3受體位於延髓最後區的催吐化療感受區中央和周圍的迷走神經末梢。化療藥物通過刺激小腸嗜鉻細胞釋放5-HT,5-HT再激活迷走傳入神經的5-HT3受體,產生嘔吐反射。
毒理研究
致癌性:CD-1小鼠的104周的致癌性研究中,動物經口給予10、30和60mg/kg/d的帕洛諾司瓊治療,結果顯示,帕洛諾司瓊無致癌性。最高試驗劑量產生的帕洛諾司瓊的系統暴露量(血漿AUC)為人類推薦靜脈給予0.25mg帕洛諾司瓊後暴露量(AUC=29.8ng.h/ml)的150-289倍。在SD大鼠104周的致癌性研究中,雄性大鼠和雌性大鼠分別經口給予15、30、60mg/kg/d和15、45、90mg/kg/d的帕洛諾司瓊,最高給藥劑量產生的帕洛諾司瓊系統暴露量(血漿AUC)為人類推薦給藥劑量暴露量的137-308倍。使用帕洛諾司瓊導致雄性大鼠中良性腎上腺嗜鉻細胞瘤和良惡性混合的嗜鉻細胞瘤發病率上升,胰腺胰島細胞腺瘤、混合性腺瘤和肉瘤以及垂體瘤的發病率上升,而在雌性大鼠中,則會導致肝細胞腺瘤和肉瘤的發生,甲狀腺C-細胞腺瘤、混合性腺瘤以及肉瘤的發病率上升。
致突變性:細菌Ames試驗、中國倉鼠卵巢細胞致突變試驗、體外肝細胞無序DNA合成(UDS)試驗或小鼠的微核試驗表明,帕洛諾司瓊無致突變毒性。但是,帕洛諾司瓊對中國倉鼠卵巢細胞染色體有畸變作用。
生殖毒性:大鼠口服給藥劑量為60mg/kg(根據體表面積計算,約為人推薦靜脈注射劑量的1894倍)時,對雌雄大鼠的生育力和生殖力均無影響。
藥代動力學
以下數據來自國外研究
健康志願者和癌症患者分別靜脈給予帕洛諾司瓊後,隨著藥物在體內緩慢消除,血藥濃度開始下降。無論是健康志願者還是癌症患者,平均最大血藥濃度(Cmax)和藥時曲線下面積(AUC0→∞),在0.3-90μg/kg的劑量範圍內均呈劑量相關性。六名癌症患者單劑量靜脈給予帕洛諾司瓊3μg/kg(或0.21mg/70kg),其最大血藥濃度為5.6±5.5ng/ml,平均AUC為35.8±20.9ng·hr/ml。
分布
帕洛諾司瓊的表觀分布容積為8.3±2.5L/kg,血漿蛋白結合率約為62%。
代謝
帕洛諾司瓊通過多種途徑代謝,約50%的主藥代謝為N-去氧帕洛諾司瓊和6-S-羥基帕洛諾司瓊,這兩種代謝產物各自拮抗5-HT3受體的活性不到帕洛諾司瓊的1%。體外代謝研究表明,以CYP2D6為主要代謝酶,其次CYP3A和CYP1A2也參與了帕洛諾司瓊的代謝。但是,CYP2D6的快代謝者和慢代謝者的臨床藥代動力學參數無明顯差別。
排泄
單劑量靜脈給予10μg/kg 14C標記的帕洛諾司瓊,144hr後,出現在尿液中的放射標記物約占給藥劑量的80%,其中,帕洛諾司瓊約給藥劑量的40%為。健康志願者中全身清除率為160±35ml/h/kg,腎清除率為66.5±18.2ml/h/kg,平均終末消除半衰期為40hr。
老年患者
群體藥代動力學分析及臨床安全性和有效性資料顯示,≥65歲的老年患者與年輕患者(18-64歲)之間無差異。因此,老年患者無需調整劑量。
不同種族
24名日本健康志願者進行了藥代動力學研究,靜脈給予3-90μg/kg劑量範圍的帕洛諾司瓊,其全身清除率比白種人高25%,但不需調整劑量。黑種人帕洛諾司瓊藥代動力學研究尚不充分。
腎損傷患者
輕至中度的腎損傷不會顯著影響帕洛諾司瓊的藥代動力學參數,重度腎損傷患者較健康志願者的系統暴露量增高約28%。因此,不同程度的腎損傷患者均無需調整劑量。
肝損傷患者
與健康志願者相比,肝臟損害對帕洛諾司瓊全身清除率無顯著影響,因此,不同程度的肝損傷患者均無需調整劑量。
適應症:
1、預防重度致吐化療引起的急性噁心、嘔吐;
2、預防中度致吐化療引起的噁心、嘔吐。
不良反應
據國外臨床研究報導:1374名成年患者參加了帕洛諾司瓊預防由中度或高度致吐化療引起的噁心、嘔吐的臨床研究。結果表明,帕洛諾司瓊引起不良反應的發生率及嚴重程度與昂丹司瓊或多拉司瓊相似。
禁忌症
禁用於已知對該藥物或藥物中任何組份過敏的患者。
用法用量
推薦劑量為,化療前約30分鐘,單劑量靜脈注射帕洛諾司瓊0.25mg,注射時間為30秒以上。
注意事項
過敏反應可能發生於對其它選擇性5-HT3受體拮抗劑過敏者。國外文獻報導,在192名心臟功能缺陷患者的Ⅲ期臨床研究中已證明帕洛諾司瓊是安全的,但是對於患有或可能發展為心臟傳導間期延長的病人,尤其是QTC延長的病人應謹慎使用帕洛諾司瓊。這些患者包括:低鉀血症或低鎂血症患者,服用利尿藥而導致電解質異常者,先天性QT綜合症患者,服用抗心律失常或其它藥物導致QT間期延長的患者,和給予累積高劑量蒽環類藥物治療者。在3項關鍵性研究中,獲得了患者基線和接受鹽酸帕洛諾司瓊注射液或對照藥後24小時的心電圖(ECGS),在部分患者中獲得用藥後15分鐘的心電圖。出現QT和QTC間期改變(絕對值>500msec或自基線的變化>60msec)患者的百分比(<1%)與對照藥物組(昂丹司瓊或多拉司瓊)的結果相似。
鹽酸帕洛諾司瓊注射液不能跟其他藥物混合,故使用帕洛諾司瓊注射液前、後均需套用生理鹽水沖洗輸注管路。尚未在妊娠期婦女中進行充分的隨機對照臨床試驗,也沒有妊娠期或分娩期婦女使用過帕洛諾司瓊,因此對其對母親及胎兒的影響並不清楚,故懷孕期間應慎用本品。帕洛諾司瓊是否通過乳汁分泌尚不明確。鑒於多數藥物均經人體乳汁排泄,對乳兒有潛在的嚴重不良反應,且在大鼠致癌作用研究發現有潛在致癌作用。因此,應充分考慮使用藥物的必要性之後,來決定是否停止哺乳或停止用藥。
孕婦及哺乳期婦女用藥:
尚未在妊娠婦女中進行充分的隨機對照臨床試驗,也沒有妊娠期或分娩期婦女使用過帕洛諾司瓊,因此對其對母親及胎兒的影響並不清楚,故懷孕期間應慎用本品。
帕洛諾司瓊是否通過乳汁分泌尚不明確。鑒於多數藥物均經人體乳汁排泄,對乳兒有潛在的嚴重不良反應,且在大鼠致癌作用研究發現有潛在致癌作用。因此,應充分考慮使用藥物的必要性之後,來決定是否停止哺乳或停止用藥。
兒童用藥
18歲以下的患者使用本品的安全性和有效性尚未經研究確定。
老年用藥
據文獻報導:帕洛諾司瓊在1374名成年腫瘤患者的臨床研究中,其中,316(23%)例≥65歲,71例(5%)≥75歲。除某些老年個體較為敏感外,帕洛諾司瓊用於老年患者與年輕患者在安全性和有效性方面無差別。因此,老年患者用帕洛諾司瓊無需調整劑量和特殊監護。
藥物相互作用
體內帕洛諾司瓊通過腎排泄和多種CYP酶參與的代謝兩種途徑進行消除。體外進一步研究表明,帕洛諾司瓊既不是CYP1A2、CYP2A6、CYP2B6、CYP2C9、CYP2D6、CYP2E1和CYP3A4/5(CYP2C19未研究)的抑制劑,也不誘導CYP1A2、CYP2D6或CYP3A4/5的活性。
因此,與帕洛諾司瓊產生明顯的臨床藥物相互作用的可能性很低。健康志願者單劑量靜脈給予0.75mg帕洛諾司瓊,穩定期口服滅吐靈(每天四次,每次10mg)的研究中未發現明顯的藥代動力學影響。臨床研究表明,帕洛諾司瓊能安全地與皮質類固醇類、鎮痛藥、止吐藥、解痙藥和抗膽鹼能藥物一起使用。鼠腫瘤模型研究表明,帕洛諾司瓊不會抑制所研究的五種化療藥物(順鉑、環磷醯胺、阿糖胞苷、阿黴素和絲裂黴素C)的抗腫瘤活性。
藥物過量
尚無已知的帕洛諾司瓊的解毒劑,因此藥物過量時應該用支持療法。在帕洛諾司瓊劑量探索研究中,50名成人癌症患者給予90μg/kg的劑量(相當於6mg的固定劑量),接近推薦劑量0.25mg的25倍。該劑量組產生的不良反應事件與其它劑量組相似,未見劑量依賴性。儘管未進行過透析治療的研究,但是由於帕洛諾司瓊具有較大的分布容積,故透析不可能作為有效的治療藥物過量手段。大鼠和小鼠單劑量靜脈給予帕洛諾司瓊的致死量為30mg/kg(按體表面積換算,大鼠和小鼠的劑量分別相當於人體推薦劑量的947和474倍),主要中毒症狀為驚厥、喘息、膚色蒼白、發紺、虛脫。
貯藏方法
室溫(10~30℃) 密閉保存,避光、防凍。

