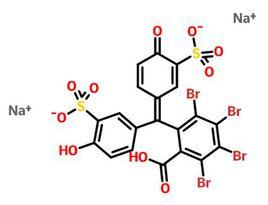
化合物簡介
中文別名:3,3'-(3-氧代-4,5,6,7-四溴-1(3H)-異苯並呋喃亞基)雙(6-羥基苯磺酸)二鈉鹽; 酚四溴酞磺酸鈉;
英文名稱:Sulfobromophthalein sodium hydrate
英文別名:disodium,2-hydroxy-5-[4,5,6,7-tetrabromo-1-(4-hydroxy-3-sulfonatophenyl)-3-oxo-2-benzofuran-1-yl]benzenesulfonate,hydrate;Sulfobromophthalein sodium;BSP,Bromsulfalein sodium disodium salt hydrate;Sulfobromophthalein disodium salt hydrate;
CAS號:123359-42-2
分子式:CHBrNaOS
結構式:
分子量:837.99700
精確質量:833.60900
PSA:205.76000
LogP:6.57600
物化性質
外觀與性狀:白色結晶粉末
密度:0.866g/mLat 25°C(lit.)
熔點:-44°C
沸點:227 °C
閃點:202°F
折射率:n20/D 1.422(lit.)
安全信息
WGK Germany:3
危險類別碼:R42/43
安全說明:S22; S36/37; S45
RTECS號:SM8395000
危險品標誌:Xn
藥典標準
含量限度
本品為3, 3’-(3-氧代-4,5,6,7- 四溴-1(3H)- 異苯並呋喃亞基) 雙[6-羥基苯磺 酸] 二鈉鹽。按乾燥品計算,含硫(S) 應為7.4 ~8.2%;含溴(Br)應為36.0~39.0%。
檢查
1.溶液的澄清度與顏色
取本品0.20g ,加水10ml溶解後,溶液應澄清無色。
2.無機鹵化物
取本品50mg,加水 5ml溶解後,加稀硝酸1ml與硝酸銀試液5ml,只許發生極微的渾濁。
3.硫酸鹽
取本品20mg,加水10ml溶解後,加稀鹽酸5 滴,煮沸後,加氯化鋇試液 1 ml,熱溶液應澄清(放冷,可有磺溴酞的鋇鹽析出)。
4.乾燥失重
取本品,在105 ℃乾燥至恆重,減失重量不得過5.0 %(附錄Ⅷ L)。
鑑別
(1) 取本品約5mg ,加新沸過的冷水使溶解成50ml,取1ml ,加0.02mo l/L氫氧化鈉溶液0.20ml,即顯深紫堇色,再加0.01mol/L 硫酸溶液0.20ml,紫堇色應 即消失。
(2) 取本品約0.1g,加碳酸鈉0.5g,混合後,熾灼至完全炭化,放冷,加熱水5ml, 置水浴上加熱 5分鐘,濾過,濾液顯溴化物的鑑別反應(附錄Ⅲ)。
(3) 本品顯鈉鹽的火焰反應(附錄Ⅲ)
含量測定
硫取本品約0.2g,精密稱定,照氧瓶燃燒法(附錄Ⅶ C)進行有 機破壞,選用1000ml燃燒瓶,以濃過氧化氫溶液0.5ml 與水30ml為吸收液,俟生成的煙 霧完全吸入吸收液後,加鹽酸2ml ,用水稀釋至200ml ,煮沸,不斷攪拌,緩緩加入熱 氯化鋇試液約20ml,至不再發生沉澱,置水浴上加熱30分鐘,靜置1 小時,用無灰濾紙 濾過,沉澱用水分次洗滌至洗液不再顯氯化物的反應,乾燥並熾灼至恆重,殘渣重量經 用空白試驗校正後,與0.1374相乘,即得供試量中含硫 (S)的重量。
溴取本品約0.2g,精密稱定,照氧瓶燃燒法(附錄Ⅶ C)進行有機破壞,選用 1000ml燃燒瓶,以0.4 %氫氧化鈉溶液10ml、濃過氧化氫溶液0.5ml 與水10ml作為吸收 液,俟生成的煙霧完全吸入吸收液後,用水稀釋至100ml ,煮沸5 分鐘,放冷,加稀硝 酸使成酸性,精密加硝酸銀滴定液(0.1mol/L)20ml,搖勻,再加硫酸鐵銨指示液2ml ,用硫氰酸銨滴定液(0.1mol/L)滴定,並將滴定的結果用空白試驗校正。每1ml 的硝酸銀 滴定液(0.1mol/L)相當於7.990mg 的溴(Br)。
藥理毒理
藥理作用本品為診斷用藥。經靜脈注射後本品幾乎全部通過肝臟加以清除。當肝功能異常時,血漿中磺溴酞鈉(BSP)清除速度減慢。定時抽取血樣,測定血液中BSP含量,觀察其清除速度即可反映肝功能狀況。
藥代動力學
注入後主要與血漿內的白蛋白和α1脂蛋白結合。在體內不發生代謝,t1/2約為5.5分鐘。本品主要經肝臟排泌入膽汁,從糞便中排出。與血漿蛋白結合的BSP到達肝細胞膜表面與蛋白質脫離,單獨進入肝細胞內,在細胞內絕大部分與谷胱甘肽結合成結合型BSP,少量呈游離狀態,然後通過肝細胞主動運轉將BSP排泌到微細膽管。正常肝功能時在注藥後45分鐘內絕大部分從血液中清除。任何使肝血流量、肝細胞攝娶轉化和排泌BSP減慢的過程都可延緩其血中清除速度。經其他器官排出量極少,不足5%。正常人在30分鐘標本內BSP瀦留量應<10%,45分鐘<6%,60分鐘應含量極微或全無。
適應症
用於肝功能檢查,靜脈注射每千克體重5mg,正常肝臟在45分鐘後大部分排出,血清中的色素應不超過注射量的5%
用量用法
注前測體重,按每千克體重靜注5mg,45分鐘後抽取血液檢查。靜注時藥液不可漏出血管外,以免造成刺激並影響檢查結果。
不良反應:
1.過敏反應包括:蕁麻疹、濕疹、呼吸困難、紫紺、心臟停搏、知覺喪失、溶血和固定紅斑等,有引起死亡報導。
2.靜脈注射可引起血栓性靜脈炎。
3.皮下滲漏可導致局部刺激和壞死。
禁忌:
1.對本品過敏者;
2.哮喘、過敏性疾病或對其他藥物有過敏史者;
3.黃疸、肝癌、肝硬變、肝脂肪變性者。
注意事項
1.個別人對本品可發生過敏反應,反覆套用後較易發生。
因本品有引發過敏反應可能,注射時和注射後必須嚴密觀察病人反應,檢查室內應備有急救藥品和器材。
2.下列情況可妨礙BSP排泄,增加血中瀦留:
(1)血膽紅素增高;
(2)肝外膽管梗阻;
(3)充血性心力衰竭、休克或大出血等情況致使肝血流量減少;
(4)發熱;
(5)肥胖;
(6)妊娠;
(7)痛風和高尿酸血症。
3.下列情況可引起BSP瀦留試驗假陰性結果:
(1)血漿容量增大;
(2)血漿蛋白濃度低下。
4.下列藥物可以影響BSP比色測定:酞類化合物、肝素及染料藥。
5.對其他檢查的干擾:
(1)血總蛋白質測定,造成假性增高;
(2)血清蛋白結合碘測定,假性增高
6.進行本試驗前病人應停用一切有色素的藥物和其他主要經肝膽系統排泄的藥物。
7.本品遇冷或久置後可析出結晶,肉眼不易察覺,注入靜脈可能發生嚴重反應,在使用本品前宜將安瓿置於水溶中加溫,振搖,使析出的結晶溶解,以減少反應。靜脈注射時必須防止藥液滲出血管外,以免引起局部刺激。
8.患者需進行膽囊或膽管造影時,BSP瀦留試驗應在其前或其後間隔數日進行。
9.臨床已見黃疸者不宜採用BSP試驗,否則結果不準確,但試驗對黃疸出現前的肝功能減退診斷有特殊價值。
藥物相互作用
碘番酸、膽影葡胺、丙磺舒、利福平、吩噻嗪類利尿藥等可能幹擾肝細胞對BSP的攝入和分泌,影響BSP瀦留實驗的結果。
貯藏
遮光,密封保存。
規格
注射液:150mg(5ml)。