介紹
登革病毒(dengue virus)屬於黃病毒科黃病毒屬中的一個血清型亞群,形態結構與乙腦病毒相似,但體積較小,約17~25nm,依抗原性不同分為1、2、3、4四個血清型,同一型中不同毒株也有抗原差異。其中2型傳播最廣泛,各型病毒間抗原性有交叉,與乙腦病毒和西尼羅病毒也有部分抗原相同。病毒在蚊體內以及白紋伊蚊傳代細胞(C6/36細胞)、猴腎、地鼠腎原代和傳代細胞中能增殖,並產生明顯的細胞病變。
登革病毒主要通過埃及伊蚊(Aedes ae-gyPti)和白紋伊蚊( Aedesalbopictus)等媒介昆蟲傳播,引起登革熱(dengue fever,DF)以及發病率和死亡率很高的登革出血熱(dengue hemorrhagic fever,DHF)和登革休克綜合徵(dengue shock syndrome,DSS)。病人及隱性感染者是本病的主要傳染源,而叢林中的靈長類是維護病毒在自然界循環的動物宿主。將發熱期患者血液接種到幼稚小鼠的腦內可被分離固定。
在我國,對登革熱的描述可以追溯到晉朝;而在西方,從16世紀開始就有了明確的登革熱病例。但是,一直到二戰發生,登革熱造成日本和盟軍士兵的大量傷亡之後,才由日本科學家和美國科學家從患者身上分離鑑定得到導致登革熱的真兇——一種被命名為登革病毒的病原體。
與其他傳染病不同的是,登革熱不能直接從一位感染者傳染給他人,而是搭乘一種叫做埃及伊蚊的蚊子大範圍肆虐。在二戰之後,亞太地區大範圍的人口遷徙和城市化給了埃及伊蚊良好的生存空間,同時它們也可以乘著飛機飛洋過海,造成登革熱的區域流行。除了埃及伊蚊以外,它的另一位近親白紋伊蚊也是散播登革熱的重要幫凶。
這些疾病廣泛流行於熱帶和亞熱帶地區,是一種分布廣、發病多、危害較大的人類傳染病。在亞洲,太平洋群島及中、南美洲等許多國家均已造成嚴重的威脅。第二次世界大戰後,在日本也曾有過流行。之後,在亞洲、非洲和南美洲的熱帶以及亞熱帶地區登革病毒感染的發病率呈明顯上升趨勢。我國於1978年在廣東佛山首次發現本病,以後在海南島及廣西等地均有發現。
生物學性狀
形態與結構
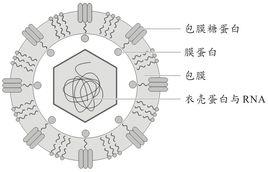
病毒顆粒呈球形,直徑約55nm。病毒顆粒外被脂蛋白包膜,並具有包膜刺突。病毒包膜的外層含有包膜蛋白E,內層含有膜蛋白M。病毒核心是由病毒的單股、正鏈RNA(+ssRNA)和病毒衣殼蛋白C共同組成的20面體核衣殼結構。病毒RNA具感染性。
基因與蛋白
登革病毒基因組RNA約含有11000個核苷酸,MW為4.2×106。其5′端為I型帽子結構,3′端缺乏poly(A)尾,基因組的5′端和3′端均有一段非編碼區。基因組只有一個開放讀碼框,其5′端1/4編碼病毒3個結構蛋白(C、PrM和E),3′端3/4編碼7個非結構蛋白(NS1、NS2a、NS2b、NS3、NS4a、NS4b和NS5)。這些蛋白是以多聚蛋白形式進行翻譯合成後,由宿主蛋白酶切割而形成的。C蛋白構成核衣殼,富含精氨酸、賴氨酸。PrM蛋白在病毒成熟時,經酶裂解形成膜蛋白M後,固定於病毒包膜內層。E蛋白是病毒包膜的主要糖蛋白,與病毒的細胞嗜性、紅細胞凝集以及誘導紅細胞凝集抑制抗體和中和抗體的產生等有關。非結構蛋白NS1功能不清。NS2a和NS2b可能參與多聚蛋白的水解過程。NS3可能是在細胞液中起作用的病毒蛋白酶。NS4a和NS4b可能與RNA複製有關。NS5是病毒編碼的依賴RNA的RNA聚合酶。
複製周期
登革病毒與敏感細胞表面受體(可能是Fc受體)結合,通過細胞吞飲和膜融合形式進入細胞後,在溶酶體酶等作用下脫殼、釋放病毒RNA。一方面,直接以病毒基因組RNA為mRNA,從單一翻譯起始點開始合成多聚蛋白前體,進而經細胞信號酶的催化進行蛋白C與PrM、PrM與E、E與NS1之間的切割。因C、PrM和E蛋白都有N-糖基化結構,主要是在細胞的粗面內質網中完成切割,並且蛋白的翻譯合成與切割是同步進行的。非結構蛋白的切割由水解酶作用完成。另一方面,在NS5聚合酶的作用下,首先以病毒基因組RNA為模板合成負鏈RNA,再由負鏈RNA複製合成子代病毒基因組+ssRNA。最後,病毒的+ssRNA和衣殼蛋白C在細胞漿中裝配成病毒核衣殼後,通過出芽釋放的形式獲得含有膜蛋白M和包膜蛋白E的病毒包膜,形成完整的病毒顆粒。
培養特性
 伊蚊
伊蚊登革病毒可以在多種昆蟲和哺乳動物細胞培養中增殖,並引起培養細胞發生折光性增強、細胞變圓或細胞融合等不同程度的細胞病變。昆蟲傳代細胞系,如白紋伊蚊C6/36等對登革病毒敏感,可用於病毒分離。哺乳動物細胞系,如人細胞系、乳地鼠腎細胞(BHK21)、胎獼猴肺細胞(FRhL)、原代狗腎細胞(PDK)等可用於病毒效價的滴定和疫苗的製備。
抗原性
根據病毒包膜蛋白E的抗原性不同,登革病毒分為1~4個血清型。各型病毒之間抗原性有交叉,但與黃病毒科的其它抗原群無交叉性。病毒包膜蛋白E的抗原決定簇既可以誘導宿主產生保護性的中和抗體和血凝抑制抗體,還可能參與登革出血熱(DHF)和登革休克綜合徵(DSS)的發生。非結構蛋白NS1和NS3均具有免疫反應性和免疫原性,可以誘導小鼠產生針對同型登革病毒致死性攻擊的保護性免疫。NS1是一種可溶性補體結合抗體,具有登革病毒的型和群特異性抗原決定簇。
變異性
登革病毒易發生變異。病毒核苷酸序列分析結果表明相同血清型病毒中不同分離株間的核苷酸變異為10%,而不同血清型病毒間的核苷酸變異為30%。並且根據病毒寡核苷酸指紋圖譜的同源程度,可以將同型病毒的不同毒株分為不同的拓撲型。由病毒變異後所形成的新的登革病毒毒株常常可引起地區性登革熱的爆發流行。抵抗力 病毒對熱敏感,56℃30分鐘可以滅活。氯仿、丙酮等脂溶劑、脂酶或去氧膽酸鈉可以通過破壞病毒包膜而滅活登革病毒。病毒經去垢劑處理後釋放出的病毒核酸可以被核酸酶迅速降解。病毒對胃酸、膽汁和蛋白酶均敏感。對紫外線、γ射線敏感。酒精、1%碘酒、2%戊二醛、2%~3%過氧化氫、3%~8%甲醛等消毒劑可以滅活登革病毒。
致病性與免疫性
傳染源與傳播媒介
登革病毒感染的自然宿主包括人、低等靈長類和蚊子。登革病毒的媒介昆蟲是伊蚊屬成員,在登革熱疫區的主要傳播媒介是埃及伊蚊和白紋伊蚊。這些伊蚊在全世界大多數地區散布存在,當叮咬感染了登革病毒的人或動物時,可以通過改換叮咬對象而直接傳播病毒。登革病毒可以在蚊子唾液腺細胞中繁殖8天~10天后隨著再次吸血而傳播。感染病毒的蚊子可以終生保持傳播登革病毒的能力,並可經卵遺傳給後代。伊蚊的卵對乾燥有很強的抵抗力,可以在體外長期存活。當人被攜帶登革病毒的蚊子叮咬時,可以通過形成蚊―人―蚊循環進行傳播和引起疾病。並且,由於登革病毒RNA的突變或新的外來毒株的侵入,常常可以引起登革熱的爆發流行。
臨床表現
登革病毒多引起無症狀的隱性感染。發病患者的主要臨床表現有登革熱、登革出血熱以及登革熱―休克綜合徵。登革熱以全身毛細血管內皮細胞的廣泛性腫脹、滲透性增強、皮膚輕微出血的病理變化為主,與病毒感染的直接作用和免疫病理損傷作用密切相關;主要表現為發熱,肌肉痛和骨、關節酸痛,伴有皮疹或輕微的皮膚出血點,血小板輕度減少。登革出血熱、登革熱-休克綜合症多發生於再次感染異型登革病毒的患者或母親抗登革病毒抗體陽性的嬰兒,病死率高。登革出血熱的病情較重,伴有明顯的皮膚和黏膜的出血症狀,血小板減少和血液濃縮顯著;登革熱-休克綜合徵除上述症狀外,主要表現為循環衰竭、血壓降低和休克等。
致病機制
病毒感染機體後,首先在毛細血管內皮細胞增殖,並釋放入血形成病毒血症,然後進一步感染血液和組織中的單核-巨噬細胞而引起登革熱。登革出血熱、登革熱-休克綜合症的可能發病機制是:
① 抗體依賴增強(antibody dependent enhancement,ADE)作用:雖然某型登革病毒感染後產生的抗體能與所有型別的病毒起交叉反應,但不能起中和作用。這些異型抗體或亞中和濃度的抗體,能與病毒顆粒相結合形成病毒抗體複合物,並通過IgG的Fc受體(FcR)結合和進入細胞繁殖,引起單核-巨噬細胞感染。這些感染的細胞可以攜帶病毒播散,引起全身性的感染。同時,機體的免疫作用、病毒抗體複合物等內源性刺激物作用被感染的單核-巨噬細胞時,可以激活細胞釋放大量的活性因子,引起瀰漫性血管內凝血(DIC)、出血、休克等一系列病理過程。
② 細胞免疫作用:CD4+細胞在病毒感染中輔助B細胞產生抗體,可能與宿主細胞的交叉免疫反應有關;並且在增殖反應中輔助T細胞產生IFN-γ,促進單核細胞FcR的表達,增強病毒感染。CD8+細胞毒性T淋巴細胞(CTL)具有血清型交叉反應性,能溶解被所有4型病毒抗原刺激或感染的細胞;可能參與病毒再次感染期間的免疫病理損傷。病毒感染可以激活各類T細胞並釋放細胞因子IL-2、IFN-γ、組胺、過敏素C3a和C5a等,從而加重感染、休克、循環衰竭和出血等表現。
免疫性
登革病毒感染形成的機體免疫主要以體液免疫為主。登革病毒感染後產生的同型病毒特異性抗體可以保持終身,但同時獲得的對其他血清型的免疫能力(異型免疫)僅持續6個月~9個月。如再次感染其它3型病毒,有可能引起DHF/DSS。病毒再次感染後激活的T淋巴細胞,可以對同型或其它型病毒發生反應,所釋放的細胞因子可能參與DHF/DSS的發生。
微生物學檢查法
大多數登革熱病例可以根據發熱、出血、肝大、休克或血小板減少等症狀進行臨床診斷。病毒分離、血清學診斷及病毒核酸檢查是確切的診斷方法。
病毒分離
可用蚊細胞培養上進行病毒分離。一般採集患者發病初期血清接種白紋伊蚊C6/36株細胞分離病毒,亦可經胸內接種巨蚊的成蚊、或腦內接種巨蚊的幼蟲進行分離。病毒分離後,可以使用登革病毒血清特異性單克隆抗體,在2周內通過間接凝集實驗進行病毒的鑑定。
血清學診斷
一般採用血凝抑制試驗進行血清學檢查。在初次感染中,血凝抑制抗體滴度於感染症狀出現後4天內一般低於1:20,但在症狀出現後1周至數周內恢復期血清中呈4倍以上的增高,可高達到1:1280。在登革病毒的再次感染中,交叉反應抗體的快速出現為主要特徵;血凝抑制抗體滴度在急性期為1:20,在恢復期可升至≥1:2560。如急性期血凝抗體滴度≥1:1280,可判定為新感染。另外,用ELISA法檢測患者血清中登革病毒特異性的IgM抗體,有助於登革病毒感染的早期診斷。
病毒核酸檢測
用逆轉錄-聚合酶鏈反應(RT-PCR)法,可以檢測病毒的雙重或多重感染。即在一對通用引物的作用下同時擴增4個型別的病毒後,經內引物擴增、核酸雜交或酶切分析的方法來進一步鑑定病毒的型別;或者用型特異的引物,直接檢測標本中的單一型別病毒。另外,用原位雜交技術可以自DHF患者的白細胞塗片或DSS死者胸腺切片中檢出不同血清型登革病毒的RNA。
預防原則
控制傳播媒介 控制傳播媒介、防止蚊蟲叮咬是防治登革病毒感染的重要措施。曾使用殺蟲劑消毒成蚊孳生地進行蚊蟲控制。但由於殺蟲劑的抗性等原因,主要通過清除蚊蟲孳生場所、開展宣傳教育增強居民自行清理蚊蟲孳生場所的意識,改善環境衛生條件等方式控制蚊蟲的數量。
預防接種尚無安全、有效的登革病毒疫苗。用DEN1~4型混合的減毒活疫苗具有一定的免疫效果;但減毒株的穩定性差,有可能引起臨床症狀和發生因ADE作用而導致的DHF和DSS。一般認為,非結構蛋白NS1不能誘導ADE作用,所以用DNA重組技術製備非結構蛋白NS1亞單位疫苗或基因工程疫苗等可能獲得滿意的免疫效果。