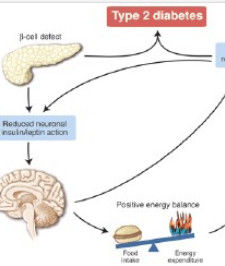
來源
 瘦素
瘦素瘦素最初主要由白色脂肪組合成和分泌,現已證實許多組織如棕色脂肪 、骨骼肌 、胃黏膜 、卵母細胞 、子宮內膜 、胎盤 、胎兒心臟和腦垂體等器官組織均可分泌瘦素。
隨著研究的深入,瘦素已經不僅僅被認為是調控體重的激素,而是能夠對機體整體生物學功能起到一定生理調控作用的整體信號系統。
瘦素是肥胖基因(ob-gene)的蛋白產物,在脂肪組織中有特異表達。某些組織器官也有瘦素表達,但量很少。人體脂肪簡單地分為皮下脂肪和內臟脂肪,前者瘦素的分泌量要明顯大於後者,因此瘦素水平主要由皮下脂肪總量來決定。
原理
瘦素與肥胖
來自美國的科學家道格拉斯·高爾曼和傑弗理·弗理德曼在20世紀60至80年代,先後致力有關方面的研究,最後成功揭
 瘦素食物
瘦素食物早在20世紀60年代,當時於美國緬因州傑克遜實驗室工作的高爾曼,在參與關於糖尿病和體重問題的老鼠實驗後,提出體重是與生物本身基因有密切關聯的科學猜想。他在受訪時憶述,隨後即開始了關於2種因基因突變而出現嚴重肥胖的老鼠的研究,結果成功發現,部分老鼠因無法產生某種抑制食慾的激素而致肥,另一部分則製造過量相關激素,但因身體缺乏接收有關激素訊息的受體,令其出現肥胖問題。
高爾曼設立的體重與激素及基因之間的假設,在80年代被於紐約洛克菲勒大學工作的弗理德曼重拾,他在長達10年的試驗中,終於定位了一種導致老鼠體重問題的基因,並將其命名為“瘦素”;他證實了某些人的確是在激素信號傳遞失衡的情況下產生肥胖,甚至因此胰島素失衡帶來糖尿病。這項“接力式”的合作科學成果為肥胖問題研究帶來革命性的改變,而弗理德曼亦將繼續嘗試從中尋找可完全治療肥胖的有效方式。
道格拉斯·高爾曼發現,極少數人食量驚人,因為他們在體記憶體在著瘦素基因突變,產生的瘦素太少,這種病人在接受瘦素替代療法以後體重迅速下降,所以瘦素的發現讓人們對肥胖症的理解和認識有了飛躍,又向著擺脫肥胖邁進了一步。由於瘦素對於治療肥胖症有著非常好的療效,堪稱“減肥素”。預計在不久的將來以瘦素為主要成分的減肥藥,也很有可能會出現在我們的生活當中,從而在很大程度上改變普通人的生活。
發現背景
歷史
1994年Zhang等首次發表了利用定位克隆技術成功克隆了小鼠的ob基因和人類的同源序列並由基因預見ob蛋白的論文,開創了人類肥胖和能量代謝研究的新領域。Halaas等於1995年套用DNA重組技術,由大腸桿菌中合成ob基因的表達產物,將該蛋白命名為——瘦素(leptin)。其主要功能是對能量平衡及體重進行調節。人血漿瘦素水平升高與人體脂肪重量成正比,瘦素及其受體基因突變可導致病態肥胖。在一項為期24周的研究中,每日皮下注射瘦素可使體重有不同程度的減輕。近年來研究發現,肥胖患者體內瘦素轉運至大腦的能力下降,從而造成肥胖個體的瘦素抵抗。因此,有研究者正致力於能通過血腦屏障的瘦素小分子類似物的研究,以開發有潛力的肥胖治療藥物。目前研究中的作用於瘦素受體的物質多為合成的短肽類物質,而小分子化合物還未見報導。
Wang等人的研究(2004)認為,瘦素,一種在脂肪組織中的胺基酸,它的作用在於存儲葡萄糖、降低體重、增加熱量、促進和刺激青春期的下丘腦—垂體—性腺軸發育成熟。他們發現:第二性徵的變化,如乳房萌芽(thelarche)和睪丸/陰莖增長呈正相關,為的是提高9到11歲的男女孩的血液凝集素水平和體重指數(BMI)測量值。此後,他們發現瘦素水平在女孩中持續增加,而在男孩中卻有所下降:在女孩中脂肪的增加是對雌激素減少生產做出的反應,而在男孩中減少是由於肌肉質量的構建。
肥胖已經成為危害人類健康的一大因素,科學家們進行了大量研究旨在找出擊退“大敵”的方法。英國媒體報導稱,英國白金漢大學克洛雷試驗中心主任邁克·考索恩教授提議將一種名為瘦素的激素加入嬰兒食品,尤其是嬰兒牛奶中,食用這種食品後嬰兒的一生就不會再有發胖的擔憂。
瘦素是一種由脂肪組織分泌的激素,人們之前普遍認為它進入血液循環後會參與糖、脂肪及能量代謝的調節,促使機體減少攝食,增加能量釋放,抑制脂肪細胞的合成,進而使體重減輕。科學家在去年的研究表明,在嬰兒時期攝取瘦素,可能可以固定大腦對食慾的反應,進而一生都不會過度飲食。
人們是在對老鼠的實驗中得到了這個發現的。據考索恩教授介紹,實際上在人類母乳中也含有這種物質,"含有添加物的牛奶不過是把原本就存在的東西的量增大了而已"。不過這一研究還處於最初階段,至少需要10年的時間才可能最終研製出可防止肥胖的嬰兒食品。
考索恩教授的計畫在科學界引起了極大爭議,人們最大的擔心就是它的安全性,比如劑量和副作用等問題。另外還有批評者認為這還涉及到倫理問題,他們認為肥胖是一種現代社會帶來的疾病,人們需要檢視並改變自己的生活方式來避免患病,而不僅僅是尋找一種可以快速解決問題的人工合成物。
最新調研顯示,肥胖已經稱為歐洲面臨的主要健康和社會負擔,兒童肥胖趨勢尤其令人擔憂。英國是歐洲兒童肥胖程度最高國家之一,超重兒童約占30%。
減肥效果
1999年11月,一位學者披露了他的研究結果,說是用瘦素治療肥胖症,可以加快體重下降速度,而使用大劑量瘦素則可使身體脂肪減少更多。在對123名肥胖者進行的4周試驗表明:使用0.01毫克瘦素者,體重下降了0.7公斤;使用0.10毫克者,下降了2.4公斤;使用0.30毫克者,則平均下降7公斤。生物學特性
瘦素結構特徵
瘦素由ob基因編碼,是一種主要由白色脂肪細胞分泌的反饋性抑制脂肪的激素樣蛋白質。血液循環中的瘦素為146個胺基酸的蛋白質,分子量為16KD,以單體存在於血漿中。瘦素具有1級細胞因子家族特有的四螺鏇束結構,該結構使其疏水性殘基大量曝露在外,部分殘基在識別受體上起著重要作用。另外,瘦素分子呈現自我締合和分子間聚集的趨勢。
天然的靈長類瘦素序列在生理條件下極易呈現物理性聚集,但其低溶解性使其結晶化過程受阻。通過定點誘變作用,瘦素表面的物理性結構及其分子間互作模式能夠被完全改變以適應結晶化。
分泌規律
瘦素的分泌呈脈衝式,動物的體重、進食和飢餓狀態可以影響脈衝的頻率和幅度。瘦素mRNA表達呈日周期變化,夜間表達量最高。禁食使瘦素表達和分泌顯著減少,同時日周期節律消失,再時食可使之恢復正常。
存在形式
在血液中的運輸有游離和結合兩種形式,在人血清中每種運輸形式各占50%,其中,游離型形式具有生物活性,是脂肪組織和中樞神經系統網路聯繫的外周信號。瘦素的血漿水平可同時受多種因素的調節,如飲食、體溫、一些酶類及細胞因子的分泌等。禁食不影響瘦素的游離和結合比例,但在肥胖的人和鼠,該比例發生變化,而且體重指數越高,游離型越多,這暗示著肥胖機體瘦素的運輸、清除及至生物活性發生了變化。
作用部位
主要在中樞神經系統,血清中瘦素通過血腦屏障進入腦內是其發揮作用的重要環節。靜脈注射I125-lep tin進入腦的擴散常數比I125標誌的白蛋白高出20倍,這一轉運過程存在飽和性,並可被未標記的瘦素竟爭性抑制,說明中樞系統存在特異的瘦素轉運系統。
影響因素
1、具有促瘦素分泌功能的因子:有胰島素、類固醇激素和去甲腎上腺素。將糖皮質激素直接作用於脂肪組織,對瘦素的合成和分泌具有最顯著的促進效應,前列腺素E2和花生四烯酸也同樣被證明能夠刺激瘦素的釋放。
2、抑制因子:已報導高含量環磷酸腺苷能夠抑制瘦素的釋放,由此推斷腺苷酸環化酶激活因子如福斯高林(血小板凝集抑制劑)和異丙腎上腺素能夠抑制瘦素分泌。細胞內游離鈣濃度的提高能夠抑制胰島素刺激導致的瘦素分泌,且其抑制水平不依賴於葡萄糖代謝。另外,褪黑激素也被證明能夠降低瘦素的生成。
作用原理
瘦素受體已證實6種亞型。其中以ob-Rb為主的長型受體主要存在下丘腦神經元,以ob-Ra為主要的短型受體多分布於脂肪、心肺等外周組織。瘦素受體的分布不同決定瘦素作用的多樣性,但其主要作用是調節機體脂肪的穩定。Ob-Rb是主要的功能受體,而ob-Ra受體的生物作用尚不清楚。
當外周脂肪增多時,血中瘦素水平升高,通過抑制乙醯輔酶A羧化酶來抑制脂肪的合成。並與下丘腦長型受體結合,通過多種神經內分泌的激素的作用,引起食慾下降,機體消耗增加,體重減輕。同時下丘腦發出神經衝動興奮交感神經釋放去甲腎上腺素,使大量儲存的能量轉變為熱量,從而減少體內脂肪含量。
瘦素還作用於外周組織器官,影響機體許多生理系統和代謝通路。
生理功能
瘦素的生物功能主要表現在對體脂及體質量的調控。此外,瘦素還可調節免疫應答功能、促進上皮細胞的以及新生血管的生長、促進胎兒發育、調節生殖功能等。
影響脂肪代謝調控
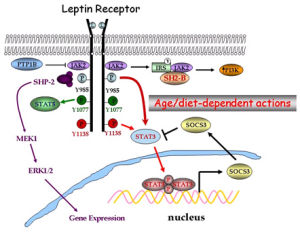 瘦素受體985位酪氨酸介導的信號通路在能量代謝平衡中的調控功能
瘦素受體985位酪氨酸介導的信號通路在能量代謝平衡中的調控功能 瘦素在調節體重、脂類代謝以及脂肪組織的編程性細胞死亡和微血管構成上起著關鍵作用。瘦素可通過特殊方式經血腦屏障進入腦脊液,與下丘腦中瘦素受體結合,影響神經肽Y NPY的合成和釋放,通過神經肽Y的減少抑制攝食並降低產熱。電生理學方法也證明,瘦素可抑制大鼠下丘腦弓狀核神經元,影響NPY的信號轉導,引起食慾減退和體重下降。
瘦素還可以增加下丘腦促黑激素(MSH)的分泌,而MSH具有明顯的食慾抑制作用。進一步研究發現不同部位注射瘦素對動物的採食量和體重影響不同,並有劑量和時間效應。另外,瘦素可作為脂肪一胰島軸的一部分,參與胰島素分泌及其敏感性的調節並發揮抑制作用;而胰島素能刺激瘦素釋放,它們之間形成一個雙向反饋環。
影響動物的生殖發育
除了在採食調控和能量消耗上的重要作用,瘦素在生殖和發育方面也起著重要的作用。
瘦素在生殖和發育的信號傳遞中起重要作用,它可作用於下丘腦—垂體—性腺這一生殖軸的各個層次。瘦素通過位於下丘腦的長型受體調節性行為和促性腺激素釋放激素(GnRH)釋放。經腦室注入瘦素可減少卵泡刺激素(PSH)催乳素(PRL)促黃體激素(LH)分泌。此外,瘦素能啟動雌性小鼠的青春期發育和性成熟。研究表明,瘦素可調節胚胎植入前的發育及宮腔的準備並對早期胚胎髮育、著床過程和維持姓娠有重要作用。也是維持正常發情周期的必需因子。
影響系統免疫
瘦素具有影響水鹽代謝、致使飲水增加、尿液稀釋、腎臟排鉀減少、增加機體免疫應答能力的作用。
在外傷性的損傷中,可檢測到瘦素的顯著升高。體內及體外的實驗也證實,機體在炎症狀態下瘦素濃度增高,激活並趨化中性粒細胞,刺激單核—巨噬系統、促進淋巴細胞的增殖、誘導外周血白細胞介素-6及腫瘤壞死因子-等炎性因子的表達,參與炎性反應。在胰腺炎的動物實驗中發現,外源性瘦素保護了動物胰腺,其可能與活化了一氧化氮氧化途徑有關。另外瘦素還具有抑制前炎性細胞因子,降低白細胞的滲透及促進組織修復的作用。
人類臨床醫學研究還發現瘦素與乳腺癌、結腸癌、前列腺癌、卵巢癌等相關。在體外培育的人類乳腺癌細胞中,瘦素通過與受體結合引起信號轉導因子和轉錄活化子、細胞外信號調節激酶及激活蛋白1介導的磷酸化,並證實瘦素誘導了絲裂原活化蛋白激酶依賴的細胞增殖途徑。同時,瘦素還促進雌激素的合成及雌激素受體的增加從面調節了乳腺癌細胞的生長、分化、增殖。因此,瘦素還拮抗了乳腺癌治療中抗雌激素的藥物的作用。
影響骨代謝
目前(2012年)尚未發現成骨細胞上有瘦素受體的表達。經腦室注入瘦素可抑制骨形成,可能是通過中樞途徑增強成骨細胞功能,影響骨重建,對破骨細胞分化功能無明顯影響。絕經後肥胖婦女發生骨質疏鬆的危險性下降(A Sahu 2000,ob/bo小鼠、db/db小鼠呈肥胖伴骨密度增強),據此推測瘦素在骨代謝中發揮作用。
瘦素可通過中樞神經系統影響骨代謝。諸多研究表明,瘦素在中樞神經系統是一個骨形成的抑制因子。Thanas等研究顯示,瘦素能夠提高成骨細胞分化產物,這種作用呈劑量和時間依賴性,可使成骨細胞基質礦化水平增加59%。表明瘦素能夠促進成骨細胞的分化,由於瘦素信號缺失導致成了骨形成增加,其證據是先天缺乏脂肪的轉基因小鼠由於沒有脂肪而瘦素水平極低,但儘管其體重減輕,卻表現出高骨量。
其他功能
近年來研究發現,瘦素還與肝臟纖維化、上皮細胞的增殖、新生血管的生長、造血、胎兒發育等生理過程密切相關。另有研究表明瘦素mRNA在胎兒皮下組織的表達和胎兒脂肪組織發育有關。盤有瘦素分泌,胎兒皮下脂肪組織內有瘦素及其長鏈瘦素受體存在,進一步研究發現瘦素在胎兒脂肪組織的發育過程中有自分泌和旁分泌調節作用。
套用前景
在畜牧業上,可以利用瘦素水平調控動物採食,從而控制動物脂肪含量,提高動物產品的適口性及營養價植。通過遺傳育種手段,培育瘦型或肥胖型動物模型,以用於動物和人類肥胖的深入研究。另外,通過控制動物內瘦素水平增強動物免疫力,提高動物生產性能;研發瘦素產品,提高動物生產性能並套用於相關的動物疾病治療。
相關研究
2012年10月,美國哈佛醫學院的研究人員發現,果蠅能夠大量炮製一種名為瘦素的激素,這一發現是研究者對缺乏一種名為Upd2的營養感知蛋白質的果蠅進行研究時所獲得的。研究人員推測,Upd2是瘦素的“功能性同族體”,從而意味著果蠅中的這種蛋白質所起的作用與人體中的瘦素非常類似。由於果蠅在實驗室中相對容易研究,因此這一發現有望揭開關於這種激素的更多秘密。