流行病學
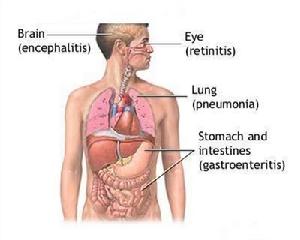 巨細胞病毒病發病機制
巨細胞病毒病發病機制2.傳播途徑 母嬰垂直傳播是巨細胞病毒病感染的重要途徑。病毒通過帶毒孕婦產道、哺乳、飛沫或密切接觸的方式在圍產期傳播給新生兒,也可直接通過胎盤導致宮內傳播感染率大約為10%。
CMV感染的水平傳播主要通過與患者的密切接觸而發生,也可能經性交傳播,因此被世界衛生組織列入性傳播疾病範疇。病毒可存在於患者器官上皮細胞、血管內皮細胞,以及白細胞內;故接受器官移植、輸入污染血製品也是感染的途徑之一。
3.易感人群 人群普遍易感,年齡越小易感性越高,臨床表現也越重,年長兒及成人則大多數為隱性感染人群中血清CMV抗體的檢出率隨年齡增加而增高育齡婦女中20%~50%為陽性,60歲以上成人大多為陽性。生活在低收入水平居住擁擠地區的兒童,CMV抗體陽性檢出率幾乎可達百分之百。
CMV感染後多數人可產生抗體並持續存在,但其僅有不完全的免疫保護作用;因此,血清抗體陽性者仍可能存在有潛伏感染,呈長期帶毒狀態,並可在一定情況下被激活;甚或遭受二次感染。
病因
CMV歸屬於人皰疹病毒科β亞科具有明顯的宿主種屬特異性,是人皰疹病毒科中最大、結構也最複雜的病毒;CMV呈球形直徑約為300nm,由雙層含脂糖蛋白外膜所包被;其基因組為230kb的線性雙鏈DNA分子,含有約200種蛋白質的編碼基因。CMV對外界抵抗力差,65℃加熱30min、紫外線照射5min、乙醚等均可使之滅活,亦不耐酸。CMV只有一個血清型常用ADl69作為代表株進行血清學檢測試驗。
發病機制:
巨細胞病毒可廣泛存在於受染患者全身各器官組織內,感染可直接導致受染宿主細胞損傷;此外還可能通過免疫病理機制產生致病效應。
巨細胞病毒主要侵犯上皮細胞全身各主要臟器(肺、肝、腦、腎、脾、心腸),腺體(涎腺、性腺),及神經系統等均可受累。受染細胞變性,體積增大呈巨細胞化,然後崩解,導致局部壞死和炎症腦組織壞死後可以發生肉芽腫和鈣化受染細胞發生巨細胞樣變後具有以下特點:細胞體積顯著腫大,達10~40 μm;胞核也變大,胞質則顯得相對較少,胞質及胞核內均可出現包涵體。胞核內可見嗜酸性包涵體,呈紅色,周圍繞以透亮暈環,與核膜分開,使其整個外觀狀似貓頭鷹眼。
臨床表現
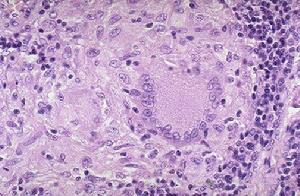 巨細胞病理圖
巨細胞病理圖對機體處於免疫抑制狀態的患者,CMV感染可導致嚴重的臨床表現。由於器官移植術受者常須接受免疫抑制處理,故CMV感染是器官移植術後嚴重併發症的主要病因之一如肝炎潰瘍性胃腸道炎、肺炎等;有的可導致術後死亡,或被迫摘除已移植的器官此類患者的CMV感染主要來源於供者(供體器官及移植手術所需的大量輸血中均可能潛伏有CMV感染),但亦可能系因患者原有CMV隱伏感染的激活,不過後者的病情可能較前者為輕。人巨細胞病毒病也常見於HIV(人類免疫缺陷病毒)感染者。HIV感染髮病成為愛滋病患者後,則易形成全身播散性CMV感染,系愛滋病患者的一個重要死因。
2.宮內感染 系孕婦體內的CMV通過胎盤使胎兒在宮內受染是人巨細胞病毒病感染的重要途徑之一受染胎兒90%為隱性感染,僅10%表現為臨床感染但有時後果較為嚴重,尤其當感染髮生在妊娠頭4個月內時,更易造成胎兒損害。例如部分受染胎兒呈現發育遲緩,出生時體重不足,或呈各種形式的先天畸形,如小頭畸形、肢體畸形、先天性心臟病、斜眼失明等或在出生後短期內出現黃疸、肝脾腫大肺炎心肌炎、出血傾向、嗜睡、昏迷、抽搐等多系統器官損害,可於數星期內死亡。
CMV宮內感染也可造成死胎流產早產。在一組3810的新生兒流行病學調查中,臍血標本的抗-CMV-IgM的陽性檢出率為1.5%;而在該組40例死產、死胎的臍血標本中,抗-CMV-IgM的陽性檢出率則高達32.5%。
併發症:
CMV宮內感染是導致流產及先天性殘障兒的一個重要病因。在出生時外觀狀似正常的宮內受染新生兒中,約5%~10%於生後數年內將不同程度地出現聾啞、智力愚鈍、行為異常、運動失調等軀體或精神發育障礙鑒於弓形蟲病(toxoplasmosis,即“T”)、其他病原體(others,即“O”)、風疹病毒(rubella virus,即“R”)、巨細胞病毒(cytomegalovirus,即“C”)、單純皰疹病毒(herpes simplex virus,即“H”)均可經宮內感染導致類似的危害因而一起被統稱為“TORCH綜合徵”,是生殖保健醫學所面臨的重要課題之一。
此外,已有研究表明,CMV感染可能有致癌作用,還可能是發生冠狀動脈狹窄症的病因之一。
診斷
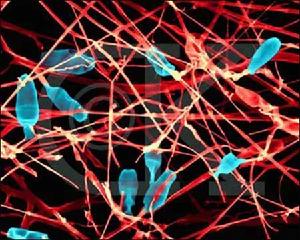 血小板病理圖
血小板病理圖外周血抗-CMV IGM陽性表明新近存在CMV感染,對於嬰幼兒患者可診斷巨細胞病毒病。由於孕婦外周血IgM型抗體不能通過胎盤屏障所以若新生兒臍血抗-CMV IgM檢測陽性則可診斷CMV宮內感染(採集臍血標本時應注意避免母血污染)嬰幼兒外周血僅單一抗-CMV IgG檢測陽性者應連續隨訪6~12個月,觀察其滴度是否有顯著意義的升高。由於成人人群中CMV抗體檢出率很高,故檢測CMV抗體用於成人患者診斷巨細胞病毒病的意義有限。
用PCR技術檢測患者標本中的巨細胞病毒基因有助於確診巨細胞病毒病;可早在出生後頭3周,就能從新生兒的尿液或唾液標本中檢測出CMV的存在,為CMV的宮內感染提供依據。
近年有報導,對於腎移植手術的陽性供者和受者,利用高靈敏度的試劑盒定量檢測其血清CMV抗原滴度,可有助於決定是否進行抗病毒治療。
檢查:
較重患者可有白細胞數增高,血中出現變異淋巴細胞;嬰幼兒患者常伴貧血、血小板數減少;累及肝臟導致CMV肝炎的患者出現肝功能異常。
利用PCR技術進行CMV基因檢測,可提供病毒在患者體記憶體在的直接證據;其靈敏度很高,可在數小時內做出檢測報告,已成為臨床診斷CMV感染或帶毒狀態的重要手段;但須在經過技術認證合格的實驗醫學實驗室內進行,並在操作過程中應注意避免污染,嚴格控制反應條件,以排除PCR技術可能導致的假陽性反應。
治療
 巨細胞病毒病藥物
巨細胞病毒病藥物更昔洛韋是阿昔洛韋的衍生物,實驗室觀察可抑制巨細胞病毒DNA的合成。臨床試用於巨細胞病毒病患者的劑量為:緩慢靜脈滴注更昔洛韋2.5mg/kg體重,1次/8h或5mg/kg體重,1次/12h共2~3周經初步觀察,此藥有一定近期療效,但停藥後病毒又可重新複製活躍,故需用藥維持數月甚至數年;由於此藥有一定毒性,例如使白細胞、血小板數減少等,故而往往難以堅持長期使用。對阿昔洛韋過敏者亦禁用此藥。此外,臨床上已發現一些CMV毒株對更昔洛韋表現出不同程度的耐藥性;而且此藥對巨細胞病毒性肺炎無效。
預後
一般成人或兒童患者發生CMV臨床感染後大多預後良好對機體處於免疫抑制狀態的患者,例如器官移植術受者、愛滋病患者、接受化療或放療的晚期癌症患者,CMV感染可導致嚴重的臨床表現,或加速其死亡。CMV宮內感染可導致流產或死產。
預防:
對CMV抗體陽性的孕婦須加強圍生期醫學保健,必要時,抽取羊水進行CMV抗體的檢測陽性者(尤其抗-CMV IgM陽性)則提示已發生CMV宮內感染。據調查表明,此類婦女再度妊娠後發生胎兒CMV宮內感染的機率則減少,故可與患者夫婦討論本次妊娠是否考慮人工流產。尤其對本次宮內感染髮生的時間可能系在妊娠頭4個月內且本次妊娠又屬該例婦女首次受孕者具有CMV宮內感染的較高風險。人工流產可能有利於優生優育。但若患者夫婦因某種緣故不易受孕,本次妊娠屬珍貴兒,則不能貿然做出決斷,可輔以B超檢查胎兒協助決策。
