定義
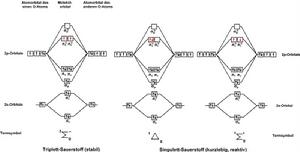
激發態氧分子。基態氧原子(三線態氧分子)被激發後,原本兩個π2p*軌道中兩個自鏇平行的電子,既可以同時占據一個π2p*軌道,自鏇相反,也可以分別占據兩個π2p*軌道,自鏇相反。兩種激發態,S=0,2S+1=1即他們的自鏇多重性均為1,是單重態(分別用1Δg和1Σg+表示)。因此,激發態氧分子又成為單線態氧1O2。
| 電子態 | π*2p 軌道電子排布 | 符號 | 高出基態的能量/kJ·mol-1 |
| 第二激發態 | ↑↓ | Σg(O2) | 154.8 |
| 第一激發態 | ↑↓ | Δg(O2) | 92.0 |
| 基態 | ↑↑ | Σg (O2) | 0 |
壽命
1ΔgO2:10^-6s~10^-5s1Σg+O2:10^-9s
1ΔgO2>>1Σg+O2,因此通常說的單線態氧就是1Δg。
單線態氧的壽命與其所處環境密切相關,在氣體環境室溫下,可達到1小時以上(有報導為72 分鐘),而在溶液不同溶液中壽命不同。
單線態氧在不同溶劑中的壽命:
溶劑 | τ(1Ο2)/μs |
水 | 2 |
乙醇 | 10 |
環己烷 | 16 |
正丁醇 | 19 |
重水 | 20 (32) |
苯 | 24 |
丙酮 | 25 |
重氫丙酮 | 25 |
乙腈 | 30 |
吡啶 | 33 |
叔丁醇 | 34 |
氯仿 | 60 |
二硫化碳 | 200 |
六氟苯 | 600 |
四氯化碳 | 700 |
氟利昂Ⅱ(CF3Cl) | 1000 |
製備
基態氧分子吸收光直接產生1O2是不可能的,躍遷高度禁阻。可以通過光敏化法、微波放電法和化學方法得到。1.光敏化法就是在光敏化劑作用下對基態氧進行輻照。常用的光敏化劑是一種螢光性染料(如螢光黃、亞甲基藍、葉綠素等),可表示為:
敏化劑----hv--->敏化劑T1
敏化劑T1+O2(基)----能量傳遞--->敏化劑+1O2
2.化學反應製備:H2O2+ClO- ----EtOH--->1O2+H20+Cl-
相關反應
1.主要是1,2-、1,3-及1,4-烯烴的加成:R2C=CR`2+1O2----->---hv或△--->R2CO+R`2CO
2.1O2在體內會不斷生成與猝滅,並且在多種生理及病理過程中起作用(包括好的和壞的)。例如,在染料光敏化氧化條件下,各種生物成分(蛋白質、胺基酸、核酸等)很容易與氧反應而使有機體損壞,如在動物和人體中會引起蛋白質光氧化疾病等。
圖解