根據化學式式量的化學計算
 化學計算
化學計算例1:某工廠用一氧化碳還原氧化鐵來生產鐵,已知有氧化鐵160噸,問:恰好反應可以生產出鐵多少噸?(可能用到的式量:Fe---56 O----16 C----12)
解:設生產出氧化鐵的質量為x。
高溫
3CO+Fe2O3=2Fe+3CO2
160 112
160t x
160 112
160t/x=160/112
160x=112×160t
x=17920t/160
x=112t
答:理論上可生產出鐵的質量為112t。
用摩爾質量的化學計算
給出一個方程式,根據已知的摩爾數(物質的量)來進行物質質量求算
公式:
m
n=—
M
*n為物質的量,單位:mol
M為物質的摩爾質量,單位:g/mol
m為物質的質量,單位:g
例2:氫氣和氧氣化合成為水,已知:氫氣2mol,問:生成水幾克?
解: 設生成xmol水
2H2+O2=2H2O
2 2
2 x
x=2
m
∵n=—
M
∴m=nM
=2×18
=36克
答:生成水36克
3.加熱分解6.3g高錳酸鉀,可以得到氧氣的質量是多少?
【解】(1)設未知量
設:加熱分解6.3g高錳酸鉀可以得到氧氣的質量為X
(2)寫出反應的化學方程式
(3)寫出相關物質的化學計量數與相對分子質量的乘積以及已知量,未知量
KMnO4==加熱==K2MnO4+MnO2+o2
2×(39+55+4*16) 1*(2*16)
6.3g X
(4)列出比例式求解
32分之2*158=x分之6.3g
x=2*158分之32*6.3g=0.6g
(5)簡明地寫出答案
答:加熱分解6.3g高錳酸鉀,可以得到0.6g氧氣。
巧妙結合數學和函式圖象簡化化學計算
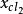 化學計算
化學計算例:氯氣和二氧化氮在室溫下可以化合生成一種新的氣態化合物A,為了測定A的組成進行以下實驗:取Cl2、NO2混合氣體總體積5L,測定反應後所得氣體體積隨Cl2在原混合氣體中所占體積分數 的變化而變化的規律。實驗測知當Cl2所占體積分數為0.2或0.6時。反應後氣體的總體積均為4L。下列說法正確的是( D )
A.A的化學式為NClO3
 化學計算
化學計算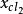 化學計算
化學計算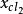 化學計算
化學計算B.當為0~ 時,反應後總體積V隨 變化的函式關係為:V=4 +3.2
 化學計算
化學計算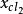 化學計算
化學計算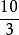 化學計算
化學計算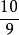 化學計算
化學計算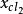 化學計算
化學計算C.當為 ~1時,反應後總體積V隨 變化的函式關係為:V= +
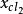 化學計算
化學計算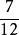 化學計算
化學計算D.當 為 時,反應後總體積V=3.96L

