物質簡介
發現歷史
 內華達州境內的家用液化石油氣罐的運輸
內華達州境內的家用液化石油氣罐的運輸1911年,沃爾特博士已經能夠製備高純度的丙烷並在同年3月25日獲得專利,專利號碼為1056845。另一個由弗蘭克·彼得斯發明的通過壓縮製備石油液化氣在1912年獲得專利。
在1920年代,液化石油氣的產量激增,現有的最早記錄顯示在1922年共生產了223000加侖。1927年,年銷量已經接近100萬加侖。而到了1935年,年銷量已經達到560萬加侖。1930年代工業上的主要發展包括使用軌道交通運輸、加入惡臭氣體以及增加丙烷填充終端。1945年,液化石油氣的年銷量達到了10億加侖。截止1947年,62%以上的美國家庭用上了天然氣或丙烷作為做飯的燃料。
1950年,芝加哥運輸管理局訂購了1000輛以丙烷作燃料的汽車。截止1958年,美國國內的年銷售量已經達到70億加侖,2004年,有報告稱整個丙烷產業價值80億美元至100億美元,年消耗量超過150億加侖。
北京奧運會火炬-祥雲便是以丙烷作為燃料的,它價格低廉,而且溫度範圍比較寬,燃燒只形成水蒸氣和二氧化碳,沒有其他物質,不會對環境造成污染,是一種清潔燃料,符合“綠色奧運”的理念。丙烷氣體燃燒的火焰顏色為亮黃色,這樣的顏色能滿足方便識別和電視轉播、新聞攝影的需要。
物質來源
丙烷是處理天然氣或精煉原油得到的副產物。在處理天然氣的過程中,必須將丁烷、丙烷和大量的乙烷從原氣中去除,否則這些揮發物會在天然氣管道中發生縮合。精煉原油的過程中,丙烷作為一個副產物出現在裂解石油製備汽油和燃料油的過程中。由於是副產物,丙烷的產量不能夠輕易的根據需求而轉變。
物質結構
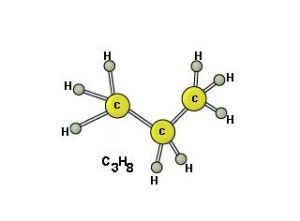
分子結構:C原子以sp3雜化軌道成鍵、分子為極性分子。結構簡式:CH3-CH2-CH3
理化特性
物理性質
 丙烷分子式
丙烷分子式外觀與性狀:無色氣體,純品無臭。
熔點(℃):-187.6(85.5K)
沸點(℃):-42.09(231.1K)
相對密度:0.5853(-45/4℃)
燃點(℃):450,易燃
相對蒸氣密度(空氣=1):1.56
飽和蒸氣壓(kPa):53.32(-55.6℃)
燃燒熱(kJ/mol):2217.8
臨界溫度(℃):96.8
臨界壓力(MPa):4.25
閃點(℃):-104
引燃溫度(℃):450
爆炸上限%(V/V):9.5
爆炸下限%(V/V):2.1
溶解性:微溶於水,溶於乙醇、乙醚。
CAS號:74-98-6
相對不溶於水,在低溫下容易與水生成固態水合物,引起天然氣管道的堵塞。丙烷在較高溫度下與過量氯氣感化,生成四氯化碳和四氯乙烯Cl2C=CCl2;在氣相與硝酸作用,生成1-硝基丙烷CH3CH2CH2NO2、2-硝基丙烷(CH3)2CHNO2、硝基乙烷CH3CH2NO2和硝基甲烷CH3NO2的混合物。上丙烷可從油田氣和裂化氣中分離得到。可作出產乙烯和丙烯(C3H6)的原料或煉油產業中的溶劑;丙烷、丁烷(C4H10)和少量乙烷的混雜物液化後可用作民用燃料,即液化石油氣(LPG)。
化學性質
同其他烷烴一樣,丙烷可以在充足氧氣下燃燒,生成水和二氧化碳。C3H8+5O2→3CO2+4H2O+熱量
當氧氣不充足時,生成水和一氧化碳。
2C3H8+7O2→6CO+8H2O+熱量
和天然氣不同的是,丙烷比空氣重(大約是空氣的1.5倍左右)。在自然的狀態下,丙烷會下落並積聚在地表附近。在常壓下,液態的丙烷會很快的變為蒸汽並且由於空氣中水的凝結而顯白色。一立方英尺的丙烷若完全燃燒能夠放出2500BTU的熱量(91,600BTU每液體加侖)。國際單位制中,一立方米丙烷的高熱值是50千焦(≈13.8kWh)或101MJ/m3。
丙烷在標準狀態下是無毒的,但是若濫用做吸入劑,有一定因為缺乏氧氣而窒息的危險。同樣值得注意的是,商業產品中通常含有其他可能導致危險的碳氫化合物。在常壓下,丙烷及其混合物快速揮發能造成凍傷。在外界溫度是20攝氏度的情況下,丙烷液體仍然保持-42度的低溫。
液化石油氣的燃燒比汽油清潔,但略遜於天然氣。由於C-C單鍵以及丙烯和丁烯中雙鍵,液化石油氣在通常情況下燃燒會產生除了二氧化碳和水之外的有機廢氣。同樣是這些鍵的原因,液化石油氣燃燒存在可見的火焰。
丙烷用途
常見用途
 零售液化石油氣罐
零售液化石油氣罐工業用途
目前隨著工業的發展,丙烷逐漸成為一種重要的石油化工原料。在石油化工上,丙烷可作為蒸汽裂化製備基礎石化產品的給料;由於丙烷與丙烯之間存在著巨大的價格差,而且丙烷資源豐富,目前全球很多公司紛紛研究用丙烷作原料生產丙烯和丙烯腈的工藝。
其他用途
丙烷的其他用途包括:蒸汽裂化製備基礎石化產品的給料。
在某些火焰噴射器中充當燃料或加壓氣體。
生產丙醇的原料。
熱氣球的主要燃料。
半導體工業中用來沉澱金剛砂
混合有矽的丙烷被用作一種氣槍的推進劑(銷售時稱作綠氣),用於生存遊戲中。
在一些主題公園和電影拍攝里,液態的丙烷被用作一種便宜而又高能量的物質來產生爆炸或一些其他的視覺效果。
製備方法
1.在石油開採和煉製時,可作為石油氣收集。石油餾分在裂化和催化裂化時,也有大量的丙烷生成。故與丙烷共存的雜質有甲烷、乙烷、丁烷、乙烯、丙烯以及低沸點硫化物、水分等。2.精製時將石油經蒸餾和裂化等過程中生成的氣體用油吸收,活性炭吸附,壓縮和冷卻使之液化等方法進行濃縮,再於低溫或加壓下分餾以分離丙烷。丙烯等不飽和成分可用濃硫酸除去或進行氫化。含硫化合物可用鹼洗滌或用脫硫劑除去。水分用濃硫酸、乙二醇、固態乾燥劑(如白土、氧化鋁類)和金屬鈉等脫水,也可用共沸蒸餾的方法除去。丙烷的回收一般用蒸餾,也可用高沸點的烴類吸收或用吸附劑吸附的方法回收。
3.以液化石油氣為原料,在0~5℃下冷凝,除去部分高沸點雜質後,進入吸附器中,先後除去原料氣中的水、丙烯、乙烯、乙烷、正丁烷、異丁烷、正丁烯、異丁烯等烴類雜質,再進入冷凝器,將丙烷凝為液體,並與氮、氧等不凝氣分離,即可。丙烷提取率可達80%以上。
使用安全
健康危害
本品有單純性窒息及麻醉作用。人短暫接觸1%丙烷,不引起症狀;10%以下的濃度,只引起輕度頭暈;接觸高濃度時可出現麻醉狀態、意識喪失;極高濃度時可致窒息。燃爆危險:本品易燃。
毒性特點:丙烷屬微毒類,為純真麻醉劑,對眼和皮膚無刺激,直接接觸可致凍傷
應急措施
吸入急救如遇人體丙烷吸入情況應迅速將遇害者脫離現場至空氣新鮮處。保持呼吸道通暢。如呼吸困難,給輸氧。如呼吸停止,立即進行人工呼吸。就醫。消防措施丙烷屬於易燃氣體。與空氣混合能形成爆炸性混合物,遇熱源和明火有燃燒爆炸的危險。與氧化劑接觸猛烈反應。氣體比空氣重,能在較低處擴散到相當遠的地方,遇火源會著火回燃,產生一氧化碳、二氧化碳等有害氣體。遇到丙烷燃燒的情況時要立刻切斷氣源。若不能切斷氣源,則不允許熄滅泄漏處的火焰。噴水冷卻容器,可能的話將容器從火場移至空曠處。
泄漏應急處理迅速撤離泄漏污染區人員至上風處,並進行隔離,嚴格限制出入。切斷火源。建議應急處理人員戴自給正壓式呼吸器,穿防靜電工作服。儘可能切斷泄漏源。用工業覆蓋層或吸附/吸收劑蓋住泄漏點附近的下水道等地方,防止氣體進入。合理通風,加速擴散。噴霧狀水稀釋、溶解。構築圍堤或挖坑收容產生的大量廢水。如有可能,將漏出氣用排風機送至空曠地方或裝設適當噴頭燒掉。漏氣容器要妥善處理,修復、檢驗後再用。
安全術語
R12極度易燃。S9保持容器置於良好通風處。
S16遠離火源。
存儲和運輸
 液化石油氣運輸車
液化石油氣運輸車需要設定卸車泵或壓縮機,有的罐車自帶卸車泵。最好設定汽化器,應根據用戶要求確定。簡易的話,如果用量不大、壓力要求不高、管道長度適中,可介質借用儲罐內壓力將丙烷壓入管道自然汽化,但需做好管道選材、防凍傷防護等。
有條件用氮氣加壓卸車,沒條件就壓縮機,或者泵卸車。罐車沒有自帶空溫加壓器。必須考慮設定空溫式氣化器氣化或者升溫。