反應機理
首先,丙二酸二乙酯在乙醇鈉的作用下,脫去α氫,得到碳負離子:
CH(COOEt) + CHONa → CHOH + NaCH(COOEt)
該反套用乙醇作溶劑。先將鈉溶於乙醇,然後加入丙二酸二乙酯,加熱沸騰幾分鐘即可。
NaCH(COOEt)為強親核劑,能與鹵代烴反應,得到烴基取代的丙二酸二乙酯:
R-Br + NaCH(COOEt) → NaBr↓ + R-CH(COOEt)生成的NaBr難溶於乙醇,所以能觀察到析出白色沉澱。這是一個SN2反應,伯鹵代烴和烯丙型鹵代烴能得到較高產率,仲鹵代烴產率低,最好不用;叔鹵代烴和鹵代乙烯型的鹵代烴不能順利反應。
R-CH(COOEt)用氫氧化鈉溶液水解,然後酸化,並加熱脫羧,就得到羧酸:
R-CH(COOEt) + 2NaOH → R-CH(COONa) + 2EtOH
R-CH(COONa) + 2HCl → R-CH(COOH) + 2NaCl
R-CH(COOH) → R-CH-COOH + CO↑(反應條件為加熱)容易看出,用丙二酸酯合成法能得到比原來的鹵代烴多兩個碳的羧酸。
此外,烴基取代的丙二酸酯R-CH(COOEt)仍然含有一個活潑α氫,尚可進一步烷基化:
R-CH(COOEt) + CHONa → R-CNa(COOEt) + CHOH
R-CNa(COOEt) + R’-Br → RR’C(COOEt) + NaBr↓
RR’C(COOEt)用氫氧化鈉溶液水解,然後酸化,並加熱脫羧,就得到兩個烷基取代的乙酸。
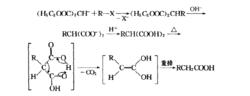 反應機理
反應機理套用
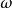 Malonic ester合成
Malonic ester合成丙二酸酯在強鹼存在下,可與多種含有活潑鹵原子的化合物(如鹵代烴及其衍生物、α,-二鹵化物、碘和醯鹵等)發生取代反應,生成取代的丙二酸酯、環狀化合物、多元羧酸及羰基酸等。在相轉移催化劑存在下, 可用弱鹼鹼代替強鹼製備取代丙二酸酯。
 合成套用
合成套用
