原子吸收分光光度法
原理
樣品經消化後,導入原子吸收分光光度計中,經火焰原子化後,吸收波長213.8nm的共振線,其吸收量與鋅含量成正比,與標準曲線比較定量。
試劑
(1)混合酸:硝酸:高氯酸=5:1;0.9%鹽酸。
(2)鋅標準貯備液:精確稱取0.500g金屬鋅(純度>99.99%)或者含0.0500g鋅相對應的氧化物,加適量鹽酸使之溶解,移入1000mL容量瓶中,用0.9%鹽酸定容至刻度,儲存於聚乙烯瓶內,置冰櫃保存。此溶液每毫升相當於500ug鋅。
(3)鋅標準使用液:
①標準使用液配製:吸取鋅標準儲備液10.0mL置於50mL容量瓶中,用0.9%鹽酸溶液定容至刻度,該溶液每毫升相當於100ug鋅。
②標準曲線製備:
吸取0.00、0.20、0.40、0.60、3.0、0.80mL的鋅標準使用液,分別置於50mL容量瓶中,以0.9%鹽酸稀釋定容至刻度,搖勻。此標準系列含鋅分別為0.00、0.4、0.8、1.2、1.6ug。
儀器
(1)原子吸收分光光度計。
(2)儀器條件:波長213.8nm,燈電流、狹縫、空氣乙炔流量及燈頭高度均按儀器說明書調至最佳狀態。
操作步驟
1.樣品濕法消化
固體樣品:精確稱取代表性樣品適量(按樣品含鈣量確定,如乾樣1.0g,濕樣3.0g,液體樣品5-10g)於150mL三角燒瓶中,加入混合酸10-15mL,蓋一玻片放置過夜。次日於電熱板上逐漸升溫加熱,溶液變成棕紅色,應注意防止炭化,如發現消化液顏色變深,再滴加濃硝酸,繼續加熱消化至冒白色煙霧,取下放冷後加入約10mL水繼續加熱消化至冒白煙為止。放冷後用0.9%鹽酸洗入50mL的刻度試管中,同時做試劑空白。
2.樣品乾法灰化
稱取製備好的代表性樣品5.0-10.0g置於瓷坩堝中,於電爐上小火炭化至無煙後移入馬弗爐中,500℃灰化約8h後取出,放冷後再加入少量混合酸,小火加熱至無炭粒,待坩堝稍涼,加20mL 0.9%鹽酸,溶解殘渣並移入50mL的容量瓶中,再用 0.9%鹽酸反覆洗滌坩堝,洗液併入容量瓶中,並稀釋至刻度,混勻備用。
3.樣品測定
將試劑空白液、處理好的樣品溶液和鋅標準溶液分別導入火焰原子化器進行測定。記錄其對應的吸光度,與標準曲線比較定量。
結果計算
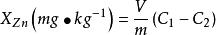 食品中鋅的測定
食品中鋅的測定式中:C為樣品液中鋅的含量(ug/mL);
C為試劑空白液中鋅的含量(ug/mL);
V為樣品處理液中總體積(mL);
m為樣品質量(g)。
允許偏差
相對標準偏差小於5%。
二硫腙比色法
原理
樣品經消化後,在pH4.5~5.0時,鋅離子與二硫腙形成紫紅色絡合物, 溶於四氯化碳,加入硫代硫酸鈉,防止銅、汞、鉛、鉍、銀和鎘等離子的干擾,與標準系列比較定量。
試劑
1.乙酸鈉溶液(2moL/L):稱取68g乙酸鈉(CHCOONa·3HO),加水溶解後稀釋至250mL。
2.乙酸(2moL/L):量取10.0mL冰乙酸,加水稀釋至85mL。
3.乙酸-乙酸鹽緩衝溶液:乙酸鈉溶液(2moL/L)與乙酸(2moL/L)等體積混合,此溶液pH為4.7左右。用二硫腙-四氯化碳溶液(0.1g/L)提取數次,每次10mL,除去其中的鋅,至四氯化碳層綠色不變為止,棄去四氯化碳層,再用四氯化碳提取乙酸-乙酸鹽緩衝液中過剩的二硫腙,至四氯化碳層無色,棄去四氯化碳層。
4.1:1氨水。
5.鹽酸(2moL/L):量取10mL鹽酸,加水稀釋至60mL。
6.鹽酸(0.02moL/L):吸取1mL鹽酸(2moL/L),加水稀釋至100mL。
7.鹽酸羥胺溶液(200g/L):稱取20g鹽酸羥胺,加60mL水,滴加1:1氨水,調節pH至4.0-5.5,以下按試劑3中用二硫腙-四氯化碳溶液(0.1g/L)處理。
8.硫代硫酸鈉溶液(250g/L):用乙酸(2moL/L)調節pH至4.0-5.5。以下按試劑3中用二硫腙-四氯化碳溶液(0.1g/L)處理。
9. 二硫腙-四氯化碳溶液(0.1g/L)。
10.二硫腙使用液:吸取1.0mL的二硫腙-四氯化碳溶液(0.1g/L),加四氯化碳至10.0mL,混勻。用1cm比色杯,以四氯化碳調節零點,于波長530nm處測吸光度(A),用下式計算出配製100mL的二硫腙使用液(57%透光率)所需0.01%二硫腙-四氯化碳溶液(0.1g/L)毫升數(V)。
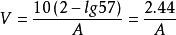 食品中鋅的測定
食品中鋅的測定11.鋅標準溶液:準確稱取0.1000g鋅,加10mL鹽酸(2moL/L),溶解後移入1000mL容量瓶中,加水稀釋至刻度。此溶液每毫升相當於100μg。
12.鋅標準使用液:吸取1.0mL鋅標準溶液,置於100mL的容量瓶中,加1mL鹽酸(2moL/L),以水稀釋至刻度,此溶液每毫升相當於1。0ug鋅。
13.酚紅指示劑(1g/L):稱取0.1g酚紅,用乙醇溶解至100mL。
儀器
分光光度計。
操作步驟
1.樣品消化
(1)硝酸高氯酸-硫酸法:
①糧食、冬粉、粉條、豆乾製品、糕點、茶葉等及其他含水分少的固體樣品:稱取粉碎樣品5.0 g或10.0g,置於250-500 mL凱氏燒瓶中,先加少量水使潤濕,加數粒玻璃珠,加硝酸-高氯酸混合液10~15 mL,放置片刻,以小火緩慢加熱,待作用緩和後,放冷。沿瓶壁加人5mL或10mL硫酸,再加熱,當瓶中液體開始變成棕色時,不斷沿瓶壁滴加硝酸-高氯酸混合液,直至有機物分解完全。加大火力,至產生白煙,待瓶口白煙冒淨後,瓶內液體再產生白煙為消化完全,該溶液應澄清無色或微帶黃色,放冷。在操作過程中注意防止爆沸或爆炸。 加入20 mL水煮沸,除去殘餘的硝酸至產生白煙為止,如此處理2次,冷卻後轉入50mL或100 mL容量瓶中,用水洗滌凱氏燒瓶,洗液並人容量瓶中,放冷,加水至刻度,混勻。定容後的溶液每10mL相當於1g樣品,相當加入硫酸量1mL。取與消化樣品相同量的硝酸-高氯酸混合液和硫酸,按同一方法做試劑空白試驗。
②蔬菜、水果:稱取25.0 g或50.0g洗淨打成勻漿的樣品,置於250-500 mL凱氏燒瓶中,加數粒玻璃珠,加硝酸-高氯酸混合液10-15 mL,以下按①中自“放置片刻”起依次操作。但定容後的溶液每10mL相當於5g樣品,相當加入硫酸1mL。
③醬、醋、冷飲、豆腐、醬醃菜等:稱取10.0 g或20.0g樣品(或吸取10.0mL或20.0gmL液體樣品),置於250-500 mL凱氏燒瓶中,加數粒玻璃珠,加硝酸-高氯酸混合液5-15 mL,以下按①中自“放置片刻”起依次操作。但定容後的溶液每10mL相當於2g或2mL樣品。
④含乙醇飲料或含二氧化碳飲料:吸取10.0mL或20.0mL樣品,置於250-500 mL凱氏燒瓶中,加數粒玻璃珠,先用小火加熱除去乙醇或二氧化碳,再加硝酸-高氯酸混合液5-10 mL,混勻,以下按①中自“放置片刻”起依次操作。定容後的溶液每10mL相當於2mL樣品。吸取5-10L水代替樣品,加與消化樣品相同量的硝酸-高氯酸混合液和硫酸,按同一方法做試劑空白試驗。
⑤含糖量高的樣品:稱取樣品5.0g或10.0g置於250-500 mL凱氏燒瓶中,先加少量水使潤濕,加數粒玻璃珠,加硝酸-高氯酸混合液5-10mL,搖勻。緩緩加入5 mL或10 mL硫酸,待作用緩和停止泡沫後,先用小火緩慢加熱(糖分易炭化),不斷沿瓶壁補加硝酸-高氯酸混合液,待泡沫完全消失後,再加大火力,直至有機物分解完全,濃白煙冒出、溶液澄清無色或微帶黃色為止,放冷。以下按①中自“放置片刻”起依次操作。
⑥水產品:取可食部分樣品搗成勻漿,稱取樣品5.0g或10.0g(海產藻類、貝類可適當減少取樣量),置於250-500 mL凱氏燒瓶中,加數粒玻璃珠,加硝酸-高氯酸混合液5-10 mL搖勻,以下按①中自“沿瓶壁加入5 mL或l0 mL硫酸”起依次操作。
(2)硝酸-硫酸法:以硝酸代替硝酸-高氯酸混合液進行操作。
2.樣品測定
(1)提取液製備
準確吸取5-10mL定容的消化液和相同量的試劑空白液。分別置於125mL分液漏斗中,加水5mL、0.5mL鹽酸羥胺溶液(200g/L),搖勻,再加2滴酚紅指示劑,用氨水(1+1)調節至紅色,再多加2滴,再加5mL二硫腙-四氯化碳溶液(0.1g/L),劇烈振搖2min,靜置分層。將四氯化碳層移至另一漏斗中,水層用少量二硫腙-四氯化碳溶液振搖提取,每次2-3mL,只是二硫腙-四氯化碳溶液綠色不變為止。合併提取液,用5mL水洗滌,四氯化碳層用鹽酸(0.02mol/L)提取2次,每次10mL,提取時劇烈振搖2min,合併鹽酸(0.02mol/L)提取提取液,並用少量四氯化碳洗去殘留的二硫腙。
(2)標準曲線製備及測定
吸取0.0、1.0、2.0、3.0、4.0、5.0ml鋅標準使用液(相當於0.0、1.0、2.0、3.0、4.0、5.0ug鋅),分別置於125mL分液漏斗中,各加入鹽酸(0.02mol/L)至20ml。於樣品提取液、試劑空白提取液及鋅標準溶液各分液漏斗中加入10ml乙酸-乙酸鹽緩衝液、1m1硫代硫酸鈉溶液(250g/L),搖勻,再各加入10.0ml二硫腙使用液,劇烈振搖2min。靜置分層後,四氯化碳層經脫脂棉濾入1cm比色杯中,以四氯化碳調節零點,于波長530nm處測定吸光度,標準各點吸光度減去零管吸光度後繪製標準曲線,或計算直線回歸方程,烊也吸收值與曲線比較或帶入方程求得含量。
結果計算
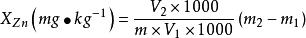 食品中鋅的測定
食品中鋅的測定式中:X為樣品中鋅的含量(mg/kg或mg/L);
m為測定用樣品消化液中鋅的質量(ug);
m為試劑空白液中鋅的質量(ug);
m為樣品質量(體積)(g或mL);
V為樣品消化液的總體積(mL);
V測定用消化液的體積(mL)。
允許偏差
相對標準偏差≤10%

