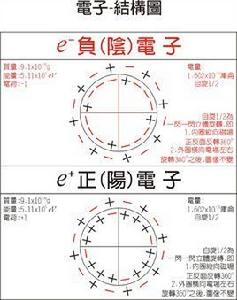
電子分布
由於電子高速運動,當他運動起來就感覺是一層一層的,可以說是電子層,也就是電子的分層分布.在多電子的原子裡,根據電子的能量的差異和通常運動區域離核的遠近不同,將核外電子分成不同的電子層。通過對許多種元素的電離能分析,人們發現,電子可以分成能量相近的若干組電子,每一個電子組即為一個電子層。依據能量由低到高,電子離核由近及遠,依次稱為1、2、3、……電子層,分別用符號K、L、M、N、O、P等表示。電子層又叫能層。電子層不能理解為電子在核外一薄層空間內運動,而是按電子出現幾率最大的區域,離核遠近來劃分的。
電子層的數量就被稱為電子層數。
套用
可用於原子半徑的比較。對於單個原子來說,原子核外電子層數越多,原子半徑越大;對於原子核外電子層數相同,最外層電子數越多,原子半徑越小。