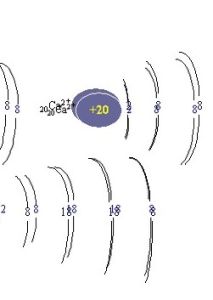
簡介
如果是主族元素,則族數=最外層電子數(He除外)最外層電子數少於3個,如鹼金屬、鹼土金屬元素,容易失去最外層電子,達到最外層8個電子的穩定結構,使得它有很強金屬性與還原性。
最外層電子數多於5個,如鹵族、氧族元素,容易得到電子達到最外層8個電子的穩定結構,使得它有很強非金屬性與氧化性。
當原子電子層最外層電子為3或5時,如氮族、硼族,既不易失去最外層電子,又不易得到電子,所以與別的原子化合困難。
當原子電子層最外層電子為4時,如碳族,既易失去最外層電子,又易得到電子,所以與別的原子以共價鍵化合。
當原子電子層最外層電子為8時,如稀有氣體,已經達到穩定結構,所以幾乎不與別的元素化合。