成份
 釓塞酸二鈉注射液
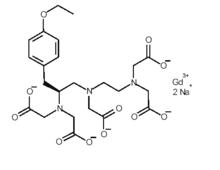
釓塞酸二鈉注射液本品主要成份為:釓塞酸二鈉
化學名稱為:(4S)-4-(4-乙氧苯基)-3,6,9-三(羧甲基)-3,6,9-三氮雜十一烷二酸,釓螯合物,二鈉鹽。
化學結構式為:
 釓塞酸二鈉注射液
釓塞酸二鈉注射液分子式:CHNOGd·2Na
輔料:卡洛酸三鈉、氨丁三醇、鹽酸、氫氧化鈉、注射用水。
性狀
本品為無色至微黃色的澄明液體。
適應症
用於診斷,僅供靜脈內給藥。
釓塞酸二鈉注射液用於檢測肝臟局灶性病變,在T1加權磁共振成像中提供病灶特徵信息。
規格
10ml預裝玻璃注射器,每1ml中含釓塞酸二鈉181.43mg
用法用量
釓塞酸二鈉注射液是一種即用型水溶液,無需稀釋,通過大孔的注射針頭或留置管(推薦用18-20G)靜脈團注給藥,注射速率約為1-2ml/秒。對比劑注射完畢後應使用生理鹽水沖洗靜脈內插管。
釓塞酸二鈉注射液的推薦劑量為:
·成人:0.1ml/kg體重釓塞酸二鈉注射液(相當於25μmol/kg體重)。
·新生兒、嬰兒、兒童及青少年:對18歲以下患者尚無臨床使用經驗。
·年齡大於等於65歲的患者:無需調整劑量。
·腎損害的患者:無需調整劑量,但是對於嚴重腎損害的患者需要謹慎使用(參見“注意事項”下相應內容)。
·肝損害的患者:無需調整劑量。
·重複使用:目前尚無有關重複使用本品的臨床資料。
不良反應
 釓塞酸二鈉注射液
釓塞酸二鈉注射液未發現任何不良反應的發生率高於”不常見“。
根據臨床試驗數據得出的不良反應發生率:
在超過1700名患者的使用經驗中,由研究者觀察並判斷的藥物相關性不良反應如下所述。
絕大多數不良反應為輕到中度。
下表列出了根據MedDRA系統器官分類(MedDRA SOCs)報告的不良反應。
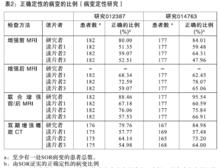 釓塞酸二鈉注射液
釓塞酸二鈉注射液在非常罕見的病例中可能會出現嚴重程度達到休克的過敏樣反應。
使用本品後,在少於1%的患者中觀察到血清鐵和膽紅素水平輕度升高,但均在1-4天內回復到其原值,且無任何臨床症狀。
來自上市後自發性報告的其他不良反應:
心臟異常、神經系統異常:
在罕見的病例報告了心動過速和不安。
由於這些不良反應來自自發性報告的數據,因此無法計算其發生率。但是由於在臨床試驗超過1700名患者中未觀察到這些不良反應,因此他們的發生應屬罕見(<1/1000)。
禁忌
對本品活性成份或相關任何輔料過敏的患者禁用。
注意事項
對駕駛和機械操作能力的影響
未知。
不相容性
在未作相容性研究的情況下,本品不得與其他藥品混合。
使用/操作說明
·檢查
本品為即用型的無色至微黃色的澄明液體。
在本品嚴重變色、出現微粒物質或容器破損時均不應使用。
預裝注射器
預裝注射器在使用前方可從包裝中取出,並應立即準備注射。
頂帽打開後應立即使用。
一次檢查後未用完的溶液必須丟棄。
特別警告和注意事項
必須遵守磁共振檢查的常規安全規範,如禁用於帶有心臟起搏器和鐵磁性植入體的患者。
噁心和嘔吐是已知的對比劑使用可能出現的不良反應,因此患者在檢查前2小時內應禁食,以降低嘔吐和誤吸的風險。
注射對比劑時,患者應儘可能平臥。患者注射完畢後應觀察至少30分鐘,因為經驗表明大部分不良反應都發生在這段時間內。
·過敏
與其他靜脈內注射對比劑一樣,使用本品可能導致類過敏反應/超敏反應或其他特異質反應,以心血管、呼吸以及皮膚表現為特徵,程度可以嚴重到甚至休克。
對任何過敏原具有過敏/過敏樣反應史的患者以及患有支氣管哮喘的患者發生嚴重反應的風險可能更高。這些反應大多發生在對比劑注射後半小時內。但在罕見病例中可能在數小時至數日後發生遲發反應。與其他對比增強診斷過程一樣,建議操作結束後對患者進行觀察。準備好針對過敏反應的治療藥物和急救措施是必要的。
在下列情況下發生過敏反應的風險較高:
-有對比劑過敏史
-有支氣管哮喘病史
-有過敏性疾病史
正在使用β受體阻滯劑的患者對套用β受體激動劑治療過敏反應會有影響。
·心血管疾病
由於目前獲得數據有限,因此在有嚴重心血管疾病的患者中使用本品時應謹慎。
·腎功能損害
曾有報導,在以下病人中使用某些含釓對比劑與腎源性系統纖維化(NSF)的發生有關:
-嚴重的急性或慢性腎功能損傷(腎小球濾過率(GFR)<30ml/min/1.73m)或
-由於肝腎綜合徵引起的或在肝移植手術期間出現的任何程度的急性腎功能不全
腎源性系統纖維化是一種以損害皮膚、肌肉和內臟器官為特徵的,影響生命功能,有時也致命的進行性疾病,主要導致皮膚和內臟器官中的結締組織增生,使得皮膚變厚、粗糙和僵硬,有時導致致殘性攣縮。雖然在本品的診斷劑量下,釓在全身的暴露量很低,同時本品具有雙重清除途徑(包括腎臟和肝膽系統),但在使用本品時仍有發生NSF的可能性,因此本品應避免用於急、慢性嚴重腎功能損傷(GFR<30ml/min/1.73m)和由於肝腎綜合徵導致的各種程度的劑型腎功能不全的患者,除非該診斷信息是必需的,且不能通過非對比增強MRI獲得。肝移植手術前後的患者需基於上述考慮,經過慎重的風險/收益評估後才可使用本品。
中度腎功能損傷(CGR 30-59ml/min/1.73m)發生腎源性系統纖維化的風險還不確定。因此本品用於這類病人時要加以警惕。當基於一種釓類對比劑時,不應超過推薦劑量並且在再次給藥前留出足夠時間使藥物從體內清除。
所有患者在使用本品前都應手機病史和/或進行實驗室檢查,以了解腎功能不全的情況。本品可通過血液透析從體內清除。對於套用本品時已經接受血液透析的患者,可考慮在注射本品後短時間內進行血液透析,以加強對比劑的清除。但是對於那些未正在進行血液透析的患者,沒有證據支持開始血液透析可以預防或治療NSF。
·局部耐受性
肌肉注射本品可能導致局部不耐受反應,包括局灶性壞死,故應嚴格避免肌肉注射。(見“藥理毒理”)
孕婦及哺乳期婦女用藥
·妊娠
目前尚無本品套用於妊娠患者的經驗。動物實驗未顯示使用釓塞酸二鈉存在致畸風險,或對胎仔出生前後的發育有影響,但在妊娠家兔試驗中重複給藥劑量相當於臨床常規劑量的26倍(按體表面積計算)時出現胚胎毒性(參見毒理研究)。因此,對於妊娠期婦女,必須在進行仔細的收益-風險權衡後方可使用本品。
·哺乳
目前尚不了解本品是否經人類乳汁分泌,臨床前實驗詩句顯示極少量的釓塞酸二鈉(低於給藥劑量的0.5%)可經母體血液進入乳汁中。對於哺乳期婦女,必須在進行仔細的收益-風險權衡狗方可使用本品。
兒童用藥
對18歲以下患者尚無臨床使用經驗。
老年用藥
對老年患者的使用沒有特殊限制。
藥物相互作用
主要經膽汁排泄的陰離子類藥物(如利福平)可能會競爭性影響本品的肝臟對比增強和膽道排泄。動物實驗表明利福平類的化合物會影響肝臟對本品的攝取,從而降低本品在肝臟的對比增強效果。在這種情況下,本品的診斷效果可能會受到限制。目前尚無數據表明本品與其他藥物與的香菇作用。
·患者膽紅素或鐵蛋白水平升高造成的干擾
膽紅素或者鐵蛋白水平升高會降低本品在肝臟的對比增強效果。
·對診斷檢查的干擾
在使用本品檢查後24小時內,採用絡合滴定法(例如二價鐵絡合法)進行血清鐵測定可能導致結果不準確,這是因為在對比劑溶液中存在的游離的絡合劑。
藥物過量
在磁共振成像中測試過的最大使用劑量0.4ml/kg體重(100μmol/kg)可以很好耐受。在臨床試驗中,數量有限的患者使用2.0ml/kg體重(500μmol/kg)的劑量,不良反應的發生率增加,但並無新的不良反應出現。
考慮到本品體積小(最大10ml)、胃腸道吸收率極低,以及本品的急性毒性數據,基本不可能發生由於誤食對比劑引起的中毒。
具有嚴重腎和肝功能損害的患者由於疏忽導致藥物過量時,可通過血液透析清除本品。
臨床試驗
 釓塞酸二鈉注射液
釓塞酸二鈉注射液釓塞酸二鈉注射液共進行了6項關鍵性/確證性Ⅲ期臨床研究,其中歐洲2項、美國2項、日本和中國各1項。在這6項關鍵性/確證性Ⅲ期臨床研究中,共招募了1228名患者。
歐洲和美國進行的關鍵性研究:
在歐洲(2項)和美國(2項)進行的4項關鍵性Ⅲ期臨床研究中,共入組了797名已知/疑似患有肝臟局灶性病變的患者,其中621名患者接受了釓塞酸二鈉注射液,劑量為0.025mmol/kg,對這些患者進行了有效性評價。在這621名患者中,334名(54%)為男性,287名(46%)為女性;平均年齡為57歲(範圍為19至84歲)。種族分布為:556名(90%)高加索人,22名(4%)黑人,21名(3%)西班牙人,15名(2%)亞洲人,7名(1%)為其他種族。
研究目的:
·釓塞酸二鈉注射液增強MRI與增強前MRI相比,對肝臟病變檢出的嗎,敏感性(2項對照研究)。參照標準(SOR)是結合手術切除肝臟組織的病理學檢查與術中超聲對全肝病變的檢查的綜合診斷。研究還建立了一套病灶跟蹤程式,對研究中磁共振成像中檢測到的病變與參照標準(SOR)中的病變進行比對。
·釓塞酸二鈉注射液增強MRI與增強前MRI相比,正確定性的肝臟病變的比例(2項對照研究)。參照標準(SOR)包括預先設定的檢查程式,如:對惡性病變的組織病理學檢查,對某些良性病變的特定影像學檢查。
患者入選後,進行預先設定的SOR檢查以及肝臟MRI檢查,包括了增強前(平掃)MRI以及0.025mmol/kg釓塞酸二鈉注射液增強後的MRI檢查,包括動態期和肝細胞期(注射後20分鐘)掃描。在每一項研究中,均由研究者以及由3名未參與過研究的放射學專家獨立對平掃MR圖像和釓塞酸二鈉注射液增強MR圖像進行盲法讀片。對於病變檢出性研究,還有另外一名獨立的放射學專家完成病變跟蹤過程。只有當SOR和研究中的MRI檢測到的病變位於同一肝段內的相同部位中時,該病變才被判定為正確檢出的病變,並進行敏感性分析。
在這4項研究中,與平掃MRI相比,釓塞酸二鈉注射液增強(包括聯合增強前/後圖像集成或者增強後圖像集)顯著提高了診斷效能。另外,該4項研究中均將釓塞酸二鈉注射液增強MRI與螺旋CT進行了比較,結果表明釓塞酸二鈉注射液增強MRI的總體表現優於螺旋CT(參見表1和表2)。
 釓塞酸二鈉注射液
釓塞酸二鈉注射液 釓塞酸二鈉注射液
釓塞酸二鈉注射液 釓塞酸二鈉注射液
釓塞酸二鈉注射液在兩項病變檢出研究中,如果綜合考慮病變的檢出和定性,所有讀片者的評估結果均顯示釓塞酸二鈉注射液增強MRI(包括聯合增強前/後圖像集或者增強後圖像集)與平掃MRI相比,正確檢出和定性的病變比例均增加。另外,釓塞酸二鈉注射液增強MR檢查也優於CT檢查。
在兩項病變定性的研究中,多數讀片者的評估結果均顯示,釓塞酸二鈉注射液增強MRI(包括聯合增強前/後圖像集或者增強後圖像集)與平掃MRI相比,對於肝轉移瘤、血管瘤、局灶性結節增生(FNH)以及肝囊腫的定性敏感性增加;對於肝細胞癌(HCC),6名盲法讀片者中有3名評估為對病變的定性敏感性增加。該研究結果同樣顯示釓塞酸注射液增強MRI優於CT。
日本進行的確證性研究:
該研究是在日本患者中進行的一項多中心、開放、單劑量用藥研究。研究目的是在已知/疑有惡性肝臟病變的成年患者中,評價釓塞酸二鈉注射液的診斷有效性和安全性。研究共招募了178名患者。
對於病變檢出,聯合增強前/後MRI比螺旋CT正確檢出更多的病變,由研究者評估正確檢出的病變增加了6%,而盲法讀片評估則增加了2-9%。對於多數盲法讀片者(3名盲法讀片者中的2名)以及平均讀片結果,這種優勢具有統計學意義(參見表3)。另外,根據研究者、3名盲法讀片者以及平均讀片評估,聯合增強前/後MRI在病變的檢出方面均優於增強前MRI,而且均具有統計學意義。
 釓塞酸二鈉注射液
釓塞酸二鈉注射液對於病變定性,所有盲法讀片者的評估均顯示聯合增強前/後MRI正確定性的病變的比率高於螺旋CT。所有盲法讀片者和平均負片的評估均顯示聯合增強前/後MRI非劣效於螺旋CT,且均具有統計學意義。另外,所有盲法讀片者和研究者的評估均顯示,聯合增強前/後MRI與增強前MRI相比,正確定性的病變比例增加,其優勢均具有統計學意義。
中國進行的臨床研究:
這是一項在中國進行的多中心、開放、單劑量給藥(25μmol/kg體重)的研究,採用盲法讀片(3名盲法讀片者)進行影像學評估,在已知/疑有肝臟局灶性病變的成年患者中評價釓塞酸二鈉注射液對於肝臟局灶性病變的診斷有效性。這項臨床研究還評價了釓塞酸二鈉注射液的安全性。
該研究的主要有效性變數是增強後MRI與增強前(平掃)MRI相比對肝臟病變檢出的敏感性,所有的肝臟病變均與參照標準(即,手術病例結合術中超聲、數字減影血管造影結合多層螺旋CT以及超聲檢查結合多層螺旋CT)進行比對予以證實。
該研究招募了247名患者,其中234名患者接受了釓塞酸二鈉注射液。在符合方案人群(PPS)中,所有盲法讀片者和平均讀片的評估結果均顯示,釓塞酸二鈉注射液增強MRI對病變檢出的敏感性(主要有效性變數)高於平掃MRI,兩者敏感性的差異分別為9.46pp(百分點)(平均讀片)、8.65pp(讀片者1)、12.23pp(讀片者2)和7.50pp(讀片者3),差異均有統計學顯著性(參見表4)。在全分析人群(FAS)中,所有盲法讀片者和平均讀片的評估結果也證實了釓塞酸二鈉注射液增強MRI對病變檢出的敏感性高於平掃MRI,差異均有統計學顯著性。研究者評估的結果與盲法讀片的評估結果一致,同樣也有統計學意義。
所有盲法讀片者和平均讀片的評估均顯示,聯合增強前/後MRI評估對病變定性的準確度(次要有效性變數)高於平掃MRI。在PPS人群中,兩者對良性病變診斷準確度差值分別為13.69pp(平均讀片者)、15.18pp(讀片者1)和17.86pp(讀片者3),差異有統計學意義。在PPS人群中,兩者對惡性病變診斷準確度的差異分別為8.95pp(讀片者平均)、12.04pp(讀片者1)和11.11pp(讀片者2),差異有統計學意義。在FAS人群中得到的結果類似,也有統計學意義。研究者評估顯示聯合增強前/後MRI對良/惡性病變分類準確度高於增強前MRI,差異也有統計學意義。
該研究中沒有報告死亡事件、嚴重不良事件(SAE)或導致患者退出的不良事件(AE)。在安全分析人群中,有8.5%的患者(20/234名)報告過至少1例不良事件,不良事件的總數為24例。234名患者中,共有2.1%(5名)報告了5例與研究藥物有關的不良事件。除了2例噁心和1例注射部位疼痛外,所有的不良事件均為實驗室檢查異常或血壓升高/降低。研究者評價所有不良事件的嚴重程度為輕度(17例)或者中度(7例)。研究藥物相關的不良事件包括噁心(2例)、血清膽紅素升高(2例)和白細胞減少(1例)。
其他支持性研究:
除上述6項關鍵性/確證性研究外,在歐洲還進行了一項隨機、平行、對照的Ⅲ期臨床研究,目的是在已知或疑有肝臟局灶性病變的患者中比較釓塞酸二鈉注射液與釓貝葡胺對肝實質的增強效果。這項研究中,嘎斯塞酸二鈉注射液包括了146名患者,對照組(釓貝葡胺)包括了149名患者。主要分析結果顯示釓塞酸二鈉和釓貝葡胺注射後對肝實質的增強(T1加權像)分別為54.2%和32.7%,釓塞酸二鈉注射液由於釓貝葡胺,且有統計學意義。
藥理毒理
 釓塞酸二鈉注射液
釓塞酸二鈉注射液藥理作用
藥物治療分類:順磁性對比劑,ATC代碼:V08 C A10
本品時用於磁共振成像的順磁性對比劑。其對比增強作用是由穩定的含釓複合物,Gd-EOB-DTPA(釓塞酸二鈉)介導的。在0.47T、pH值為7、溫度為39℃的條件下的順磁效應即弛豫率(取決於對血漿中質子的自旋-晶格弛豫時間的影響)大約為8.7L/mmol/秒,並且與磁場強度只有很小的相關性。在T1加權掃描時,釓離子誘導處於激發態的原子核,使其自旋-晶格弛豫時間縮短,導致信號強度增加,進而導致某些組織的圖像對比增強。
EOB-DTPA和順磁性的釓離子形成一種穩定化合物,具有極高的熱力學穩定性(log K=-23.46)。Gd-EOB-DTPA是一種高度水溶性的親水化合物,同時由於含有乙氧基苯甲基而具有一定親脂性。該化合物僅表現出輕度的蛋白結合。
即用型釓塞酸二鈉溶液的理化性質如下:
成像
對成像的視覺評估顯示在所有劑量的所有時間點,肝的造影增強都是同質的。對於GRE序列,在注射後的前2分鐘信號強度急劇增加(以標準品為參照其變化的平均值為0.3-0.86),然後是一個緩慢的增加(以標準品為參照其變化的平均值為0.2-0.4),直到注射後20分鐘,接著在10μmol/kg體重劑量組有持續90分鐘的平台期,在25和50μmol/kg體重的劑量組有持續2小時平台期。在10到50μmol/kg體重劑量範圍內,信號呈劑量依賴性增加。從50到100μmol/kg體重劑量沒有觀察到信號的增加。
團注本品後,在包括動脈期、門靜脈期及平衡期的動態期成像中,不同肝臟病變在各時間點表現為不同的增強特徵,據此進行病變的分類(良性/惡性)和定性。本品可以進一步改善多血管的肝臟病灶的顯影。
延遲期(肝細胞期)可在注射後大約10分鐘(再確證性研究中大多數數據在注射後20分鐘獲得)進行掃描,成像的時間窗可持續至少120分鐘。在需要血液透析以及膽紅素值升高(>3mg/dl)的患者,成像時間窗縮短到60分鐘。
肝細胞期內肝實質的增強有助於確定肝臟病變的數量、葉段分布、病灶顯示及邊界顯影,從而提高了病灶的檢出。肝臟病灶的不通話增強/洗脫模式有助於動態期成像信息的判斷。
釓塞酸二鈉注射液的肝臟排泄導致單管結構的增強。
毒理研究
動物急性毒性、亞急性毒性研究和遺傳毒性研究結果未顯示本品用於診斷對人體有特殊危害。
·全身毒性
對於遙測的意識清醒的犬,給予最高劑量0.5mmol/kg(人體所用劑量的20倍)進行試驗時,曾觀察到較小的一過性的QT間期延長。在離體豚鼠乳頭肌中,高濃度的Gd-EOB-DTPA能阻滯HERG通道,延長動作電位時間。這意味著過量使用本品時可能會導致QT間期的延長。在給予小鼠本品劑量約1.1mmol/kg時,3隻小鼠中有1隻出現步態異常,異常發生於給要結束30分鐘後,在給藥結束4小時後消失。目前在其他系統器官的安全性藥理學研究中尚無異常發現。
·遺傳毒性、致癌性
在體外細菌回復突變試驗中,或人外周血淋巴細胞的染色體畸變試驗中,釓塞酸二鈉未顯示誘導突變作用。在靜脈注射4mmol/kg本品後,小鼠體內微核試驗結果為陰性。
由於本品遺傳毒性試驗陰性、對快速生長的組織無毒性作用,而且本品用於診斷目的,通常患者僅接受一次注射,因此認為不需要進行動物致癌性研究。
·生殖毒性
在大鼠和家兔中進行了生殖和發育毒性研究。在相當於人體推薦單次給藥劑量的32倍(按體表面積計算)時,釓塞酸二鈉用於器官形成期間的妊娠大鼠時沒有致畸作用,但在相當於人體劑量3.2倍(按體表面積計算)時觀察到著床後丟失、吸收率增加和窩仔數量降低。此時因動物本品每天重讀給藥,其在動物體內的總暴露量明顯高於人體常規劑量單次給藥達到的暴露量。給藥劑量為人體臨床劑量的6.5倍(按體表面積計算)時,本品不影響雄性和雌性大鼠的生育力和一般生殖行為。
·局部耐受性和潛在致癌性
局部耐受性實驗顯示本品血管內注射(靜脈內和動脈內)和靜脈旁註射給藥具有良好的耐受性。但肌肉注射給藥會引起局部不耐受反應,包括中度組織間隙出血、水腫和局部肌纖維壞死,因此在人體應該嚴格避免肌肉注射。
抗原和接觸-致敏研究未顯示本品有致敏性。
藥代動力學
·分布
靜脈注射後,本品快速擴散入細胞外間隙。對大鼠和狗靜脈注射Gd-EOB-DTPA7天后,在其體內僅測得低於1%的注射劑量,其中在腎臟和肝臟中的濃度最高。本品不能通過完整的血-腦屏障,僅有少量可擴散通過胎盤屏障。
·清除
在人體中,Gd-EOB-DTPA在血清中的有效半衰期為1.0±0.1小時,其餘注射劑量無顯著相關性,其終末半衰期為1.65±0.23小時或更少。在低於0.4ml/kg(100μmol/kg)的劑量下,藥代動力學呈劑量-線性特徵。Gd-EOB-DTPA以相同的例;量通過腎臟和肝膽途徑完全清除。
·患者的特性
在嚴重腎臟或肝膽損害的患者中,本品的清除方式發生相應的改變。在嚴重肝臟損害的患者中,血清半衰期輕度延長;而在嚴重腎臟損害(需要血液透析)的患者中,半衰期顯著延長。
貯藏
密閉保存。
包裝
10ml預裝注射器,1支/盒,5支/盒,10支/盒。
有效期
60個月
執行標準
JX20060140
