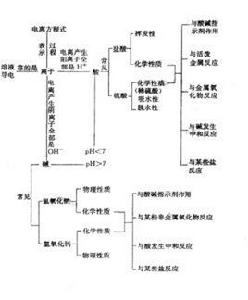
重點知識
與吸水性的區別
吸水性是一種物理性質,體現於物理變化(有的也是化學變化,如濃硫酸能吸收它的周圍的空氣中的水蒸氣,形成一系列的多水化合物,另一方面濃硫酸溶解於吸收的水中使自己變稀),如氫氧化鈉固體有強烈的吸濕性,只要幾分鐘,它就會因為吸收它周圍的水蒸氣,而溶解於吸收來的水中,變成氫氧化鈉的濃溶液。
脫水性
脫水性,脫水的過程是一種化學變化,此過程生成了新的物質,如濃硫酸能將有機物(包括木材,布匹,皮膚,糖類等)中的氫元素和氧元素按照2比1的比例(以水的形式)脫去,最後只剩下碳元素(有時還有其他元素,或氫元素和氧元素沒有脫完)(此過程稱為碳化)。
不慎接觸
物質在脫水過程中會放出大量熱.,不慎接觸到濃硫酸時套用大量水沖洗,最後塗上碳酸氫鈉溶液。【大量的冷水沖洗能夠有效的帶走反應放出的熱,因此直接用大量水沖洗快速有效(找到水就能操作)。倒是用布擦去的時候可能導致時間上的延誤,並且有擴大接觸面的危險(之前是一小點,一擦一大片)】
常見類型
濃硫酸 濃HSO
焦硫酸(又叫發煙硫酸) HSO
五氧化二磷PO
相關套用
乙醇→硫酸(濃)→乙烯+水,條件為170℃。CHOH==HSO/340K==CH+HO
該反應的實質是乙醇分子中1號C上的羥基和2號C上的氫原子發生了消去反應,脫水形成碳碳雙鍵。在這個反應中,濃硫酸既體現了催化劑的作用,又體現了脫水劑的作用(脫水性)。
1.乙醇→硫酸(濃)→乙烯+水,條件為170℃。CHOH==HSO/340K==CH+HO
2.該反應的實質是乙醇分子中1號C上的羥基和2號C上的氫原子發生了消去反應,脫水形成碳碳雙鍵。在這個反應中,濃硫酸既體現了催化劑的作用,又體現了脫水劑的作用(脫水性)。