簡介
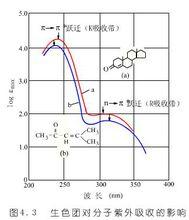 生色團對分子紫外吸收的影響
生色團對分子紫外吸收的影響分子的紫外可見吸收光譜法是基於分子內電子躍遷產生的吸收光譜進行分析的一種常用的光譜分析法。分子在紫外-可見區的吸收與其電子結構緊密相關。紫外光譜的研究對象大多是具有共軛雙鍵結構的分子。如,膽甾酮(a)與異亞丙基丙酮(b)分子結構差異很大,但兩者具有相似的紫外吸收峰。兩分子中相同的O=C-C=C共軛結構是產生紫外吸收的關鍵基團。
 紫外-可見光譜區域
紫外-可見光譜區域紫外-可見以及近紅外光譜區域的詳細劃分如圖4.4所示。紫外-可見光區一般用波長(nm)表示。其研究對象大多在200-380 nm的近紫外光區和/或380-780 nm的可見光區有吸收。紫外-可見吸收測定的靈敏度取決於產生光吸收分子的摩爾吸光係數。該法儀器設備簡單,套用十分廣泛。如醫院的常規化驗中,95%的定量分析都用紫外-可見分光光度法。在化學研究中,如平衡常數的測定、求算主-客體結合常數等都離不開紫外-可見吸收光譜。
基本原理
紫外可見吸收光譜的基本原理是利用在光的照射下待測樣品內部的電子躍遷,電子躍遷類型有:
(1)σ→σ* 躍遷 指處於成鍵軌道上的σ電子吸收光子後被激發躍遷到σ*反鍵軌道
(2)n→σ* 躍遷 指分子中處於非鍵軌道上的n電子吸收能量後向σ*反鍵軌道的躍遷
(3)π→π* 躍遷 指不飽和鍵中的π電子吸收光波能量後躍遷到π*反鍵軌道。
(4)n→π* 躍遷 指分子中處於非鍵軌道上的n電子吸收能量後向π*反鍵軌道的躍遷。
電子躍遷類型不同,實際躍遷需要的能量不同:
 電子躍遷所處的波長範圍
電子躍遷所處的波長範圍σ→σ* ~150nm
n→σ* ~200nm
π→π* ~200nm
n→π* ~300nm
吸收能量的次序為:σ→σ*>n→σ*≥π→π*>n→π*
特殊的結構就會有特殊的電子躍遷,對應著不同的能量(波長),反映在紫外可見吸收光譜圖上就有一定位置一定強度的吸收峰,根據吸收峰的位置和強度就可以推知待測樣品的結構信息。
特點
1、紫外可見吸收光譜所對應的電磁波長較短,能量大,它反映了分子中價電子能級躍遷情況。主要套用於共軛體系(共軛烯烴和不飽和羰基化合物)及芳香族化合物的分析。
2、由於電子能級改變的同時,往往伴隨有振動能級的躍遷,所以電子光譜圖比較簡單,但峰形較寬。一般來說,利用紫外吸收光譜進行定性分析信號較少。
3、紫外可見吸收光譜常用於共軛體系的定量分析,靈敏度高,檢出限低。
儀器組成
紫外可見吸收光譜儀由光源、單色器、吸收池、檢測器以及數據處理及記錄(計算機)等部分組成
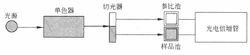 雙光束分光光度計的原理圖
雙光束分光光度計的原理圖普通紫外可見光譜儀,主要由光源、單色器、樣品池(吸光池)、檢測器、記錄裝置組成.為得到全波長範圍(200~800-nm)的光,使用分立的雙光源,其中氘燈的波長為185~395 nm,鎢燈的為350~800nm.絕大多數儀器都通過一個動鏡實現光源之間的平滑切換,可以平滑地在全光譜範圍掃描.光源發出的光通過光孔調製成光束,然後進入單色器;單色器由色散稜鏡或衍射光柵組成,光束從單色器的色散原件發出後成為多組分不同波長的單色光,通過光柵的轉動分別將不同波長的單色光經狹縫送入樣品池,然後進入檢測器(檢測器通常為光電管或光電倍增管),最後由電子放大電路放大,從微安表或數字電壓表讀取吸光度,或驅動記錄設備,得到光譜圖。
紫外、可見光譜儀設計一般都儘量避免在光路中使用透鏡,主要使用反射鏡,以防止由儀器帶來的吸收誤差.當光路中不能避免使用透明元件時,應選擇對紫外、可見光均透明的材料(如樣品池和參考池均選用石英玻璃).
儀器的發展主要集中在光電倍增管、檢測器和光柵的改進上,提高儀器的解析度、準確性和掃描速度,最大限度地降低雜散光干擾.目前,大多數儀器都配置微機操作,軟體界面更貼近我們所要完成的分析工作.
套用
總述
物質的紫外吸收光譜基本上是其分子中生色團及助色團的特徵,而不是整個分子的特徵。如果物質組成的變化不影響生色團和助色團,就不會顯著地影響其吸收光譜,如甲苯和乙苯具有相同的紫外吸收光譜。另外,外界因素如溶劑的改變也會影響吸收光譜,在極性溶劑中某些化合物吸收光譜的精細結構會消失,成為一個寬頻。所以,只根據紫外光譜是不能完全確定物質的分子結構,還必須與紅外吸收光譜、核磁共振波譜、質譜以及其他化學、物理方法共同配合才能得出可靠的結論。
化合物的鑑定
利用紫外光譜可以推導有機化合物的分子骨架中是否含有共軛結構體系,如C=C-C=C、C=C-C=O、苯環等。利用紫外光譜鑑定有機化合物遠不如利用紅外光譜有效,因為很多化合物在紫外沒有吸收或者只有微弱的吸收,並且紫外光譜一般比較簡單,特徵性不強。利用紫外光譜可以用來檢驗一些具有大的共軛體系或發色官能團的化合物,可以作為其他鑑定方法的補充。
(1)如果一個化合物在紫外區是透明的,則說明分子中不存在共軛體系,不含有醛基、酮基或溴和碘。可能是脂肪族碳氫化合物、胺、腈、醇等不含雙鍵或環狀共軛體系的化合物。
(2)如果在210~250nm有強吸收,表示有K吸收帶,則可能含有兩個雙鍵的共軛體系,如共軛二烯或α,β-不飽和酮等。同樣在260,300,330nm處有高強度K吸收帶,在表示有三個、四個和五個共軛體系存在。
(3)如果在260~300nm有中強吸收(ε=200~1 000),則表示有B帶吸收,體系中可能有苯環存在。如果苯環上有共軛的生色基團存在時,則ε可以大於10 000。
(4)如果在250~300nm有弱吸收帶(R吸收帶),則可能含有簡單的非共軛並含有n電子的生色基團,如羰基等。
純度檢查
如果有機化合物在紫外可見光區沒有明顯的吸收峰,而雜質在紫外區有較強的吸收,則可利用紫外光譜檢驗化合物的純度。對於異構體的確定,可以通過經驗規則計算出λmax值,與實測值比較,即可證實化合物是哪種異構體。如: 乙醯乙酸乙酯的酮-烯醇式互變異構
位阻作用的測定
由於位阻作用會影響共軛體系的共平面性質,當組成共軛體系的生色基團近似處於同一平面,兩個生色基團具有較大的共振作用時,λmax不改變,εmax略為降低,空間位阻作用較小;當兩個生色基團具有部分共振作用,兩共振體系部分偏離共平面時,λmax和εmax略有降低;當連線兩生色基團的單鍵或雙鍵被扭曲得很厲害,以致兩生色基團基本未共軛,或具有極小共振作用或無共振作用,劇烈影響其UV光譜特徵時,情況較為複雜化。在多數情況下,該化合物的紫外光譜特徵近似等於它所含孤立生色基團光譜的“加合”。
氫鍵強度的測定
溶劑分子與溶質分子締合生成氫鍵時,對溶質分子的UV光譜有較大的影響。對於羰基化合物,根據在極性溶劑和非極性溶劑中R帶的差別,可以近似測定氫鍵的強度。溶劑分子與溶質分子締合生成氫鍵時,對溶質分子的UV光譜有較大的影響。對於羰基化合物,根據在極性溶劑和非極性溶劑中R帶的差別,可以近似測定氫鍵的強度。
定量分析
朗伯-比爾定律是紫外-可見吸收光譜法進行定量分析的理論基礎,它的數學表達式為: A = ε b c
影響因素
影響紫外吸收光譜的因素有:1、共軛效應;2、超共軛效應;3、溶劑效應;4、溶劑pH值。
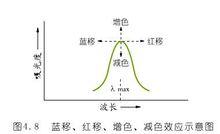 效應示意圖
效應示意圖各種因素對吸收譜帶的影響表現為譜帶位移、譜帶強度的變化、譜帶精細結構的出現或消失等。譜帶位移包括藍移(或紫移,hypsochromic shift or blue shift))和紅移(bathochromic shift or red shift)。藍移(或紫移)指吸收峰向短波長移動,紅移指吸收峰向長波長移動。吸收峰強度變化包括增色效應(hyperchromic effect)和減色效應(hypochromic effect)。前者指吸收強度增加,後者指吸收強度減小。各種因素對吸收譜帶的影響結果總結於圖中。