概述
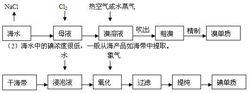 海水提碘
海水提碘碘是國防、工業、農業、醫藥等部門和行業所依賴的重要原料,海水提碘是從海水中提取元素碘的技術。海洋水體蘊藏的碘極豐富,總數估計達800億噸,世界上有許多國家從事海水提碘。20世紀70年代末,中國提出“離子-共價”的概念,研究成功JA-2型吸著劑,可直接從海水中提碘和溴;此後發展了液一固分配等富集方法,亦可直接從海水中提取碘。利用曬鹽後的滷水也可製取碘,所採用的方法有 活性炭吸附法 、澱粉吸附法、硝酸銀或硫酸銅沉澱法、離子交換樹脂法等。某些海藻具有吸附碘的能力,如乾海帶中碘的含量一般為0.3%~0.5%,比海水中碘的濃度高10萬倍。因此, 利用浸泡液浸泡海帶亦可製取碘。
海帶中碘的提取
實驗目的
提取海帶中的碘元素
實驗原理
:利用氧化劑把碘離子氧化成碘單質,再用澱粉檢驗
2KI +Cl2== I2 +2KCl I2 遇到澱粉變藍
實驗需要的儀器
天平,鑷子,剪刀,鐵架台,酒精燈,坩堝,坩堝鉗,泥三角,玻璃棒,分液漏斗
實驗藥品的選擇
海帶,氯水,澱粉溶液,四氯化碳
實驗步驟及現象
實驗步驟
①用稱取5g乾海帶,用刷子把海帶表面的附著物(不要用水洗),用酒精潤濕後,放在坩堝中。 海帶表面原理有較多白色的附著物 不用水洗是為了防止海帶中的碘化物溶於水而損失。用酒精潤濕是為了讓海帶充分燃燒。
②把坩堝置於泥三角上,用酒精燈加熱灼燒海帶成至成灰,停止加熱,自然冷卻 乾海帶燒成白色灰燼 將有機碘化物轉化為無機碘化物
③將海帶灰轉移到小燒杯中,加入20ml蒸餾水,攪拌,煮沸2~3min,使可溶物溶解,冷卻。 海帶灰煮沸時溶液渾濁 使碘離子進入溶液
④過濾,收集濾液,棄去濾渣 濾液 得到碘離子溶液
⑤向濾液中滴入1ml氯水,振盪。 滴入後溶液由無色變為棕黃色 方程式:cl2+2I-=2CL-+I2
⑥將氧化後溶液轉移到分液漏斗中,向其中加入2mlccl4,振盪,靜置。 加入ccl4後,溶液分層,有色層在上層,振盪後溶液仍分層有色層在下層,碘單質在有機溶劑中的溶解度比在水中大。

