危險級別
危險級別:8
危險等級:34
安全等級:20-26-36/37/39-45
聯合國編號:UN3260
若非註明,所有數據都依從國際單位制,以及來自標準狀況(0 °C, 100 kPa)的條件。
分子結構
固態和氣態的三氯化金都是二聚物;金的溴化物——AuBr3也是如此。兩個Au分別位於兩個正方平面的中心。此結構稱為平面型結構,AlCl3及FeCl3也屬於這個結構。AuCl3中的化學鍵主要是共價的,反映了它的高化合價和相對高的電負性。
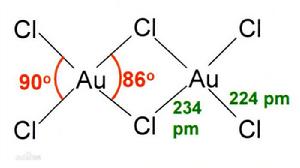 三氯化金的結構
三氯化金的結構製取方法
最常用的製備氯化金(III)的方法,是直接在高溫中氯化該金屬:
2Au + 3Cl2 → 2AuCl3 用王水與金反應可得到氯化金:
Au+HNO3+3HCl=AuCl3+NO↑+2H2O
化學性質極不穩定,加熱極易分解。常溫下水溶液呈無色。能與可溶性鹼反應:
AuCl3+3NaOH=Au(OH)3↓+3NaCl
AuCl3+3KOH=Au(OH)3↓+3KCl
而一般不能與酸反應。
物性數據
1. 性狀:紅寶石色結晶(經升華而得)或紅褐色至暗紅色的結晶塊。
2. 密度(g/mL,25/4℃):3.7
3. 相對蒸汽密度(g/mL,空氣=1):未確定
4. 熔點(ºC):229
5. 沸點(ºC,常壓):265
6. 沸點(ºC,5.2kPa):254
7. 折射率:未確定
8. 閃點(ºC):未確定
9. 比鏇光度(º):未確定
10. 自燃點或引燃溫度(ºC):未確定
11. 蒸氣壓(kPa,25ºC):未確定
12. 飽和蒸氣壓(kPa,60ºC):未確定
13. 燃燒熱(KJ/mol):未確定
14. 臨界溫度(ºC):未確定
15. 臨界壓力(KPa):未確定
16. 油水(辛醇/水)分配係數的對數值:未確定
17. 爆炸上限(%,V/V):未確定
18. 爆炸下限(%,V/V):未確定
19. 溶解性:易溶於水
存儲方法
常溫密閉,陰涼通風乾燥
合成方法
由王水作用於金,或用過量氯氣於200℃處理金而製得。往Na[AuCl4]的水溶液中加入亞硫酸而沉澱出金,經充分洗滌後,在180℃下乾燥。所得的微粉狀金置於玻璃管內的瓷舟中,並通入壓力為900~950mmHg(1mmHg=133.322Pa)的氯氣,控制反應溫度在225~250℃,便可製得氯化金。
安全信息
風險術語
R36/37/38:Irritating to eyes, respiratory system and skin. 刺激眼睛、呼吸系統和皮膚。;
安全術語
S26:In case of contact with eyes, rinse immediately with plenty of water and seek medical advice.不慎與眼睛接觸後,請立即用大量清水沖洗並徵求醫生意見。
S37/39:Wear suitable gloves and eye/face protection戴適當的手套和護目鏡或面具。
系統編號
CAS號:13453-07-1
MDL號:MFCD00014172
EINECS號:236-623-1
RTECS號:MD5420000
PubChem號:24863702
毒理學數據
1、急性毒性:主要的刺激性影響:
在皮膚上面:在皮膚和黏膜上造成腐蝕性影響,刺激皮膚和黏膜;
在眼睛上面:強烈的腐蝕性影響,刺激的影響;沒有已知的敏化影響。
計算化學數據
1、 氫鍵供體數量:0
2、 氫鍵受體數量:0
3、 可鏇轉化學鍵數量:0
4、 拓撲分子極性表面積(TPSA):0
5、 重原子數量:4
6、 表面電荷:0
7、 複雜度:8
8、 同位素原子數量:0
9、 確定原子立構中心數量:0
10、 不確定原子立構中心數量:0
11、 確定化學鍵立構中心數量:0
12、 不確定化學鍵立構中心數量:0
13、 共價鍵單元數量:1
生態學數據
通常對水體是稍微有害的,不要將未稀釋或大量產品接觸地下水,水道或污水系統,未經政府許可勿將材料排入周圍環境。
性質與穩定性
常溫常壓下穩定
避免的物料 氧化物 胺.
AuCl3有吸濕性,在水中溶解生成H2(AuCl3O);在酸性液體中稍穩定。可溶於乙醇或乙醚。
用途
金(III)鹽,特別是NaAuCl4(由 AuCl3與NaCl反應製得),可取代有毒的汞(II)鹽作為炔烴反應的催化劑。例如,通過終端炔烴的水合作用來製備甲基酮。
一般在這些條件下,酮的產量可達90%。還有一個用途是在炔烴的胺化反應中作為催化劑。近年,AuCl3開始引起有機化學家的青睞,因為它可作為其他化學反應的弱酸性催化劑,例如︰芳香烴的烷基化反應,以及把呋喃轉換成苯酚(見下)。在有機物的合成以及在製藥工業中也會用到此化學反應。例如︰2-甲基呋喃(斯而烷)可在第5位置與甲基乙烯基酮順利發生烷基化反應。
常溫下,用甲基腈中1 mole%的AuCl3隻需進行40分鐘的反應便可產生91%的產物。這個量量值得注意,因為呋喃和酮通常在酸性環境下極易發生聚合反應等的副反應。有時當炔烴存在時,會生成苯酚。
此反應中,碳原子經歷了一系列複雜的重排,產生新的芳香環。
錯誤看法編輯
認為氯金酸和氯化金是同一種物質
解析:氯金酸是由三氯化金溶於濃鹽酸得到的,氯化金是一種鹽。
實驗注意事項編輯
三氯化金刺激性很強,處理三氯化金時應戴上手套及護目鏡,避免直接接觸物料,若不小心沾上應當立即就醫。

