教學分析
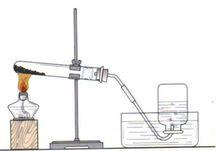 氧氣的製備
氧氣的製備教材從空氣課時,介紹空氣成分及用途,然後引入氧氣的性質,用途和製法,對氧氣進行了初步介紹。氧氣的性質和製法為進一步理解化學變化和化學性質提供了事實材料,也為概括化合反應和分解反應提供了依據,這部分教學既能加深學生對氧氣性質的認識,又能通過聯繫實際,提供學生學習化學的積極性和求知慾。
學情分析: 學生經過之前學習和活動,對氧氣的性質及用途有了較深刻的認識,對氧氣產生了濃厚的探究欲望,加之知識和實驗技能的儲備,學生早已渴望製取一瓶純淨的氧氣。這是學生第一次學習氣體製備,沒有頭緒,需要教師加以引導。本課題是氣體製備的起始課,是學生對化學實驗基本操作的綜合套用,能為今後“物質的製備”奠定基礎。
教學目標
知識與技能:
1、了解實驗室製取氧氣的主要方法和原理。
2、初步了解通過化學實驗製取新物質的方法。
過程與方法:
1、練習連線儀器的基本操作,動手製取氧氣。
2、初步學習自主設計裝置製取氧氣。
3、採用分析對比的方法認識分解反應。
情感態度與價值觀:
了解人們認識物質的過程和方法。
重點難點
重點:探究催化劑的性質和作用。
難點:探究實驗的設計和操作。
設計思路
1、本課題內容可以分為兩部分,一部分是實驗原理及分解反應,另一部分是活動與探究,由學生製取氧氣並試驗氧氣的性質。本課題的重點是氧氣的製法及實驗操作,難點是催化劑的概念、實驗室製取氧氣的反應原理。催化作用雖不是重點,但卻是教學的難點。實驗時要引導學生認真觀察並思考:
(1)不加熱過氧化氫溶液時,帶有火星的木條不能復燃;
(2)加熱過氧化氫溶液時,帶有火星的木條復燃;
(3)不加熱,但在過氧化氫溶液中加入二氧化錳時,帶有火星的木條復燃。
此時學生會產生過氧化氫溶液與二氧化錳反應,二氧化錳也是一種反應物的想法。這時再做實驗,並加以解釋,引出催化劑的概念。
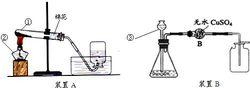 氧氣的製備
氧氣的製備2、由於過氧化氫溶液分解製取氧氣時,需要用二氧化錳做催化劑,因此在這裡介紹催化劑和催化作用。催化理論是一個難度較大的課題,在此只能根據實驗的表面現象作些簡單的介紹,使學生了解催化劑和催化作用。當然催化劑在生產和科學研究中具有廣泛套用,生物活體中的酶也是一種生物催化劑。學習這些可以激發學生學習化學的自覺性和積極性。在本課題的習題中安排了一道習題,延續這個實驗,讓學生探索有沒有其他物質能代替二氧化錳做催化劑,並用一些新的方法製取氧氣,試驗性質。這樣的習題有利於培養學生創造能力。
3、分解反應的概念可以在分析過氧化氫溶液分解的文字表達式後引出,並注意跟化合反應的要領相對照,找出二者的區別。
4、氧氣的工業製法主要是分離液態空氣。液態空氣的分餾應屬物理方法,全過程很少涉及化學變化。在本課題中把這部分內容作為資料供學生閱讀。
5、本課題的活動與探究,實際上是由學生親自動手製取氧氣並試驗氧氣的性質。要注意交待清楚以下問題:
(1)實驗裝置和操作原理,要引導學生對照觀察。學會觀察圖示是一種基本的觀察能力。按照討論的順序,引導學生從左到右,從上到下認真觀察。
(2)引導學生討論實驗中應注意哪些問題。如儀器怎樣裝置?怎樣檢查儀器的氣密性?怎樣裝入固體試劑?試管口內為什麼要放一團棉花?試管口為什麼要稍向下傾斜?怎樣用酒精燈給試管加熱?為什麼可以用排水法收集氧氣?收集氣體後為什麼要先將導管從水中撤出,然後再移去酒精燈?等等。
(3)用帶有火星的木條去試驗氧氣,是鑑定氧氣的一種常用方法。
[實驗]2-5 2-6
過氧化氫產生氧氣的條件。
二氧化錳作為催化劑(觸媒)的特徵:“一變兩不變”。
化學反應速率改變;在反應前後,催化劑的質量不變,催化劑的化學性質不變。
反應物的狀態、生成物的性質、反應條件決定發反應設備的設計與改進。
[實驗]2-7
比較兩種不同的方法選擇設備的依據。收集氧氣的方法與依據。
[概念教學]
化學反應的分類:
化合反應“多變一”;
分解反應“一變多”。
分類方法與學習技巧。
教學過程
引入
老師敘述圍棋擂台賽聶衛平吸氧戰勝日本主將加藤正夫九段取得擂台賽勝利的故事。氧氣的作用可真不小!那么,我們又是如何獲得氧氣的呢?
學生:你上次不是用加熱高錳酸鉀的方法的嗎?
師:不錯。今天我還想介紹另一種製備方法,即分解過氧化氫的方法。
新課
1.讓我們一起來製備氧氣(老師適當介紹分液漏斗等儀器後,由學生來裝配實驗裝置、添加藥品、收集氧氣並檢驗。)
2.讓我們思考:在上述實驗中,我們為什麼要添加一些灰粉-----二氧化錳?你觀察到它發生了什麼變化?如果不放又將怎樣?(學生嘗試不加二氧化錳來制氧氣,結果並沒有產生。)問題出在哪裡?
3.一起來探究:二氧化錳究竟起什麼作用?
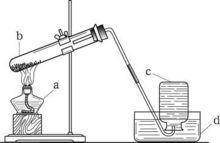 氧氣的製備
氧氣的製備學生參考作業本總複習題18設計實驗:
A..設計對比實驗分析二氧化錳的作用。
B.將反應後的物質過濾烘乾,稱重。
C將上述烘乾藥品.重新試驗。.
4.實驗:第一步前面已完成.第二步要引導學生烘乾的方法------在酒精燈上方直接烘?在石棉網上烘?日光曬?電吹風?最後,選擇最好方案進行操作。
5.得出結論:二氧化錳能加快反應速度,反應前後質量不變,性質也不變。
6.小結:分解雙氧水可制氧氣.在反應過程中能改變反應速度,本身的質量和性質並不改變的物質叫催化劑。.
7.想一想:二氧化錳能加快其他化學反應嗎?
教學反思
這節課,我改變了以往的教學策略:實行學生閱讀與帶領學生體會集合起來。一上課,我先讓學生們閱讀教材有關內容,之後讓學生分組展開討論概括教材講述的知識點,以及對該知識的理解。帶著學生的疑惑開始本節課的探究學習,這時學生已經不再是一個坐在底下被動接受知識的聽者,而是探究活動中的主體。
通過對過氧化氫實驗(①取過氧化氫溶液,用帶火星的木條檢驗;②取過氧化氫溶液,向其中加入適量二氧化錳,用帶火星的木條檢驗;③實驗②沒有氣泡冒出時,再向其中加入適量過氧化氫溶液,用帶火星的木條檢驗)的對比觀察、探討和分析,學生的疑惑輕鬆得以解決。師生共同探討的過程,明顯體現出師生互動的過程。在跟學生一起進行探究的時候,老師應是組織者、引導者,學生才是真正的主體。教師鼓勵學生對問題發表不同的見解,對他們提出的見解中合理的部分給予充分的肯定和表揚,對其中不合理的部分加以詳細的分析,用學生能懂的理論或實驗來說服他,讓他明白自己的錯誤所在。當學生在探究過程中遇到了困難,老師要及時加以幫助,以確保探究能順利的進行下去,同時也鞏固了老師在學生心目中的地位:老師還是一個智者。
由於在本課題中集中了一些基本操作,而學生的動手能力還很差,因此,主要採用教師演示實驗、與學生討論一些基本操作的要點和要求。在用二氧化錳做催化劑分解過氧化氫的實驗中,只須加綠豆體積大的二氧化錳粉末,不要像書中圖示那樣多,否則反應會很劇烈,難以控制。用加熱氯酸鉀、二氧化錳、氯酸鉀和二氧化錳混合物這三組對比實驗來講解催化劑的概念比較好,用時短,現象明顯。
新課程改革帶來了教師教學觀念和方式的改變。在以後的教學過程中我們教師一定要善於發現機會、尋找機會、製造機會,與學生一起進行探究活動,在活動中讓學生的思維能力、創新能力得到磨練、升華,使學生的終生學習能力得以提高。而本節課恰好能夠充分發揮學生的主體作用,培養學生的動手興趣,發揮學生的想像力。真正把培養學生的素養放在教學的地位上來。

