發現
1982年,美國科學家T.Cech和他的同事在對“四膜蟲編碼rRNA前體的DNA序列含有間隔內含子序列”的研究中發現,自身剪接內含子的RNA具有催化功能,並因此獲得了1989年諾貝爾化學獎。
為了與酶(enzyme)區分,Cech將它命名為ribozyme,其中文譯名“核酶”已得到大多數人的認可。因為其本質是RNA,而且不參與翻譯,所以它又屬於組成型非編碼RNA中的一份子。核酶在非編碼RNA的分類中亦被稱為“催化性小RNA”。
特點
與一般的反義RNA相比,核酶具有較穩定的空間結構,不易受到RNA酶的攻擊。更重要的是,核酶在切斷mRNA後,又可從雜交鏈上解脫下來,重新結合和切割其它的mRNA分子。
分類
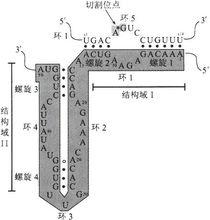 核酶
核酶核酶是具有催化活性的RNA ,主要參加RNA的加工與成熟。天然核酶可分為四類:(1)異體催化剪下型,如RNaseP;(2)自體催化的剪下型,如植物類病毒、擬病毒和衛星RNA;(3)第一組內含子自我剪接型,如四膜蟲大核26SrRNA;(4)第二組內含子自我剪接型。利用反義技術研製的藥物稱反義藥物。反義藥物作用於產生蛋白的基因,因此可廣泛套用於多種疾病的治療,如傳染病、炎症、心血管疾病及腫瘤等。與傳統藥物比較反義藥物更具選擇性及效率,因此也更高效低毒。基於上述特點反義藥物已成為藥物研究和開發的熱點。而且反義技術還可以套用於生物科學的基礎研究。
作用
隨著對核酶的深入研究,已經認識到核酶在遺傳病,腫瘤和病毒性疾病上的潛力。
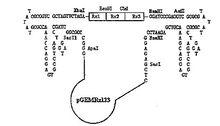 核酶
核酶比如,對於愛滋病毒HIV的轉錄信息來源於RNA而非DNA,核酶能夠在特定位點切斷RNA,使得它失去活性。如果一個能專一識別HIV的RNA的核酶存在於被病毒感染的細胞內,那么它就能建立抵抗入侵的第一防線。甚至,HIV確實進入到了細胞並進行了複製,RNA也可以在病毒生活史的不同階段切斷HIV的RNA而不影響自身的RNA。又如,白血病是造血系統的惡性腫瘤,目前尚缺少有效的治療方法。核酶的發現,尤其是錘頭狀核酶,為白血病的基因治療帶來了新的希望。近些年,在國外的一些國家已經在小白鼠體內得到較好的效果。 核酶是在對多種植物病毒衛星RNA及類病毒RNA的自我剪接研究中 發現的,數量較少,常見於rRNA的內含子。
核酶的具體作用主要有:
1. 核苷酸轉移作用。
2. 水解反應,即磷酸二酯酶作用。
3. 磷酸轉移反應,類似磷酸轉移酶作用。
4. 脫磷酸作用,即酸性磷酸酶作用。
5. RNA內切反應,即RNA限制性內切酶作用。核酸內切酶可以催化水解多核苷酸內部的磷酸二酯鍵。有些核酸內切酶僅水解5′磷酸二酯鍵,把磷酸基團留在3′位置上,稱為5′-內切酶;而有些僅水解3′-磷酸二酯鍵,把磷酸基團留在5′位置上,稱為3′-內切酶。能專一性地識別並水解雙鏈DNA上的特異核苷酸順序,稱為限制性核酸內切酶(restriction endonuclease,簡稱限制酶)。當外源DNA侵入細菌後,限制性內切酶可將其水解切成片段,從而限制了外源DNA在細菌細胞內的表達,而細菌本身的DNA由於在該特異核苷酸順序處被甲基化酶修飾,不被水解,從而得到保護。限制性核酸內切酶可被分成三種類型。Ⅰ型和Ⅲ型限制酶水解DNA需要消耗ATP,全酶中的部分亞基有通過在特殊鹼基上補加甲基基團對DNA進行化學修飾的活性。Ⅱ型限制酶水解DNA不需要ATP也不以甲基化或其它方式修飾DNA,能在所識別的特殊核苷酸順序內或附近切割DNA。因此,被廣泛用於DNA分子克隆和序列測定。
人工合成
 核酶
核酶隨著對核酶進一步研究,人們還人工合成了一些具有催化活性的DNA。
目前,並沒有發現有天然存在的催化性DNA。