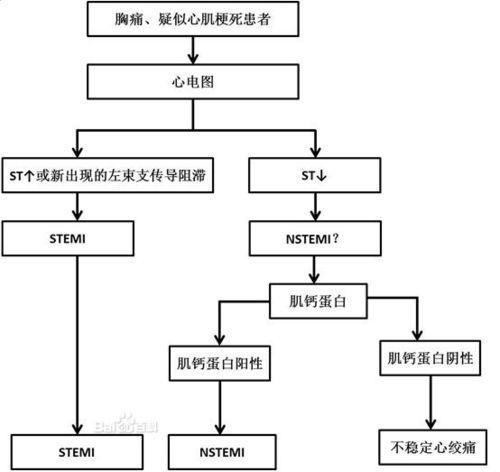
分類
由於不同類型的ACS的治療策略存在一定差異,根據患者發病時的心電圖ST段是否抬高,可將ACS分為急性ST段抬高性心肌梗死(STEMI)和非ST段抬高性急性冠狀動脈綜合徵(NSTE-ACS)。其中,根據心肌損傷血清生物標誌物[肌酸激酶同工酶(CK)-MB或心臟肌鈣蛋白(Cardiactroponin,cTn)]測定結果,NSTE-ACS又包括非ST段抬高性心肌梗死(NSTEMI)和不穩定型心絞痛(UA)(見圖1)。
圖1ACS的分類和命名
 急性冠狀動脈綜合徵
急性冠狀動脈綜合徵病因
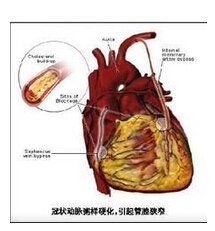
絕大多數ACS是冠狀動脈粥樣硬化斑塊不穩定的結果。
極少數ACS由非動脈粥樣硬化性疾病所致(如動脈炎、外傷、夾層、血栓栓塞、先天異常、濫用古柯鹼,或心臟介入治療併發症)。
當冠狀動脈的供血與心肌的需血之間發生矛盾,冠狀動脈血流量不能滿足心肌代謝的需要,引起心肌急劇的、暫時的缺血缺氧時,即可發生心絞痛。
冠狀動脈粥樣硬化可造成一支或多支血管管腔狹窄和心肌血供不足,一旦血供急劇減少或中斷,使心肌嚴重而持久地急性缺血達20~30分鐘以上,即可發生急性心肌梗死(AMI)。
危險因素
1.主要的危險因素
(1)年齡、性別本病臨床上多見於40歲以上的中、老年人。近年來,臨床發病年齡有年輕化趨勢。與男性相比,女性發病率較低,但在更年期後發病率增加。
(2)血脂異常脂質代謝異常是動脈粥樣硬化最重要的危險因素。總膽固醇(TC)、甘油三酯(TG)、低密度脂蛋白(LDL)或極低密度脂蛋白(VLDL)增高,相應的載脂蛋白B(ApoB)增高;高密度脂蛋白(HDL)減低,載脂蛋白A(ApoA)降低都被認為是危險因素。此外脂蛋白(a)[Lp(a)]增高也可能是獨立的危險因素。在臨床實踐中,以TC及LDL增高最受關注。
(3)高血壓血壓增高與本病關係密切。60%~70%的冠狀動脈粥樣硬化患者有高血壓,高血壓患者患本病較血壓正常者高3~4倍。收縮壓和舒張壓增高都與本病密切相關。
(4)吸菸吸菸者與不吸菸者比較,本病的發病率和病死率增高2~6倍,且與每日吸菸的支數呈正比。被動吸菸也是危險因素。
(5)糖尿病和糖耐量異常糖尿病患者中不僅本病發病率較非糖尿病者高出數倍,且病變進展迅速。本病患者糖耐量減低者也十分常見。
2.其他危險因素
①肥胖。②從事體力活動少,腦力活動緊張,經常有工作緊迫感者。③西方的飲食方式:常進較高熱量、含較多動物性脂肪、膽固醇、糖和鹽的食物者。④遺傳因素:家族中有在年齡<50歲時患本病者,其近親得病的機會可5倍於無這種情況的家族。⑤性情急躁、好勝心和競爭性強、不善於勞逸結合的A型性格者。
3.新近發現的危險因素
①血中同型半胱氨酸增高;②胰島素抵抗增強;③血中纖維蛋白原及一些凝血因子增高;④病毒、衣原體感染等。
臨床表現
典型表現為發作性胸骨後悶痛,緊縮壓榨感或壓迫感、燒灼感,可向左上臂、下頜、頸、背、肩部或左前臂尺側放射,呈間斷性或持續性,伴有出汗、噁心、呼吸困難、窒息感、甚至暈厥,持續>10~20分鐘,含硝酸甘油不能完全緩解時常提示AMI。
部分患者在AMI發病前數日有乏力,胸部不適,活動時心悸、氣急、煩躁、心絞痛等前驅症狀。
不典型表現有:牙痛、咽痛、上腹隱痛、消化不良、胸部針刺樣痛或僅有呼吸困難。這些常見於老年、女性、糖尿病、慢性腎功能不全或痴呆症患者。臨床缺乏典型胸痛,特別當心電圖正常或臨界改變時,常易被忽略和延誤治療,應注意連續觀察。大多數ACS患者無明顯的體徵。
重症患者可出現皮膚濕冷、面色蒼白、煩躁不安、頸靜脈怒張等,聽診可聞肺部囉音、心律不齊、心臟雜音、心音分裂、第三心音、心包摩擦音和奔馬律。
檢查
1.心肌損傷標誌物
AMI時會出現心肌損傷標誌物的升高,且其增高水平與心肌梗死範圍及預後明顯相關。 ①肌鈣蛋白I(cTnI)或T(cTnT)起病3~4小時後升高,cTnI於11~24小時達高峰,7~10天降至正常,cTnT於24~48小時達高峰,10~14天降至正常。肌鈣蛋白增高是診斷心肌梗死的敏感指標。 ②肌酸激酶同工酶CK-MB起病後4小時內增高,16~24小時達高峰,3~4天恢復正常。
2.心電圖
(1)STEMI①ST段抬高呈弓背向上型,在面向壞死區周圍心肌損傷區的導聯上出現;②寬而深的Q波(病理性Q波),在面向透壁心肌壞死區的導聯上出現;③T波倒置,在面向損傷區周圍心肌缺血區的導聯上出現。在背向梗死區的導聯則出現相反的改變,即R波增高、ST段壓低和T波直立並增高。
(2)NSTE-ACSST-T波動態變化是NSTE-ACS最有診斷價值的心電圖異常表現。症狀發作時可記錄到一過性ST段改變(常表現2個或以上相鄰導聯ST段下移≥O.1mV),症狀緩解後ST段缺血性改變改善,或者發作時倒置T波是“偽正常化”,發作後恢復至原倒置狀態更具有診斷意義,並提示有急性心肌缺血或嚴重冠脈疾病。初始心電圖正常或臨界改變,不能排除NSTE-ACS的可能性;患者出現症狀時應再次記錄心電圖,且與無症狀時或既往心電圖對比,注意ST-T波的動態變化。
3.超聲心動圖
AMI及嚴重心肌缺血時可見室壁節段性運動異常。同時有助於了解左心室功能,診斷室壁瘤和乳頭肌功能失調等。
4.其他影像學檢查
放射性核素檢查,MRI等。
診斷
當有典型的缺血性胸痛症狀或心電圖動態改變而無心肌壞死標誌物升高時,可診斷為心絞痛。
存在下列任何一項時,可以診斷心肌梗死。
1.心臟生物標誌物(最好是肌鈣蛋白)增高或增高后降低,至少有1次數值超過正常上限,並有以下至少1項心肌缺血的證據:
(1)心肌缺血臨床症狀;
(2)心電圖出現新的心肌缺血變化,即新的ST段改變或左束支傳導阻滯(按心電圖是否有ST段抬高,分為STEMI和NSTEMI);
(3)心電圖出現病理性Q波;
(4)影像學證據顯示新的心肌活力喪失或區域性室壁運動異常。
2.突發、未預料的心臟性死亡,涉及心臟停跳,常伴有提示心肌缺血的症狀、推測為新的ST段抬高或左束支傳導阻滯、冠狀動脈造影或屍體檢驗顯示新鮮血栓的證據,死亡發生在可取得血標本之前,或心臟生物標誌物在血中出現之前。
3.在基線肌鈣蛋白正常、接受經皮冠狀動脈介人治療(PCI)的患者,心臟生物標誌物升高超過正常上限提示圍手術期心肌壞死。心臟生物標誌物升高超過正常上限的3倍定為PCI相關的心肌梗死,其中包括1種已經證實的支架血栓形成相關的亞型。
4.基線肌鈣蛋白值正常、行冠狀動脈旁路移植術(CABG)患者,心臟生物標誌物升高超過正常上限,提示圍手術期心肌壞死。將心臟生物標誌物升高超過正常上限的5倍並發生新的病理性Q波或新的左束支傳導阻滯,或冠狀動脈造影證實新移植的或自身的冠狀動脈閉塞,或有心肌活力喪失的影像學證據,定為與CABG相關的心肌梗死。
5.有AMI的病理學發現。
鑑別診斷
1.穩定型心絞痛
胸痛常由體力勞動或情緒激動(如憤怒、焦急、過度興奮等)所誘發,飽食、寒冷、吸菸、心動過速、休克等亦可誘發。疼痛多發生於勞力或激動的當時,而不是在一天勞累之後。典型的心絞痛常在相似的條件下重複發生,但有時同樣的勞力只在早晨而不在下午引起心絞痛。疼痛出現後常逐步加重,然後在3~5分鐘內漸消失。停止原來誘發症狀的活動或舌下含用硝酸甘油能在幾分鐘內使之緩解。
2.主動脈夾層
胸痛一開始即達高峰,常放射到背、肋、腹、腰和下肢,兩上肢的血壓和脈搏可有明顯差別,可有主動脈瓣關閉不全的表現,偶有意識模糊和偏癱等神經系統受損症狀。但無血清心肌壞死標記物升高等可資鑑別。二維超聲心動圖檢查、X線或磁共振體層顯像有助於診斷。
3.急性肺動脈栓塞
可發生胸痛、咯血、呼吸困難和休克。但有右心負荷急劇增加的表現如發紺、肺動脈瓣區第二心音亢進、頸靜脈充盈、肝大、下肢水腫等。心電圖示I導聯S波加深,Ⅲ導聯Q波顯著T波倒置,胸導聯過度區左移,右胸導聯T波倒置等改變,可資鑑別。
4.急腹症
急性胰腺炎、消化性潰瘍穿孔、急性膽囊炎、膽石症等,均有上腹部疼痛,可能伴休克。仔細詢問病史、作體格檢查、心電圖檢查、血清心肌酶和肌鈣蛋白測定可協助鑑別。
5.急性心包炎
心包炎的疼痛與發熱同時出現,呼吸和咳嗽時加重,早期即有心包摩擦音,後者和疼痛在心包腔出現滲液時均消失;全身症狀一般不如AMI嚴重;心電圖除aVR外,其餘導聯均有ST段弓背向下的抬高,T波倒置,無異常Q波出現。
併發症
AMI患者可並發:
1.心律失常
見於75%~95%的AMI患者,多發生在起病1~2天,而以24小時內最多見。各種心律失常中以室性心律失常最多,尤其是室性期前收縮。室顫是AMI早期,特別是入院前主要的死因。房室傳導阻滯和束支傳導阻滯也較多見,室上性心律失常則較少,多發生在心力衰竭者中。
2.低血壓和休克
休克多在起病後數小時至數日內發生,見於約20%的AMI患者,主要是心源性,為心肌廣泛(40%以上)壞死,心排血量急劇下降所致。
3.心力衰竭
主要是急性左心衰竭,可在AMI起病最初幾天內發生,或在疼痛、休克好轉階段出現,為梗死後心臟舒縮力顯著減弱或不協調所致,發生率約為32%~48%。出現呼吸困難、咳嗽、發紺、煩躁等症狀,嚴重者可發生肺水腫,隨後可有頸靜脈怒張、肝大、水腫等右心衰竭表現。右心室AMI者可一開始即出現右心衰竭表現,伴血壓下降。
4.乳頭肌功能失調或斷裂
總發生率可高達50%。造成不同程度的二尖瓣脫垂並關閉不全,引起心力衰竭。重症者可在數日內死亡。
5.心臟破裂
少見,常在起病1周內出現,多為心室游離壁破裂,造成猝死。偶為心室間隔破裂造成穿孔,可引起心力衰竭和休克而在數日內死亡。心臟破裂也可為亞急性,患者能存活數月。
6.栓塞
發生率1%~6%,見於起病後1~2周,可為左心室附壁血栓脫落所致,引起腦、腎、脾或四肢等動脈栓塞。也可因下肢靜脈血栓形成部分脫落所致,則產生肺動脈栓塞。
7.心室壁瘤
主要見於左心室,發生率5%~20%。瘤內可發生附壁血栓而導致栓塞。
8.心肌梗死后綜合征
發生率約10%。於AMI後數周至數月內出現,可反覆發生,表現為心包炎、胸膜炎或肺炎,有發熱、胸痛等症狀。
治療
急救措施:發生疑似急性缺血性胸痛症狀時應立即停止活動、休息,並儘早向急救中心呼救。對無禁忌證的ACS患者應立即舌下含服硝酸甘油,每5分鐘重複1次,總量不超過1.5mg。
“時間就是心肌,時間就是生命”。對於STEMI患者,採用溶栓或介入治療(PCI)方式儘可能早地開通梗死相關動脈可明顯降低死亡率、減少併發症、改善患者的預後。
治療方法:藥物治療、手術治療、介入治療、其他治療等。
1.STEMI的治療
圖2ACS患者評估與處理流程
(1)住院後初始處理所有STEMI患者到院後應立即給予吸氧和心電圖、血壓和血氧飽和度監測,伴有嚴重低氧血症者,需面罩加壓給氧或氣管插管並機械通氣。鎮痛治療。
(2)溶栓治療STEMI急性期行直接PCI已成為首選方法,但由於能開展直接PCI的醫院不多,當前尚難以普遍套用。溶栓治療具有快速、簡便、經濟、易操作的特點,靜脈溶栓仍然是較好的選擇。
發病3小時內行溶栓治療,其臨床療效與直接PCI相當。發病3~12小時內行溶栓治療,其療效不如直接PCI,但仍能獲益。發病12~24小時內,如果仍有持續或間斷的缺血症狀和持續ST段抬高,溶栓治療仍然有效。STEMI發生後,血管開通時間越早,則挽救的心肌越多。目標是在救護車到達的30分鐘內開始溶栓。
(3)經皮冠狀動脈介入(PCI)治療PCI可快速有效開通梗死相關動脈,是STEMI急性期的首選治療。
1)直接PCI①如果即刻可行,且能及時進行(就診-球囊擴張時間<90min),對症狀發病12小時內的STEMI(包括正後壁心肌梗死)或伴有新出現或可能新出現左束支傳導阻滯的患者應行直接PCI。②年齡<75歲,在發病36小時內出現休克,病變適合血管重建,並能在休克發生18小時內完成者,應行直接PCI,除非因為患者拒絕、有禁忌證和(或)不適合行有創治療。③症狀發作12小時、無症狀、血液動力學和心電穩定的患者不宜行直接PCI治療。
2)轉運PCI高危STEMI患者就診於無直接PCI條件的醫院,尤其是有溶栓禁忌證或雖無溶栓禁忌證但已發病>3小時的患者,可在抗栓(抗血小板或抗凝)治療同時,儘快轉運患者至可行PCI的醫院。
(4)抗栓治療
1)抗血小板治療①阿司匹林:所有患者只要無禁忌證,均應立即口服水溶性阿司匹林或嚼服腸溶阿司匹林300mg,繼以100mg/d長期維持。②噻吩並吡啶類:在首次或再次PCI之前或當時應儘快服用氯吡格雷初始負荷量300mg(擬直接PCI者最好600mg)。住院期間,所有患者繼續服用氯吡格雷75mg/d。出院後,未置入支架患者,應使用氯吡格雷75mg/d至少28天,條件允許者也可用至1年。因急性冠狀動脈綜合徵接受支架置入的患者,術後使用氯吡格雷75mg/d至少12個月。置入藥物洗脫支架的患者可考慮氯吡格雷75mg/d,15個月以上。對阿司匹林禁忌者,可長期服用氯吡格雷。③GPIIb/IIIa受體拮抗劑:阿昔單抗、依替非巴肽、替羅非班等,可選擇性用於血栓負荷重的患者和噻吩並吡啶類藥物未給予適當負荷量的患者。
2)抗凝治療①普通肝素;②低分子量肝素;③磺達肝癸鈉;④比伐盧定;⑤口服抗凝劑治療:STMI急性期後,以下情況需口服抗凝劑治療:超聲心動圖提示心腔內有活動性血栓,口服華法林3~6個月;合併心房顫動者;不能耐受阿司匹林和氯吡格雷者,可長期服用華法林,維持INR2-3。若需在阿司匹林和氯吡格雷的基礎上加用華法林時,需注意出血的風險,嚴密監測INR,縮短監測間隔。
(5)抗心肌缺血和其他治療
1)硝酸酯類如患者收縮壓低於90mmHg或較基礎血壓降低>30%、嚴重心動過緩(心率分)或心動過速(心率>100次/分)、擬診右心室梗死,則不應使用硝酸酯類藥物。
2)β受體阻滯劑縮小心肌梗死面積,減少復發性心肌缺血、再梗死、室顫及其他惡性心律失常,對降低急性期病死率有肯定的療效。無該藥禁忌證時,應於發病後24h內常規口服套用。
3)血管緊張素轉換酶抑制劑(ACEI)和血管緊張素受體阻滯劑(ARB)可減少充盈性心力衰竭的發生,降低病死率。如無禁忌證,所有STEMI患者均應給予ACEI長期治療。如果患者不能耐受ACEI,可考慮換用ARB。
4)醛固酮受體拮抗劑對STEMI後左室射血分數(LVEF)≤0.4,有心功能不全或糖尿病,無明顯腎功能不全(血肌酐男性小於等於221μmol/L(2.5mg/dl),女性小於等於177μmol/L(2.0mg/dl)、血鉀小於等於5mmol/L〕的患者,應給予醛固酮受體拮抗劑。
5)鈣拮抗劑不推薦使用短效二氫吡啶類鈣拮抗劑。
6)他汀類藥物除調脂作用外,他汀類藥物還具有抗炎、改善內皮功能、抑制血小板聚集的多效性,因此,所有無禁忌證的STEMI患者入院後應儘早開始他汀類藥物治療,且無需考慮膽固醇水平。他汀類治療的益處不僅見於膽固醇升高患者,也見於膽固醇正常的冠心病患者。所有心肌梗死後患者都應該使用他汀類藥物將低密度脂蛋白膽固醇水平控制在2.6mmol/L(100mg/dl)以下。
(6)冠脈搭橋術(CABG)對少數STEMI合併心源性休克不適宜PCI者,急診CABG可降低病死率。機械性併發症(如心室游離壁破裂、乳頭肌斷裂、室間隔穿孔)引起心源性休克時,在急性期需行CABG和相應心臟手術治療。
(7)治療併發症
2.NSTE-ACS的治療
NSTE-ACS的處理旨在根據危險分層採取適當的藥物治療和冠脈血運重建策略(表1)。可使用TIMI或GRACE積分系統對NSTE-ACS患者的缺血風險進行危險分層。使用CRUSADE出血積分系統對NSTE-ACS患者的出血風險進行危險評估。
表1NSTE-ACS早期危險分層
(1)抗栓治療與STEMI相似。
(2)抗心肌缺血和其他治療與STEMI相似。
(3)溶栓治療由於發病機制與STEMI存在不同,NSTE-ACS不建議使用溶栓治療。
(4)PCI治療
1)高危患者對高危NSTE-ACS[包括有血清cTn或心電圖ST-T波變化,糖尿病、腎功能不全(eGFR<60ml/min・1.73m )、心功能減退(LVEF<40%)、梗死後早期心絞痛、最近PCI、以往CABG史和中至高GRACE危險積分]的患者主張於症狀發生最初72h內行診斷性冠脈造影,然後根據病變情況作血運重建治療。對心肌缺血極高危患者,即難治性心絞痛伴心力衰竭、危及生命的室性心律失常或血液動力學不穩定,可行緊急侵入性策略(140合併多項其他高危因素(例如cTnT或ST-T波變化)的患者,推薦早期(<24小時)侵入性策略。
2)早期穩定患者對發生臨床事件高風險的NSTE-ACS患者,如無嚴重合併症或血運重建禁忌證,應及早冠脈造影或血運重建。對最初穩定的高危NSTE-ACS患者,應早期介入(入院12~24小時內)。對最初穩定且無嚴重合併症和血運重建禁忌證的NSTE-ACS患者,最初可考慮保守治療,以後的治療決策(保守或介入)由醫生根據病情或患者的意願決定。
3)低至中危患者對低至中危且無症狀復發的NSTE-ACS患者,行無創性心肌缺血評估。心肌血運重建策略(PCI或CABG)應基於臨床症狀和冠脈病變嚴重性。
4)嚴重並存疾病患者肝功能和肺功能衰竭或癌腫患者,不主張行早期診斷性冠脈造影和血運重建。
(5)CABG
(6)治療併發症
預後
AMI患者的預後與梗死範圍的大小、側支循環產生的情況以及治療是否及時有關。急性期住院病死率過去一般為30%左右,採用監護治療後降至15%左右,採用溶栓療法後再降至8%左右,住院90分鐘內施行介入治療後進一步降至4%左右。死亡多發生在第一周內,尤其在數小時內,發生嚴重心律失常、休克或心力衰竭者,病死率尤高。NSTEMI近期預後雖佳,但長期預後則較差,NSTE-ACS患者經急性期處理、病情穩定後,仍可能因冠脈粥樣硬化病變持續發展,而引起心肌缺血事件復發。出院後1年內再次住院率高達20%,大於40歲患者的病死率在男性為18%,在女性為20%。
預防
1.非藥物干預
(1)戒菸
(2)運動ACS患者出院前應作運動耐量評估,並制定個體化體力運動方案。對於所有病情穩定的患者,建議每日進行30~60分鐘中等強度的有氧運動(例如快步行走等),每周至少堅持5天。此外,還可建議每周進行1~2次阻力訓練。體力運動應循序漸進,並避免誘發心絞痛等不適症狀。
(3)控制體重出院前以及出院後隨診時應監測體重,並建議其通過控制飲食與增加運動將體質指數控制於24kg/m 以下。
2.藥物預防
(1)抗血小板治療若無禁忌證,所有ACS患者出院後均應長期服用阿司匹林(75~150mg/d)治療。因存在禁忌證而不能套用阿司匹林者,可用氯吡格雷(75mg/d)替代。接受PCI的患者,需聯合套用阿司匹林和氯吡格雷。
(2)ACEI和ARB類藥物若無禁忌證,所有伴有心力衰竭(LVEF<0.45)、高血壓、糖尿病或慢性腎臟疾病的STEMI患者均應長期服用ACEI。低危STEMI患者(即LVEF正常、已成功實施血運重建且各種心血管危險因素已得到滿意控制者)亦可考慮ACEI治療。具有適應證但不能耐受ACEI治療者,可套用ARB類藥物。
(3)β受體阻滯劑若無禁忌證,所有STEMI患者均應長期服用β受體阻滯劑治療,並根據患者耐受情況確定個體化的治療劑量。
(4)醛固酮拮抗劑無明顯腎功能損害和高血鉀的心肌梗死後患者,經過有效劑量的ACEI與β受體阻滯劑治療後其LVEF<0.4者,可考慮套用醛固酮拮抗劑治療,但須密切觀察相關不良反應(特別是高鉀血症)的發生。
3.控制心血管危險因素
(1)控制血壓應將其血壓控制於<140/90mmHg,合併慢性腎病者應將血壓控制於<130/80mmHg。此類患者宜首選β受體阻滯劑和(或)ACEI治療,必要時可考慮套用小劑量噻嗪類利尿劑等藥物。
(2)調脂治療出院後應堅持使用他汀類藥物,將LDL-C控制在<2.60mmol/L(100mg/dl),並可考慮達到更低的目標值[LDL-C<2.08mmol/L(80mg/dl)];對於合併糖尿病者,應將LDL-C控制在L(80mg/dl)以下。達標後不可停藥,也不宜盲目減小劑量。LDL-C未達標時,聯合使用膽固醇吸收抑制劑或其他降脂藥物。LDL-C達標後,若甘油三酯>2.26mmol/l,則聯合使用貝特類或菸鹼類藥物。甘油三酯>1.70mmol/l且改善生活方式治療3個月後仍高時,應加用貝特類或煙酸類藥物。
(3)血糖管理若患者一般健康狀況較好、糖尿病病史較短、年齡較輕,可將其糖化血紅蛋白控制在7%以下;若患者一般健康狀況較差、糖尿病病史較長、年齡較大時,宜將糖化血紅蛋白控制於7%~8%。
(4)置入式心臟除顫器(ICD)以下兩類患者置入ICD可以顯著獲益:①LVEF小於等於0.4,且伴有自發非持續性室速,和(或)電程式刺激可誘發出單形持續性室速者;②心肌梗死至少40d後患者仍存在心力衰竭症狀(NYHA心功能且II一lV級),且LVEF小於等於0.30者。AMI後雖經最佳藥物治療仍存在輕度心力衰竭症狀(NYHA心功能I級)且LVEF小於等於0.35者也可考慮置入ICD。
(5)康復治療出院後堅持規律適度的體力鍛鍊有助於控制肥胖、高血壓、血脂異常以及高血糖等心血管危險因素,並增加心血管儲備功能,從而對其預後產生有益影響。與一般體力運動相比,以體力活動為基礎的程式化康復治療可能具有更佳效果。薈萃分析顯示,冠心病患者接受康復治療可使總病死率降低20%~30%,使心臟性病死率降低約30%。
護理
ACS患者應注意採用清淡易消化的飲食,急性期過後宜採用低鹽低脂飲食,如合併糖尿病還應注意控制糖分的攝入。
AMI急性期時,應以臥床休息為主。對血液動力學穩定且無併發症的患者可根據病情臥床休息1~3天,一般第2天可允許患者坐在床旁大便,病情不穩定及高危患者臥床時間可適當延長。避免過度緊張、焦慮、興奮和勞累,注意保持大便通暢,便秘者應適當通便,切不可過度用力排便,以免誘發心肌缺血、心律失常甚至心臟破裂。
戒菸:所有ACS患者均需戒菸。
運動:ACS患者出院前應作運動耐量評估,並制定個體化體力運動方案。對於所有病情穩定的患者,建議每日進行30~60分鐘中等強度的有氧運動(例如快步行走等),每周至少堅持5天。此外,還可建議每周進行1~2次阻力訓練。體力運動應循序漸進,並避免誘發心絞痛等不適症狀。
控制體重:應監測體重,建議通過控制飲食與增加運動將體質指數控制於24kg/m 以下。
參考文獻:
[1]中華醫學會心血管病學分會,中華心血管病雜誌編輯委員會.急性ST段抬高型心肌梗死診斷和治療指南.中華心血管病雜誌,2010,38(8):675-690.
[2]中華醫學會心血管病學分會,中華心血管病雜誌編輯委員會.非ST段抬高急性冠狀動脈綜合徵診斷和治療指南.中華心血管病雜誌,2012,40(5):353-367.
[3]陸再英,鍾南山.內科學,第七版。北京:人民衛生出版社,2007.267-302.