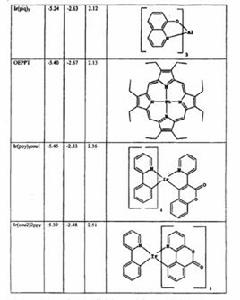
定義
當取代基取代苯環上的氫後,導致苯環上電子密度升高的叫基團供電子基團;反之,苯環上電子密度降低的基團叫吸電子基團。一般定義為對外表現正電場的基團。
分類
強吸電子基團
叔胺正離子(-N R)、硝基(-NO)、三鹵甲基(-CX)X=F、Cl
中吸電子基團
氰基(-CN)、磺酸基(-SOH)
弱吸電子基團
甲醯基(-CHO)、醯基(-COR)、羧基(-COOH)
判斷方法
只有吸電子誘導效應(-I),如:三鹵甲基(-CX)X=F、Cl
吸電子誘導效應(-I)和吸電子共軛效應(-C)共同作用的結果是基團表現為吸電子,如:
叔胺正離子(-NR)、硝基(-NO)、氰基(-CN)、磺酸基(-SOH)、甲醯基(-CHO)、醯基(-COR)、羧基(-COOH)
電負法辨別
還原法
將基團加上一個氫原子(-H)或者羥基(-OH)使之構成一個中心元素的化合價為常用的分子,如此以來,分子呈中性,氫原子顯正電,羥基顯負電,剩下的基團所表現出的電性就可以判斷了。如:甲基(CH),用還原法給它加上一個氫原子(-H)將其還原為甲烷,因為我們知道甲烷是一個分子,呈點中性,而氫原子電負性很低,通常與其他基團結合時都顯正電場,故此甲基就應該顯負電場,根據上面的定義可知甲基為供電基團。
再如:硝基(NO),用還原法給它加上一個羥基(-OH)使之構成硝酸分子(HNO),因羥基顯負電,故硝基顯正電,根據上述定義可知硝基為吸電子基團。這種分析法適用於普遍基團的分析(當然也包括苯環),並且還可以用來幫助理解誘導效應、共軛效應、活化與鈍化等作用 。
電子效應
在大多數反應中,由於取代基(與氫原子相比)傾向於給電子或是吸電子,使分子某些部分的電子密度下降或上升,使反應分子在某個階段帶有正電荷(或部分正電荷)或負電荷(或部分負電荷)的效應。
電子效應是在總結大量實驗事實的基礎上提出的用來解釋化學現象的一種理論。電子效應包括 誘導效應(Inductive effect)和共軛效應(Conjugative effect)兩種,誘導效應是建立在定域鍵基礎上、短程的電子效應;而共軛效應是建立在離域鍵的基礎上、遠程的電子效應,在有機化合物中,往往兩種效應同時存在。
(1) 誘導效應(Inductive effect)
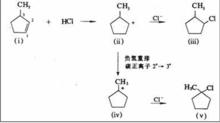 吸電子基團
吸電子基團誘導效應是電子效應的一種,用符號I表示。我們以C—H鍵中的H作為比較標準,有下列情況:X是一個電負性大於H的基團,當X取代H後C-X鍵的電子云偏向X,X稱為吸電子基團。Y是一個電負性小於H的基團,稱為供電子基團。無論是X還是Y取代了H以後,都將使鍵的極性發生變化,整個分子的電子云密度分布也將隨之而發生一定程度的改變,這種改變在靠近X或Y的地方表現最強烈,通過靜電誘導作用沿著分子鏈由近及遠地傳遞下去,並逐漸減弱,一般在三個碳原子以後基本消失。這種原子間的相互影響叫做誘導效應。吸電子基團引起的誘導效應叫做吸電子誘導效應(-I效應);斥電子基團引起的誘導效應叫做供電子誘導效應(+I效應)。
據實驗結果,一些取代基的吸、斥電子能力如下:位於H 前面的基團為吸電子基團;位於H 後面的基團為供電子基團。即吸電子基團使吸收峰向高頻方向移動,供電子基團使吸收峰向低頻方向移動。
與碳原子直接相連的原子,如同一族的隨原子序數增加而吸電子誘導效應降低,同一周期的自左到右吸電子誘導效應增強。
-F>-Cl>-Br>-I,-OR>SR,-F>-OR>-NR>-CR
與碳原子直接相連的基團不飽和程度越大,吸電子能力越強。
帶正電荷的基團具有吸電子誘導效應,帶負電荷的基團具有給電子的誘導效應。
烷基有給電子的誘導效應,同時又有給電子的超共軛效應。
(2)共軛效應
單雙鍵交替出現的體系稱為共軛效應。在共軛體系中,由於原子間的相互影響而使體系內的π電子(或P電子)分布發生變化的一種電子效應稱為共軛效應。
凡共軛體系上的取代基能降低體系的π電子云密度,則這些基團有吸電子的共軛效應。
凡共軛體系上的取代基能增高共軛體系的π電子云密度,則這些基團有給電子的共軛效應。
電子效應影響
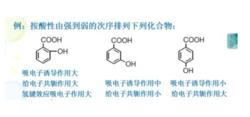 吸電子基團
吸電子基團當鹵代苯中鹵素的鄰、對位有強吸電子基團時,容易發生親核取代反應,為取代苯酚的製備提供了理論基礎。
酚羥基的鄰、對位連有供電子基團時,將使其酸性降低,供電子基團數目越多,酸性越弱。相反,酚羥基的鄰、對位連有吸電子基團時,將使其酸性增加,吸電子基團數目越多,酸性越強。當吸電子基團處於間位時,由於它們之間只存在誘導效應的影響,而不存在共軛效應,故酸性的增加並不明顯。
二芳基醚的製備比較困難,由於芳鹵難與親核試劑反應;但當鹵原子的鄰、對位有強吸電子基團時,反應則易於發生。