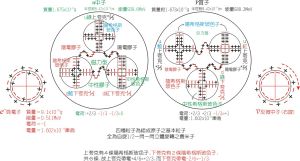
 原子核(含中子,質子)及電子-內部結構模型圖
原子核(含中子,質子)及電子-內部結構模型圖原子軌道的種類
主頁面:原子軌道
作為薛丁格方程的解,原子軌道的種類取決於主量子數(n)、角量子數(l)和磁量子數(m)。其中,主量子數就相當於電子層,角量子數相當於亞層,而磁量子數決定了原子軌道的伸展方向。另外,每個原子軌道里都可以填充兩個電子,所以對於電子,需要再加一個自旋量子數(ms),一共四個量子數。
n可以取任意正整數。在n取一定值時,l可以取小於n的自然數,ml可以取±l。不論什麼軌道,ms都只能取±1/2,兩個電子自旋相反。因此,s軌道(l=0)上只能填充2個電子,p軌道(l=1)上能填充6個,一個亞層填充的電子數為4l+2。
具有角量子數0、1、2、3的軌道分別叫做s軌道、p軌道、d軌道、f軌道。之後的軌道名稱,按字母順序排列,如l=4時叫g軌道。
排布的規則
電子的排布遵循以下三個規則:
能量最低原理
整個體系的能量越低越好。一般來說,新填入的電子都是填在能量最低的空軌道上的。
Hund規則
電子儘可能的占據不同軌道,自旋方向相同。
Pauli不相容原理
在同一體系中,沒有兩個電子的四個量子數是完全相同的。
同一亞層中的各個軌道是簡併的,所以電子一般都是先填滿能量較低的亞層,再填能量稍高一點的亞層。各亞層之間有能級交錯現象:
1s
2s 2p
3s 3p
4s 3d 4p
5s 4d 5p
6s 4f 5d 6p
7s 5f 6d 7P
8s 5g 6f 7d 8p
...
有幾個原子的排布不完全遵守上面的規則,如:
Cr:[ Ar ]3d54s1
這是因為同一亞層中,全充滿、半充滿、全空的狀態是最穩定的。這種方式的整體能量比3d44s2要低,因為所有亞層均處於穩定狀態。
排布示例
以鉻為例:
鉻原子核外有24個電子,可以填滿1s至4s所有的軌道,還剩餘4個填入3d軌道:
1s22s22p63s23p64s23d4
由於半充滿更穩定,排布發生變化:
1s22s22p63s23p64s13d5
除了6個價電子之外,其餘的電子一般不發生化學反應,於是簡寫為:
[Ar]4s13d5
這裡,具有氬的電子構型的那18個電子稱為“原子實”。一般把主量子數小的寫在前面:
[Ar]3d54s1
電子構型對性質的影響
主頁面:元素周期律
電子的排布情況,即電子構型,是元素性質的決定性因素。
為了達到全充滿、半充滿、全空的穩定狀態,不同的原子選擇不同的方式。具有同樣價電子構型的原子,理論上得或失電子的趨勢是相同的,這就是同一族元素性質相近的原因;同一族元素中,由於周期越高,價電子的能量就越高,就越容易失去。
元素周期表中的區塊是根據價電子構型的顯著區別劃分的。不同區的元素性質差別同樣顯著:如s區元素只能形成簡單的離子,而d區的過渡金屬可以形成配合物。
