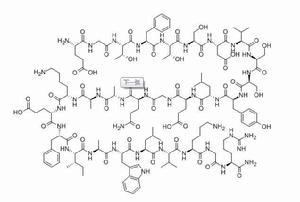
物質結構
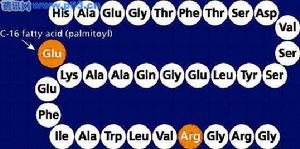 GLP-1(7-37)的胺基酸序列
GLP-1(7-37)的胺基酸序列人胰高糖素樣肽-1(GLP-1)類似物,又稱腸促胰高素樣肽1類似物, 與天然GLP-1分子結構相比有一個胺基酸差異,並增加了一個16碳棕櫚醯脂肪酸側鏈,與天然人GLP-1有95%同源性。並且由於脂肪酸側鏈的存在,其分子不易被DPP-IV降解,並能與白蛋白結合因而有較高的代謝穩定性,t1/2長達12-14小時。
分子式
C151H228N40O47分子量
3355.7
藥物類型
研製出的具有同樣生物學活性的GLP-1類似物有以下數類。
一、對GLP-1結構進行修飾的類似物丹麥諾和諾德製藥公司研究開發的GLP—1類似物NN221l屬於此類,其結構上的特點為將GLP—l第20位的賴氨酸換成谷氨酸,並在此谷氨酸殘基處接上1分子十六脘酸:棕櫚醯(軟脂醯),這一結構上的變化使NN221l與白蛋白相結合,可保護其免被DPP—Ⅳ迅速降解,延緩在吸收處的吸收,並可不被腎臟排泄,從而使其於人的血漿半衰期達到約12min。於2型糖尿病患者,注射1次,可維持]2h降糖效果。
二、天然的GLP·1類似物:艾桑丁—4(excendin-4)艾桑丁—4為一天然的GLP-1類似物,是由一種蜥蜴(gilamonsterlizard)唾腺所分泌毒液中提出的39肽,與GLP-1的胺基酸序列呈53%同源性,此物可與GLPd受體結合,為一完全的受體激活物,由於其第2位為甘氨酸而不似GLP-1為丙氨酸,能免受DPP—Ⅳ迅速降解,故其皮下注射後的效果可持續數小時,不像GLP-1需持續靜脈滴注方能奏效。
三、DPP·Ⅳ的抑制物已研製出數種DPP—Ⅳ抑制物,此酶被抑制後,內生的或外源性GLP—1的降解明顯延緩,生物活性延長,可達到類似套用GLP-1的效果。如瑞士諾華製藥公司研製的NVP-DP728是一種口服有效的選擇性DPP—Ⅳ抑制劑,其他還有纈氨酸吡咯(valinepyr—rolide),以及代號為P32/98的DPP—Ⅳ抑制劑。
生物效應
GLP—l有多種生物學效應,而這些作用都有利於用來治療2型糖尿病。
一、GLP-1促進胰島素的分泌及生物合成GLP—l具促胰島素分泌的效應,而且這一作用是葡萄糖依賴性的,效應的強弱與血糖濃度的高低有關,血糖愈高,作用愈強,血糖下降時減弱,血糖低至3.36mmol/L時不再有刺激胰島素分泌的作用。由於這一特點,可避免引起嚴重低血糖。GLP—1在胰島B細胞上有特異性的受體,此受體的基因被定位於第6號染色體。當GLP—1與其受體結合後,與受體偶聯的G蛋白即被激活,繼而G蛋白。亞基使腺苷酸環化酶活化,於是B細胞內cAMP濃度升高,依賴cAMP的蛋白激酶A(PKA)被激活,PKA使葡萄糖信號轉導途徑中一些起關鍵作用的蛋白質磷酸化而促使胰島素分泌,包括對A丁P敏感的鉀離子通道,電壓依賴性的鈣離子通道,以及與胰島素釋放機制相關的分子。GLP—l不僅促使胰島素釋放,還促進胰島素的生物合成。從胰島素基因轉錄到胰島素生物合成的多個步驟皆受到興奮,從而可保證胰島素的供應以備分泌之需。GLP—1能上調與胰島素分泌機制有關組成分子的基因轉錄。。PKA可使一種稱為CRE結合蛋白(CREB)的核轉錄因子磷酸化並活化,繼而CREB與胰島素原基因啟動子區的一個關鍵性的DNA序列:cAMP反應元件(cAMPresponseelement,CRE)結合,從而加強胰島素原基因轉錄的效率。
二、GLP-1可增加胰島B細胞的數量GLP—l可促使B細胞增生,還能促使胰管上皮細胞的前體細胞(progenitorcells)分化成新的B細胞,使糖耐量下降的老年大鼠胰腺內分泌細胞的數量增加。GLP—1及excendin-4已被證明可通過兩種機制增加B細胞量,前體細胞的分化/新生及已存在B細胞的凋亡減少。Movassat等研究了excendin-4對人胚胎胰腺類胰島細胞簇(ⅡCCs)中未分化前體細胞分化成B細胞的效果。將excendin-4加入培養中的ICCs可刺激PDXl的表達但不能刺激胰島素的表達。如將人ICCs移植至無胸腺大鼠腎包膜下,每日給大鼠腹腔注射excendin-4,連用lo日,8周后在葡萄糖刺激下,血中可測到人C肽,而於注射鹽水的對照大鼠,C肽無變化。於excendin-4處理的大鼠,腎包膜下移植物的組織學檢查也顯示與對照動物相比,含胰島素的細胞多3倍。此研究說明在體內ex—cendin-4可引起B細胞的分化,而在體外條件下只能上調PDXl的表達,提示excendin-4促進B細胞的分化及功能還需要其他旁分泌/內分泌因素。
三、CLP-l抑制胰升糖素的分泌GLP—l不僅促胰島素釋放,還抑制胰高糖素分泌,這種作用可為直接的,作用於胰島A細胞,或是間接的,通過興奮B細胞分泌胰島素,後者以旁分泌方式抑制A細咆分泌胰升糖素。於B細胞功能已衰竭,C肽反應已消失的1型糖尿病患者,GLP-1可使肝糖輸出減少,空腹血糖下降,此主要由於抑制了胰高糖素的分泌。
四、抑制食慾及攝食於正常人、肥胖者及肥胖的2型糖尿病患者,已證實GLP—1和另一種B細胞分泌的多肽:胰淀素(amylin)相仿,對食慾和攝食有抑制作用,這一效應對肥胖的2型糖尿病患者也是有益的。GLP—l作歷於下丘腦促進飽感的機制可有兩條途徑:①神經性,進食引起迷走神經活動增強,刺激位於下丘腦的迷走神經核的受體。②體液性,迴腸及結腸的L細胞將GLP—1分泌入血循環,通過脈絡膜叢被攝取而達到下丘腦。
五、延緩胃內容物排空作用GLP—l抑制胃腸的分泌功能及動力,延緩胃內容物的排空?這一作用對糖尿病患者也有益,胃排空速率減慢可減輕餐後高血糖。
六、GLP-1的擬胰島素作用一些離體試驗顯示GLP-1於脂肪細胞可刺激脂肪生成,而於肌細胞及肝細胞可刺激糖原生成,這些作用是否通過GLP-1受體實現的尚不肯定,有報導在肌肉、脂肪組織、肝中鑑定到GLP-1受體,也有人持否定意見。GLP-1是否具擬胰島素作用尚有待進一步明確。
適應症狀
用於治療2型糖尿病。
治療效果
GLP-1類似物如利拉魯肽,主要通過以下途徑改善2型糖尿病患者的代謝紊亂:
①葡萄糖濃度依賴性促胰島素分泌;
②抑制餐後胰高血糖素的分泌,減少肝糖的釋放;
③增強胰島素的敏感性;
④減慢胃的排空;
⑤抑制食慾。
此外,GLP-1的促胰島素分泌和抑制胰高血糖素分泌作用具有血糖濃度依賴性,當血糖濃度恢復正常時。GLP-1的促胰島素分泌作用減弱,因此,長期接受外源性GLP-1治療,不會引起低血糖的發生。
臨床
儘管GLP-1具有多種治療T2DM的有益機制,將其作為藥物用於臨床,長期以來卻有難度。GLP-1進入人體後,可被廣泛存在的二肽基肽酶-4(DPP-4)快速降解,半衰期僅為1~2分鐘。因此,如使用天然GLP-1治療T2DM,只有持續輸注才能將其濃度保持在有效水平。而對於T2DM這種慢性疾病的治療,持續輸注的用藥方式無疑會限制GLP-1的套用。
為使GLP-1套用於臨床,有兩種思路是可行的:對GLP-1進行結構修飾,使其不易被DPP-4降解;或是抑制DPP-4,延緩內源性GLP-1的降解使其水平升高。GLP-1類似物和DPP-4抑制劑這兩個類別均已有藥物獲得FDA審批用於治療T2DM,並顯示出較好的安全性和降糖療效。
從臨床數據看,GLP-1類似物升高GLP-1水平、降低HbA1c和餐後血糖的效果很可能優於DPP-4抑制劑,並可較DPP-4抑制劑更有效地發揮延遲胃排空、減少熱量攝入和改善胰島功能等作用。
DPP-4不僅可降解GLP-1,還可降解包括GIP在內的多種肽類。套用DPP-4抑制劑後,GLP-1、GIP等多種受DPP-4降解的多肽水平均可升高。如前所述,GIP不具備降低胰高血糖素分泌、抑制攝食和胃排空等GLP-1所具備的功能。此外,在T2DM患者中並未觀察到GIP缺乏,但發現了類似於GIP抵抗的狀況,使GIP作用減弱。因此DPP-4抑制劑升高GIP的作用對T2DM並無明顯的治療價值。其他受DPP-4降解的肽類水平升高后產生的作用尚待研究。而GLP-1類似物可較DPP-4抑制劑更加強效、特異地升高GLP-1水平,更充分地發揮降糖作用。