臨床意義
 高密度脂蛋白
高密度脂蛋白高密度脂蛋白在生理上起著將肝外組織的膽固醇運送到肝臟的運載工具的作用,
因而可以防止游離膽固醇在肝外組織細胞上的沉積。高密度脂蛋白膽固醇對冠心病的臨床診斷是一個重要的參考指標。它的升高是臨床冠心病保護因子之一,並能防治和延緩動脈粥樣硬化的發展。
血清高密度脂蛋白膽固醇的降低,預示著冠心病的出現。臨床上常同時測定高密度脂蛋白和血清總膽固醇,並根據它們的比值作為冠心病的信息指標。
代謝理論
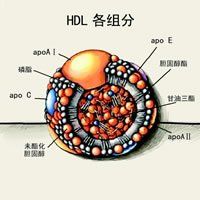 高密度脂蛋白
高密度脂蛋白早在1975年,國外一些醫學雜誌上,發表了一篇豆腐塊式的文章,小小的篇幅里記錄了一個科研成果——“美國的Miller博士發現了抗動脈硬化因子HDL的功能和作用機理”,文章中說:Miller博士和他的研究小組,發現了八例患者血脂水平都在正常範圍,卻患上了嚴重的冠心病(冠心病是心腦血管疾病的代表性疾病);同時又發現,這八例冠心病患者都有HDL偏低的特點。在當時,這例文章並沒有引起人們過多的重視,但從現代的角度來看,這簡直就是一個爆炸式的新聞,因為它說明了冠心病並不都是由高血脂引發,HDL水平的降低也可能是冠心病的一個重要的甚至是關鍵性的發病原因。並且有可能從此人們就會找到一條解決冠心病、解決心腦血管疾病的根本途徑。統治血脂代謝理論界幾十載的“脂質浸潤學說”,受到了嚴厲的挑戰。
 高密度脂蛋白
高密度脂蛋白一直到1985年,美國的麥可·布朗和約瑟夫·里歐納德·戈爾茨坦教授以全新的角度闡述了脂蛋白代謝的機理:人體血液中固有的一種載脂蛋白—高密度脂蛋白(HDL)能夠驅動膽固醇逆轉運,通過逆轉運作用把血液和組織中多餘的膽固醇等“血液垃圾”攜帶經肝臟分解逆向排除體外,同時HDL具有逆轉內皮功能不良、刺激前列環素生成(它具有擴血管和抗血栓形成作用)、抑制內皮細胞凋亡、減少血小板聚集、抑制LDL氧化等許多功能。這一理論奠定了脂蛋白代謝的理論基礎,HDL在生理機體內的重要性,又被提到了非常重
要的地位。尤其是由於這兩位博士的突出貢獻,被授予當年的諾貝爾醫學大獎,理論下面深層的科學奧妙和光彩四射的社會榮譽,頓時吸引了眾多的人,各種各樣的研究幾乎同時在世界各大洲開展了起來,HDL儼然成了珠穆朗瑪峰頂的一顆璀璨的明珠。
HDL代謝理論的發現,就是世界醫學史上的一顆核子彈,他的爆炸力和衝擊波,波及了幾十年,很多人一輩子為此嘔心瀝血,因為大家都清楚地知道——誰能大幅度升高HDL,誰就解決了冠心病甚至是整個心腦血管疾病的問題,誰就能把人類的壽命從理論上延長几十年。
正常比值
總膽固醇低而高密度脂蛋白高對健康有利,那么是不是總膽固醇越低越好而高密度脂蛋白越高越好呢?不是的。總膽固醇與高密度脂蛋白的比值男性最好小於4.5,女性最好小於3.5;即對成年男性來說,高密度脂蛋白應在1.2毫摩爾/升(45毫克/分升)以上,成年女性在1.4毫摩爾/升(55毫克/分升)以上。如一位男性,總膽固醇為5.2毫摩爾/升(200毫克/分升),那么他的高密度脂蛋白最低應是1.0毫摩爾/升(40毫克/分升),最好在1.2毫摩爾/升(45毫克/分升)以上;如果總膽固醇與高密度脂蛋白比值大於5,其患動脈粥樣硬化和冠心病的可能性就增加了。是否總膽固醇低,就能保證不發生冠心病呢?答案是否定的。我們曾收治過一位急性心肌梗死患者,其總膽固醇值僅4.4毫摩爾/升(168毫克/分升),但高密度脂蛋白比值為6.7,遠遠高於正常值5。
那么是不是高密度脂蛋白水平高,就保證不發生冠心病呢?也不是。例如有一位男性冠心病患者,其高密度脂蛋白為1.4毫摩爾/升(55毫克/分升),高於正常值,但他的總膽固醇為9.9毫摩爾/升(380毫克/分升)其總膽固醇與高密度脂蛋白比值為6.9。故單純高密度脂蛋白水平高,也不能保證不發生心臟病。由此可見,總膽固醇與高密度脂蛋白比值正常其重要。一些動物,如海豚,它的高密度脂蛋白達20.8毫摩爾/升(800毫克/分升),占總膽固醇的90%,它極少患動脈硬化。故總膽固醇與高密度脂蛋白的比值越低,心腦血管系統就越健康。
研究進展
高密度脂蛋白(highdensitylipoprotein,HDL)具有抗動脈粥樣硬化的作用[,血漿高密度脂蛋白膽固醇濃度降低是冠心病的危險因素。因此,有關HDL的研究日益成為人們關注的一個熱點。套用序列免疫親合層析技術,根據載脂蛋白的不同,可將正常人血漿HDL分為僅含載脂蛋白AI的HDL(稱為脂蛋白AI,LipoproteinAI,LPAI)及同時含載脂蛋白AI和載脂蛋白AII的HDL(脂蛋白AI:AII,LipoproteinAI:AII,LPAI:AII)兩個主要類別(後來又分離出脂蛋白AIV及脂蛋白AI:AIV)。非變性梯度凝膠電泳結果表明:LPAI和LPAI:AII都包括小、中和大HDL顆粒。這些亞類具有各自的代謝、功能和臨床意義。對HDL的代謝進行了深入的研究,並取得了新的認識。
1、大、小高密度脂蛋白顆粒代謝Colvin等[4-5]在非人靈長類猴實驗中第一次揭示HDL代謝過程中大顆粒HDL並沒有轉變為中或小顆粒HDL(包括β極低密度脂蛋白),小顆粒HDL僅單向轉化為較大的顆粒HDL(中、大顆粒HDL),所有中、大顆粒HDL均來源於小顆粒HDL。研究顯示:在成熟過程中較大顆粒HDL中的載脂蛋白AI除來源於小顆粒HDL外,還可以通過肝臟合成獲得。大顆粒HDL中載脂蛋白AI的濃度主要取決於載脂蛋白AI產生速率而非分解速率。這些結果提示,HDL是代謝穩定的成熟顆粒,較大的HDL是HDL亞類代謝通路的終產物,它可直接從血漿中移除。另外研究還提示小顆粒HDL的轉化發生在非循環池內(外周血管邊緣,血管內皮孔隙通路和動脈內膜下等)。在這裡,小HDL與細胞膜脂質或膜蛋白(如清道夫受體BI)相互作用,由此通過液相擴散或與膜受體的直接結合,從細胞表面直接獲得游離膽固醇。無或貧脂質的載脂蛋白AI也可以與外周細胞膜脂質或受體相互作用,使細胞膜脂質發生微溶解並形成可與小HDL融合的新生HDL。這些發生在循環外的過程導致小HDL向較大HDL轉化,然後返回血循環內。另外,離體孵育研究顯示:HDL亞類之間沒有觀察到有意義的載脂蛋白AI交換。表明體內參與轉化的一些基本組分在僅僅模擬血清的體外孵育研究中是缺乏的,進一步支持前述體內轉化並非在循環血漿內。小顆粒HDL單向轉化為較大HDL有利於組織細胞脂質的輸出。小顆粒HDL在血管內外的穿梭,一方面完成了自身的轉變,另一方面啟動了膽固醇的逆轉運。
2、含載脂蛋白AI或/和載脂蛋白AII的高密度脂蛋白代謝一般認為LPAI比LPAI:AII具有更強的抗動脈粥樣硬化作用,而其中大LPAI對冠心病發生的危險更具預測價值[9-10]。早年,Rader等報導,LPAI中的載脂蛋白AI分解速率快於LPAI:AII的載脂蛋白AI,但實驗過程中示蹤子經受了超速離心處理,不能區分HDL亞類。Lamarche[等對健康禁食者和經過5小時靜滴合成甘油三酯乳劑的個體進行研究,結果發現靜注乳劑造成血漿HDL中甘油三酯增加2倍,磷脂增加25%,而HDL顆粒大小沒有變化。富含甘油三酯的HDL比禁食者HDL清除更迅速。進一步研究顯示:富含甘油三酯的LPAI部分分解速率快于禁食者LPAI。富含甘油三酯的LPAI:AII部分分解速率與禁食者相比,沒有統計學差異。實驗首次表明富含甘油三酯的HDL促進了血漿載脂蛋白AI的代謝清除。臨床上觀察到高甘油三酯血症患者往往伴有低血漿高密度脂蛋白膽固醇,可能與此有關。有學者在獼猴體內通過脂蛋白脂酶抑制劑誘導富含甘油三酯的HDL,同樣發現其載脂蛋白的部分分解速率成倍增加。在Lamanche研究中,靜滴乳劑後使HDL顆粒表面富含多不飽和脂肪酸磷脂(來自甘油三酯乳劑中的大豆油磷脂)引起HDL載脂蛋白AI不穩定和構形變化。這為上述部分分解速率的差異提供了一種解釋。已證實含有多不飽和脂肪酸的重組HDL顆粒中載脂蛋白AI對鹽酸胍變性穩定性較差,且apoAI構形發生變化。Tilly-Kiesi等觀察到LPAI和LPAI:AII中載脂蛋白AI存留時間相近。絕經後婦女血漿中總載脂蛋白AI分泌率較高,LPAI及LPAI:AII的載脂蛋白AI分泌率之間的差異接近統計學意義,而其清除率基本相似。很顯然,血漿HDL-C濃度增加是由於載脂蛋白AI產生的增多。這與Colvin等的結果相符合。前已述及,小顆粒HDL單向轉變為較大顆粒HDL。但在HDL動力學研究還顯示,注入體內放射性標記的小或大LPAI有40%轉變為LPAI:LPAII,尚不清楚這是否為LPAI獲得了載脂蛋白AII分子的結果。不過卻提示HDL亞類在另一個水平的代謝複雜性,有待於進一步探討。
3、高密度脂蛋白膽固醇的轉運,通常認為HDL保護心血管的作用在於維持肝外組織的膽固醇平衡。通過膽固醇的逆轉運,防止外周組織過多脂質的蓄積。現在還沒有實驗方法能直接追蹤多餘膽固醇從外周組織特別是從血管內膜到肝的轉運過程。近來,Jolley在載脂蛋白AI敲除鼠的研究中發現無論膽固醇的合成、LDL的攝取或外周組織膽固醇濃度實驗組與對照組沒有差異。作者推論逆向膽固醇轉運也沒有差別。這些結果表明外周組織細胞膽固醇淨平衡並非由血漿高密度脂蛋白膽固醇和載脂蛋白AI濃度調節,很可能由細胞內的過程控制。通過轉基因鼠過度表達膽固醇酯轉運蛋白降低血漿高密度脂蛋白膽固醇(59mg/dl到15mg/dl),結果也顯示膽固醇的逆轉運並不依賴於其濃度(至少在鼠)。相似地,在兔體內卵磷脂-膽固醇醯基轉移酶的過表達使血血漿高密度脂蛋白膽固醇的濃度增加四倍(28mg/dl到121mg/dl),但通過血漿的載脂蛋白AI淨流出基本保持不變(8.1±0.6mg/天/公斤體重比10.8±1.4mg/天/公斤體重)。可見血漿高密度脂蛋白膽固醇濃度對膽固醇的逆轉運似乎沒有影響。這是否可以推測是其他的機制代替了降低的HDL作用?抑或HDL抗動脈粥樣硬化益處更在於它的抗氧化等其他作用?Spady等套用載脂蛋白AI-/-鼠觀察到即使HDL異常低下,在任何組織高密度脂蛋白膽固醇酯轉運活性和清道夫受體BI的mRNA都沒有發生上調。已知到清道夫受體BI可介導高密度脂蛋白膽固醇酯的選擇性攝取和流出。這表明高密度脂蛋白膽固醇酯的某些代謝調節機制並不受血漿HDL降低的影響。在另一實驗中,Plump等認為載脂蛋白AI敲除鼠並無外周組織膽固醇積聚和動脈粥樣硬化很可能由於高密度脂蛋白膽固醇酯輸送到組織的減少與極低密度脂蛋白、中間密度脂蛋白等血漿非高密度脂蛋白膽固醇的減低。而Morrtti等發現:膽固醇酯轉移蛋白過度表達降低高密度脂蛋白膽固醇,將導致高膽固醇飲食鼠更嚴重的動脈粥樣硬化。可以認為,這些結果的差異不僅與HDL有關,而且與包括血漿非高密度脂蛋白膽固醇的變化等因素有關。另有學者認為血漿高密度脂蛋白膽固醇改善動脈粥樣斑塊的分子機制不同於肝外組織細胞內維持生理性膽固醇平衡的那些特殊步驟。把這兩個過程聯繫起來統稱為“膽固醇逆轉運”是不適當的。人和鼠脂蛋白存在一些差異:小鼠缺乏膽固醇脂轉移蛋白,鼠和人載脂蛋白AII生理特性亦不同,造成載脂蛋白AI缺陷鼠比載脂蛋白AI缺陷的人具有更高的血漿高密度脂蛋白膽固醇水平。載脂蛋白AI缺陷鼠血漿極低密度脂蛋白、中間密度脂蛋白膽固醇等減少,很可能是由於膽固醇以高密度脂蛋白膽固醇酯形式輸送至肝臟減少有關。對於人體來說,血漿高密度脂蛋白膽固醇與甘油三酯水平呈強負相關。因此在載脂蛋白AI缺陷鼠模型,低高密度脂蛋白膽固醇創造了一個已被減少的膽固醇轉運至外周組織和肝臟的新平衡。
4、影響高密度脂蛋白代謝的酶和蛋白類,已知卵磷脂-膽固醇醯基轉移酶促進膽固醇的酯化並轉入HDL顆粒的核心,膽固醇脂轉移蛋白促進極低密度脂蛋白的甘油三酯轉移到HDL,因而加速了HDL的成熟和代謝。肝臟甘油三酯脂酶(肝脂酶)可催化水解富甘油三酯的脂蛋白。近來發現在清道夫受體BI介導的高密度脂蛋白膽固醇酯選擇性攝取過程中,肝脂酶是主要的調節因素。正常男性個體HDL亞組份分布的特異性差異與肝脂酶活性正常變異有關,高肝脂酶活性導致HDL2b和HDL2a濃度減少,而肝脂酶活性的變異對最小HDL(HDL3b和HDL3c)濃度沒有影響。Ehnholm等報導磷脂轉移蛋白促進HDL重塑形成大的顆粒和載脂蛋白AI-磷脂複合物,大HDL可被肝臟直接清除,小載脂蛋白AI-磷脂複合物可滲透到間質作為膽固醇逆轉運過程中外周細胞膜膽固醇接受體。因此,磷脂轉移蛋白在HDL代謝中處於中心角色。還有學者發現它能引起HDL載脂蛋白AI的蛋白水解清除。小鼠磷脂轉移蛋白是HDL水平和大小的決定因素。在體和離體實驗證據表明調節HDL顆粒大小和濃度是磷脂轉移蛋白關鍵的生理功能。最近Jay等報導了一種內皮源性脂酶(內皮脂酶),屬於甘油三酯脂酶家族,在肝、肺、腎和胎盤中表達。內皮脂酶具有很高的磷脂酶活性和較低甘油三酯脂酶活性。小鼠體內內皮脂酶過量表達減少血漿HDL-C和載脂蛋白AI濃度,在脂蛋白代謝和血管生物學方面具有獨特作用。
綜上所述,HDL亞類之間的相互關係、複雜的代謝機制及其在膽固醇逆轉運過程的整和尚待確定。血漿HDL-C濃度的差異源於載脂蛋白A-I的生產,而對調節載脂蛋白A-I產生的遺傳和環境因素(如富集甘油三酯)了解較少。關於增加HDL分解速率的因素還未闡明。LPAI和LPAI:AII代謝相關性仍不清楚。在組織膽固醇蓄積變化的情況下,多餘膽固醇的轉運與HDL亞類代謝的相關性仍需要進一步研究。
