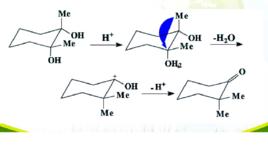
定義
頻哪醇在酸的作用下,發生重排,脫去一分子水,生成頻哪醇。
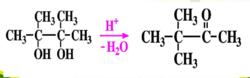 頻哪醇重排反應
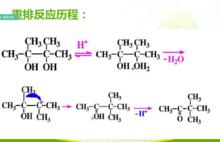
頻哪醇重排反應機理
反應時,頻哪醇在酸性條件下與一個質子結合得到質子化醇,質子化醇隨後脫水生成碳正離子,含碳正離子的中間產物發生重排,生成不對稱的質子化酮,該質子化酮脫去質子,生成重排產物。
一般而言,基團重排的能力為:芳基>烴基>氫,但有時氫原子的遷移會比烴基更快。
 頻哪醇重排反應
頻哪醇重排反應反應特點
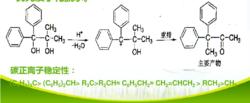
(1)在不對稱取代的乙二醇中,一般能夠形成相對穩定碳正離子的碳上的羥基(兩個羥基中電子云密度大)優先質子化脫水。
 頻哪醇重排反應
頻哪醇重排反應(2)如果形成的碳正離子的相鄰兩個碳上的基團不同,通常是供電子能力強的基團優先遷移。重排時遷移基團的先後次序為,供電子芳基>苯基>烷基。
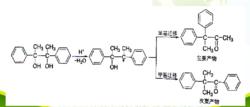 頻哪醇重排反應
頻哪醇重排反應(3)遷移過程的立體化學是反式共平面遷移,即遷移基團與離去基團需要處於反面位置。
 頻哪醇重排反應
頻哪醇重排反應重要套用
可用於環的縮小,擴大,以及螺環化合物的形成:
 頻哪醇重排反應
頻哪醇重排反應知識擴展
半頻哪醇重排:α-碳原子上面有雜原子取代基(如鹵素,氨基,-SR等)的醇的重排反應。半頻哪醇重排選擇性更強,反應條件更溫和。
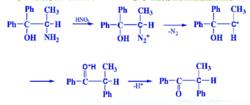 頻哪醇重排反應
頻哪醇重排反應霍夫曼降解反應(又名霍夫曼重排,Hofmann rearrangement)指的是醯胺與次氯酸鈉或次溴酸鈉的鹼溶液作用時,脫去羰基生成少一個碳的伯胺反應:R-CONH₂ + NaOX + 2NaOH——→R-NH₂ +Na₂CO₃+ NaX +H₂O。由於在反應及過程中由於發生了親核重排,所以又稱為霍夫曼重排反應,具有光學活性的基團在重排後構型不變。
柯提斯重排反應( Curtius rearrangement)是一類親核重排反應,反應中,羧酸與疊氮化物作用生成醯基疊氮化物再重排為異氰酸酯,異氰酸酯水解得到少一碳的伯胺,該反應可用於幾乎所有羧酸,是製備伯胺的方法之一。
施密特重排反應( Schmidt rearangement)指的是疊氮酸和羧酸在路易斯酸或硫酸的催化下重排生成異氰酸酯並水解生成少一碳伯胺的反應。在實際操作中,疊氮酸有毒且極易爆炸,因此往往使用疊氮化鈉、硫酸和反應物在氯仿中進行反應,該反應的產率隨碳鏈的增長而增大,簡單的芳香族羧酸不太適用。
沃爾夫重排反應(Wolff rearrangement)指的是重氮酮在氧化銀或光照催化下重排生成烯酮的親核重排反應,重排過程中生成酮碳烯。沃爾夫重排反應生成的烯酮有很高的反應活性,可與水、醇、氨等反應生成對應的羧酸或羧酸衍生物。沃爾夫重排是阿恩特-艾斯特爾特反應( Arndt-Eistert reaction)的關鍵步驟。