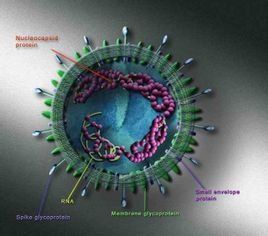
病毒確認
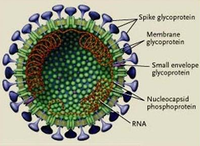 SARS病毒
SARS病毒世界衛生組織宣布,正式確認冠狀病毒的一個變種是引起非典型肺炎的病原體。科學家們說,變種冠狀病毒與流感病毒有親緣關係,但它非常獨特,以前從未在人類身上發現,科學家將其命名為"SARS病毒"(SARS是"非典"學名的英文縮寫)。1965年,醫學專家用人胚氣管培養方法,從普通感冒病人鼻洗液中分離出一株病毒,命名為B814病毒。隨後,Hamre等用人胚腎細胞分離到類似病毒,代表株命名為229E病毒。1967年,Mclntosh等用人胚氣管培養從感冒病人中分離到一批病毒,其代表株是OC43株。1968年,Almeida等對這些病毒進行了形態學研究,電子顯微鏡觀察發現,這些病毒的包膜上有形狀類似日冕的棘突,故提出命名這類病毒為冠狀病毒。
香港衛生專家排除了它與甲型流感和乙型流感病毒有關的可能性,與1997年出現的H5N1禽流感病毒也沒有聯繫。國家曾於1975年正式命名了冠狀病毒科。據香港衛生官員說,非典型肺炎通常由病毒引起,例如流感病毒、腺病毒和其他呼吸道病毒,非典型肺炎也可能由生物體引起。冠狀病毒感染在全世界非常普遍,人群中普遍冠狀病毒抗體,成年人高於兒童。各國報導的人群抗體陽性率不同,我國人群以往冠狀病毒抗體陽性率在30%至60%,前蘇聯的抗體陽性率則在53%至97%。
發現過程
2002年底,中國廣東等地出現了多例原因不明的、危及生命的呼吸系統疾病。隨後,越南,加拿大和香港等地也先後報導了類似病例。世界衛生組織將此類疾病命名為“嚴重急性呼吸道綜合症(SARS)” 。隨後世界各國的實驗室都致力於發現這種疾病的病原體。香港大學最先於2003年3月22日宣布分離出一種未知的冠狀病毒。隨後,有多個實驗室在NJEM、Lancet等國際知名醫學雜誌上發表了關於該病原體的研究論文。2003年4月12日加拿大BC腫瘤研究所基因組科學中心(BC Cancer Agency‘s Genome Sciences Center)首先完成了該病毒的全基因組測序。2003年4月16日,WHO在上述各方面研究成果的基礎上,正式宣布一種前所未知的冠狀病毒,為導致嚴重急性呼吸道綜合症(SARS)的病原體,並命名為SARS冠狀病毒(SARS Coronavirus,SARS-CoV)。
形態特徵
 SARS病毒
SARS病毒SARS病毒粒子呈不規則形狀,直徑約60-220mm。病毒粒子外包著脂肪膜,膜表面有三種糖蛋白:刺突糖蛋白(S,Spike Protein,是受體結合位點、溶細胞作用和主要抗原位點);小包膜糖蛋白(E,Envelope Protein,較小,與包膜結合的蛋白);膜糖蛋白(M,Membrane Protein,負責營養物質的跨膜運輸、新生病毒出芽釋放與病毒外包膜的形成)。少數種類還有血凝素糖蛋白(HE蛋白,Haemaglutinin-esterase)。
SARS病毒的核酸為非節段單鏈(+)RNA,長27-31kb,是RNA病毒中最長的RNA核酸鏈,具有正鏈RNA特有的重要結構特徵:即RNA鏈5’端有甲基化“帽子”,3’端有PolyA “尾巴”結構。這一結構與真核mRNA非常相似,也是其基因組RNA自身可以發揮翻譯模板作用的重要結構基礎,而省去了RNA-DNA-RNA的轉錄過程。SARS病毒的RNA和RNA之間重組率非常高,病毒出現變異正是由於這種高重組率。重組後,RNA序列發生了變化,由此核酸編碼的胺基酸序列也變了,胺基酸構成的蛋白質隨之發生變化,使其抗原性發生了變化。而抗原性發生變化的結果是導致原有疫苗失效,免疫失敗。
病毒周期
SARS病毒成熟粒子中,並不存在RNA病毒複製所需的RNA聚合酶(Viral RNA polymerase),它進入宿主細胞後,直接以病毒基因組RNA為翻譯模板,表達出病毒RNA聚合酶。再利用這個酶完成負鏈亞基因組RNA(sub-genomic RNA)的轉錄合成、各種結構蛋白mRNA的合成,以及病毒基因組RNA的複製。SARS病毒各個結構蛋白成熟的mRNA合成,不存在轉錄後的修飾剪下過程,而是直接通過RNA聚合酶和一些轉錄因子,以一種“不連續轉錄”(discontinuous transcription)的機制,通過識別特定的轉錄調控序列(transcription regulating sequences, TSR),有選擇性的從負義鏈RNA上,一次性轉錄得到構成一個成熟mRNA的全部組成部分。結構蛋白和基因組RNA複製完成後,將在宿主細胞內質網處裝配(assembly)生成新的冠狀病毒顆粒,並通過高爾基體分泌至細胞外,完成其生命周期。
流行病學
 電子顯微鏡下的SARS病毒
電子顯微鏡下的SARS病毒SARS病毒在世界各地極為普遍。大約有15種不同冠狀病毒被發現,能夠感染多種哺乳動物和鳥類,有些可使人發病。
SARS病毒引起的人類疾病主要是呼吸系統感染(包括嚴重急性呼吸綜合症)。該病毒對溫度很敏感,在33℃時生長良好,但35℃就使之受到抑制。由於這個特性,冬季和早春是該病毒疾病的流行季節。SARS病毒是成人普通感冒的主要病原之一,兒童感染率較高,主要是上呼吸道感染,一般很少波及下呼吸道。另外,還可引起嬰兒和新生兒急性腸胃炎,主要症狀是水樣大便、發熱、嘔吐,每天可拉10餘次,嚴重者甚至出現血水樣便,極少數情況下也引起神經系統綜合徵。
病毒的生長多位於上皮細胞內,也可以感染肝臟、腎、心臟和眼睛,在另外的一些細胞類型(例如巨噬細胞)中也能生長。如今人類冠狀病毒還沒有合適的可作研究用的動物模型(人類疾病的動物模型(animal model of human disease)是指各種醫學科學研究中建立的具有人類疾病模擬表現的動物。動物疾病模型主要用於實驗生理學、實驗病理學和實驗治療學(包括新藥篩選)研究),因此對冠狀病毒的分離工作難度很大,需用人肝臟細胞、氣管及鼻黏膜細胞,經器官培養才能分離得到。增殖病毒也要用上述材料,亦很困難。
SARS病毒的血清型和抗原變異性還不明確。SARS病毒可以發生重複感染,表明其存在有多種血清型(至少有4種已知)並有抗原的變異,其免疫較困難。
傳播途徑
SARS病毒通過呼吸道分泌物排出體外,經口液、噴嚏、接觸傳染,並通過空氣飛沫傳播,感染高峰在秋冬和早春。病毒對熱敏感,紫外線、來蘇水、0.1%過氧乙酸及1%克遼林等都可在短時間內將病毒殺死。
疾病預防
對SARS病毒預防有特異性預防,即針對性預防措施(疫苗,疫苗的研製是有可能的,但需要時間較長,解決病毒繁殖問題是其難題)和非特異性預防措施(即預防春季呼吸道傳染疾病的措施,如保暖、洗手、通風、勿過度疲勞及勿接觸病人,少去人多的公共場所等)。
疫苗研究
臨床疫苗
1. 套用黏膜疫苗和抑制性抗體進行免疫預防(基於對猴子所做的動物實驗模型)。
2. 對SARS疫苗的免疫可誘導產生針對冠狀病毒的抑制性抗體,表明黏膜免疫可引發系統免疫反應。動物實驗中,給予冠狀病毒後,對照組動物均有病毒傳播,而在接種過SARS疫苗的猴子中無一發病。
3. 研究者用抑制性人類單克隆抗體治療被SARS病毒感染的雪貂,顯著減少了病毒在肺部的複製,阻止肺部發展到典型病理階段,未見病毒在咽部分泌傳播。
4. 研究顯示動物模型中呼吸道黏膜免疫及免疫接種能有效預防SARS。
併發症
SARS病毒可能引起休克、心率紊亂或心功能不全、腎功能損害、肝功能損害、DIC(disseminated intravascular coagulation,即彌散性血管內凝血)、敗血症、消化道出血等。
傳染源
 SARS病毒
SARS病毒果子狸與SARS
在中國大陸尤其是南方,特別是在雲貴高原及兩廣(廣東、廣西)地區,常被用以食用,因此醫學界許多人士認為人類通過食用果子狸而感染到嚴重急性呼吸道綜合症(SARS“非典”[Severe Acute Respiratory Syndrome])。因為有不利的證據表明嚴重急性呼吸道綜合症(SARS)與果子狸關係密切,支持者如鍾南山。致使果子狸在中國部分地區遭到大規模的宰殺。但是也有人認為其證據不足以證明這一點。
如同瘋牛病、禽流感等傳染病一樣,人類通過大規模屠殺動物起到防止傳染疾病的方法在一定程度上遭到了保護動物人士的質疑。該物種已被列入國家林業局2000年8月1日發布的《國家保護的有益的或者有重要經濟、科學研究價值的陸生野生動物名錄》。
專家證實中華菊頭蝠是SARS病毒的源頭
中國科學院武漢病毒研究所研究員石正麗帶領的國際研究團隊分離到一株與SARS病毒高度同源的SARS樣冠狀病毒,進一步證實中華菊頭蝠是SARS病毒的源頭。
SARS冠狀病毒是造成2002年至2003年SARS暴發的病原。已有的流行病學證據和生物信息學分析顯示,野生動物市場上的果子狸是SARS冠狀病毒的直接來源。
雖然在世界各地的蝙蝠體內均發現與SARS病毒相似的SARS樣冠狀病毒,但這些病毒均不能利用人和果子狸的ACE2(即人SARS病毒受體)作為受體,不是SARS病毒的近親。該團隊分離的SARS樣冠狀病毒可以利用人、果子狸和中華菊頭蝠ACE2作為其功能受體,並且能感染人、豬、猴以及蝙蝠的多種細胞。這些實驗結果為中華菊頭蝠是SARS冠狀病毒的自然宿主提供了更為直接的證據。
預防措施
為預防SARS病毒傳染,養成良好的衛生習慣,勤洗手,勤洗臉,勤飲水,勤通風。患者耍戴口罩,調整好心態,加強身體鍛鍊。目前暫無特效藥治療。