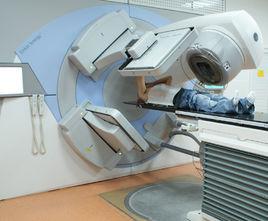
設計
1、正向計畫設計調強放療
在CT影像上勾畫好解剖輪廓後,三維適形放射治療是由計畫者根據靶區部位和大小在計畫系統上安排照射野的入射方向、大小、形數目並對各個輻射野分配權重然後由計算機系統進行劑量計算,算完後顯示射野分布,計畫者依據靶區及正常組織所受劑量來評估計畫的好壞。如果劑量分布不符合治療要求,再由計畫者改變射野的入射方向和權重,重新計算,如此反覆進行,直至滿意為止。這種制定計畫的方式叫做正向計畫設計。
2、調強放療多採用逆向計畫設計方案
調強概念是受了CT成像的逆原理啟發:當CT的X射線管發出強度均勻的X射線穿過人體後,其強度分布與組織厚度和組織密度的乘積成反比;那么我們不是可以先確定射線照到靶區及正常組織上產生的劑量分布,然後再由此推算出各個射野應該貢獻的束流強度嗎?根據調強的概念,首先要依據病變(靶區)與周圍重要器官和正常組織的三維解剖特點,以及期望的靶區劑量分布和危及器官(OAR)的劑量耐受極限,由計畫者輸入最佳化參數,通過計畫系統計算出各個射野方向上需要的強度分布。即在完成勾畫輪廓和確定輻射野數目及入射方向後,先確定對CT影像中各個興趣區的劑量要求。由計畫者以數學形式輸入這些臨床參數(即目標函式),如對靶區劑量範圍的要求,對相關危及器官劑量的限制等,然後由計算機通過數學的方法(如疊代法、模擬[font color=#000000]退火[/font]法、蒙特卡洛法等)自動進行最佳化,在經過幾百乃至上千次計算與比較後得出最接近目標函式並能夠實現的計畫方案。它是常規治療計畫設計的逆過程,所以叫做逆向計畫設計。
在患者影像獲取、勾畫輪廓和確定輻射野數目及方向這些步驟上兩者相同,但它們的最佳化過程是不同的。前者是先計算劑量,看結果如何,不行就人為地改動計畫再試,如此反覆,直到可以接受為止。後者是先由計畫者通過輸入目標函式來限定靶區和危及器官主劑量分布,再由計畫系統自動反覆進行最佳化計算,反覆的次數由病例的複雜程度決定,至少需要一二百次。
套用
調強放射治療中,把每一個輻射野分割成多個細小的野(也叫做線束)。在制定計畫時,按照靶區的三維形狀和與相關危及器官之間的解剖關係,對這些線束分配以不同的權重,使同一個射野內產生最佳化的、不均勻的強度分布,以便使通過危及器官的束流通量減少,而靶區其他部分的束流通量增大。
調強放射治療也不是萬能的,在制定調強計畫時幾乎總是有一些限度,有些度劑量分布(或劑量一體積組合)無法真正實現。例如,一個腦幹旁的腫瘤,假如要求給予腫瘤致死劑量而不許照射腦幹,即使用調強技術也是無法實現的。而且目前我們關於什麼是臨床最佳要求以及如何確定調強劑量目標的知識也有限。此外,由於數學公式的限制,或由於計算機速度及時時間的限制,我們往往找不到最好的結果。還有各種各樣的不確定性,例如,患者每天相關的治療位置、內解剖位置的變化、在治療期間器官的變形及各個分次之間的位移限制了調強的適用範圍和功效。傳輸裝置的劑量特性,如通過多葉光柵(MLC)葉片的散射和透射,也對調強放療的精度及可傳輸性產生某些限制。另外當前所用的劑量計算模式在精度上都有局限性,有可能在劑量計算上出現誤差。對某些部位,例如肝、肺部的腫瘤,因為他們受呼吸影響較大,位置移動較多,在實施調強時要格外小心。
在組織補量的調強放射治療中使用大分次劑量的結果可能會增大嵌在靶區內或緊鄰靶區的正常組織的損傷機會。調強放射治療的高度適形可能導致病變的地理遺漏(如擺位不準確)和復發,尤其對位置與運動不確定的病變影響更大。
這些局限性和風險表明,在現階段使用調強技術要格外小心,還要繼續研究改進技術並減少誤差,這樣的研究是調強技術全部潛力的根本。
方法
1、物理補償法
用於調強的補償器可以作為射野擋塊的一部分放在治療機擋塊托盤架上。由逆向計畫系統根據目標函式的要求計算出每個射野的強度分布形狀或被補償的組織厚度分布,並將數據輸出到PC機控制的補償器生成器,就可以製作補償器了。製作出來的補償器就可以進行調強補償用了。這種方法出現在用MLC進行調強以前,缺點是因為這種技術需要對每個射野都來製作補償器,費時費力效率低;治療時每個照射野都需要工作人員進治療室工作,擺位也不方便;補償器作為一種濾過器,也會影響原射線的能譜分布。
2)、用常規MLC進行多個固定野調強治療
加速器中的MLC最初設計目的主要是為了代替射野擋塊,隨著計算機技術的發展,MLC不僅能在鏇轉治療中調節射野形狀跟隨靶區,而且還可以在計算機控制下實現靜態調強和動態調強。
靜態和動態調強都是由逆向計畫系統先按照目標函式的要求通過最佳化計算得出射野的強度分布。目標函式參數是由計畫者根據具體病例的臨床要求輸入到計畫系統中的,在治療計畫被認可後,這些強度分布就被轉換為葉片位置序列檔案,然後傳送到加速器的MLC控制系統中,在治療時由調強控制系統控制葉片運動,實現這些調強分布。
雖然對三維適形而言,MLC的葉片寬度只影響了射野的形狀,但對調強而言,葉片寬度卻影響到整個層面上的劑量,所以MLC葉片寬度越小越好,但是葉片越薄,製作越困難,成本也就越高。目前國內的MLC一般只有30多對葉片,但國外,已經出現了100對葉片以上的MLC系統。
類型
靜態調強
靜態調強是由逆向調強計畫系統根據臨床數據將各個射野要求的強度分布進行分級,利用MLC將每個照射野分成若干個子野,,每個子野內的強度是均勻的。
最佳化計算賦予每個子野不同的權重,所有射野的子野都被最佳化,由此產生期望的治療計畫。
治療時各個子野分步按順序進行,在實施治療過程中,葉片運動到第一個子野規定的位置停下,加速器出束,達到規定mu停下,然後葉片運動到下一個子野的規定位置停下後加速器再出束;如此進行下去,使得每個子野的強度累加,直到完成整個射野,所有子野的束流強度相加形成要求的強度分布。
一般來說,希望儘量減少子野數目、葉片運動次數和MU數以便保證劑量傳送的精度,但是子野太少劑量分布就達不到調強的要求。MLC靜態調強在每個子野照射結束後必須關斷射線才能轉到下一個子野,由於加速器射線的開關動作,帶來劑量率的穩定問題,從而對AFC系統提出了較高的要求;或者說只有柵控電子槍才能完全實現這種要求!
靜態調強劑量驗證比較容易,但是需要的治療時間比較長。
動態調強
這種調強是利用MLC相對應的一對葉片的相對運動來實現對射野內強度的調節的。
在每個射野的照射過程中,由計算機系統按照調強計畫給出的數據進行控制,在各對葉片作變速運動時,加速器不停地以變化的劑量率出束,由此得到所要求的強度分布。治療時每對葉片構成一個窗,它們在計算機控制下橫掃過靶區。窗的開口和葉片運動速度都按照預定的方案不斷調節,以便產生需要的強度分布。這也同樣決定於滑窗軌跡之下的治療區內各點的吸收劑量。在計畫過程中計算機用一種算法將葉片位置作為每個射野出束時間的函式,將需要的強度分布轉換為葉片位置。
動態調強的技術特點是:一對相對的葉片總是向一個方向運動,並在運動過程中不斷形成各種形狀的視窗(即子野)掃過靶區。
一般動態調強的每個射野都由上百個子野組成,滑窗開口的設定及每對葉片任何時刻都由一個程式控制。在相對的葉片之間的視窗開到最大時,使用最大的葉片速度,這樣可以縮短治療時間。需要參與射束傳輸的葉片數目取決於靶區的長度,靶區越長涉及的葉片就越多。
這種調強方法治療需要的時間比較短,然而劑量驗證工作比靜態調強困難得多。
容積調強
容積調強治療是用加速器內置的標準MLC完成的,是將動態MLC與弧形治療相結合,用鏇轉射束來實現最佳化的劑量分布。用這種技術同樣要先制定調強治療計畫,人為地選擇弧形射野數目及入射角度,再由計畫系統對射束的權重進行最佳化,最佳化計算出臨床要求的強度分布,再轉換為MLC的驅動檔案。
在治療過程中,機架圍繞患者鏇轉,MLC葉片位置每隔10°變化一次以便跟隨靶區形狀,並與楔形板結合使用多共面或非共面弧形照射野。最終的計畫結果被輸入到葉片序列發生器,這個發生器直接複製每個射束的MU數並通過MLC形成射束。這樣的MLC處方被傳送到MLC控制器用於驅動葉片。在出束期間有程式控制加速器實施弧形治療,同時控制MLC動態地逐步完成一系列射野形狀。所有弧形射野的累計劑量分布與計畫期望的分布一致從而達到調強的目的。
當機架圍繞患者鏇轉時加速器是出束的,因此射束角相鄰的照射野不應該要求MLC的葉片運動很長距離。在多數臨床病例中,各個角度之間的射野形狀變化也是緩慢的。為了縮短出束時間,可以用治療機最高的劑量率配以最大的機架放置速度;偶爾由於MLC葉片速度的限制也會要求降低機器劑量率以避免治療時出束暫停。
斷層調強
步進式斷層調強是利用NOMOS公司的孔雀系統(peacock)來進行的。孔雀系統包括一台專門設計的調強準直器,叫做MIMiC。它是一台電動氣動式裝置,可以通過附屬檔案插槽安裝到加速器機頭形成細長的矩形射野,叫做扇形束。在機架放置時,利用MIMiC的開關(ON ,OFF)運動,實現調強治療。MIMiC由兩組40個葉片組成,每組20片,相對排列。葉片是由鎢製作成的,每個葉片高8cm,近源端寬5cm,接近患者一端6 cm寬,葉片在加速器等中心處投影約為10mm。相鄰葉片間有凹凸槽,以減少漏射線。每組葉片形成的細長條矩形野在等中心處的長度的兩擋,分別為10mm和20mm。每個葉片由一個微型氣動活塞獨立控制,兩組葉片同時獨立運動,形成兩個細長條矩形野。也就是說,機架繞患者鏇轉一次,只能治療兩層切片(即2cm) ,一般來說靶區長度都不只2cm,所以要想治療整個靶區就要多次鏇轉機架,與此同時治療床必須連續向前步進,這種步進/鏇轉過程持續進行,直到治療完整個靶區。
在這個過程中MIMiC受氣閥操縱運動,當氣閥打開後,高壓氣體推動活塞使葉片進入射野,當氣閥關閉時,活塞內的低壓氣體反向拉回活塞使葉片推出射野。活塞雙向運動時間約為40-60ms。按照治療計畫給出的強度分布要求,通過計算機控制活塞停留在射野內的時間,就能達到調強需要的強度分布。MIMiC本身有感測器和顯示屏,可以監測葉片運動速度和位置。
這種治療方式,床步進的控制精度對相鄰野劑量分布影響很大。為了減少由於相鄰野不重合產生的不均勻性,治療床步進的精度和可確定性是非常重要的。為此需專門涉及一個控制床步進的配合裝置,以提供0.5mm以內的可選步進。
輻射束調製所需要的控制參數也是從治療計畫得出,由計畫系統寫在軟碟上,用作MIMiC的數據檔案。MIMiC中的控制系統包括微處理器、機架角度感測器和葉片運動感測器。
步進式斷層調強方式治療時間需要很長,而且由於使用氣動閥門,治療時發出很大噪聲可能使得患者會感到不舒服。
適應症
(1) 神經系統腫瘤包括腦膠質瘤、垂體瘤、腦膜瘤、腦轉移瘤、生殖細胞瘤、髓母細胞瘤、室管膜瘤、松果體、脊索瘤、顱內淋巴瘤、腦幹腫瘤、脊髓腫瘤等。
(2) 頭頸部腫瘤 包括鼻咽癌、喉癌、上頜竇癌、口腔癌及中耳癌等。
(3) 胸部腫瘤 包括肺癌、食管癌、縱隔腫瘤及乳腺癌等。
(4) 腹部腫瘤 包括胰腺癌、肝癌、膽管癌、腸癌等
(5) 泌尿及生殖系統腫瘤 包括前列腺癌、腎癌及盆腔腫瘤等
(6) 骨腫瘤 包括骨肉瘤,、軟骨肉瘤、纖維肉瘤等
(7) 其它 血管瘤、惡性肉芽腫等。