背景知識
碳正離子
碳正離子(Carbenium ion)是一種帶正電的不穩定的有機物。與自由基一樣,是一個活潑的中間體,有一個正電荷,最外層有6個電子。經典的碳正離子是平面結構。帶正電荷的碳原子是sp2雜化狀態,三個sp2雜化軌道與其他三個原子的軌道形成σ鍵,構成一個平面,鍵角接近120°,碳原子剩下的p軌道與這個平面垂直,p軌道中無電子。分析這種物質對發現能廉價製造幾十種當代必需的化工產品是至關重要的。
碳正離子的形成過程大概是這樣的: C+上原本連有一個電負性較大的或者吸電子的基團(如-Br, -OH等) 那么這個基團就會將它連線的碳上的電子吸引過去 使該碳稍微顯正電性吸電子基團在適當溶液中還可能帶著一對電子離去(例如Br- ),那么剩下的烴基就形成了碳正離子。
穩定性通常用的數量增加的烷基鍵合到電荷軸承碳。叔碳陽離子是更穩定(並形成更容易)比仲碳陽離子,因為它們是由穩定的超共軛。主要碳正離子是非常不穩定的。因此,反應如Sñ1反應和E1的消除反應通常不如果將形成伯碳正發生。然而,雙重鍵合有離子化的碳的碳可以穩定離子通過共振。這些陽離子作為烯丙基陽離子,CH2= CH-CH2,和苄基陽離子,C6ħ5-CH2,比大多數其他碳陽離子更穩定。能形成烯丙基或苄carbeniums分子是特別反應性的。碳鎓離子,也可通過穩定的雜原子。碳正離子可能發生重排反應,從不太穩定的結構,以同樣穩定或較穩定的人與速率常數超過10/秒。這一事實複雜的合成途徑許多化合物。例如,當3-戊醇中加熱用HCl水溶液中,最初形成的3-戊基碳正離子重新排列到3-戊基和2-戊基的統計混合物。這些陽離子與氯離子反應,產生約1/3 3-氯戊烷和2/3 -2-氯戊烷。
芳正離子
芳烴與B酸作用,可以生成芳基正碳離子,其中帶有正電荷的H 原子位於苯環與側鏈連線處的C原子上。通過模擬計算,可以得出芳基正碳離子的結構示意圖和電子云圖。下面分別列出甲苯、乙苯和正丙苯的電子云圖。
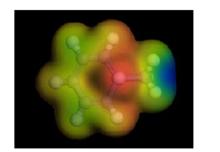 芳基正離子
芳基正離子是甲苯正碳離子的電子云圖,其中紅色位置代表電子云密度較小的區域,藍色位置代表電子云密度較大的區域,從圖中可以看出,正電荷主要集中在H 原子上。
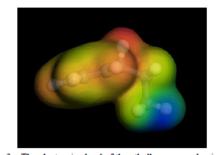 圖2
圖2上圖是乙苯正碳離子的側面電子云圖。
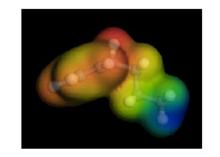 芳基正離子
芳基正離子上圖是丙苯正碳離子的側面電子云圖。從圖中可以看出,與前面分析的芳基正碳離子類似,正電荷主要集中在H 原子上。由於芳基正碳離子的正電荷主要集中在H 原子上,使得該H 原子具有較強的吸電子特性,會對整個離子的結構產生非常大的影響,使得其反應特點發生非常明顯的變化。
下面列出一部分芳烴與芳基正碳離子的結構數據。
表1 部分低碳芳基正碳離子結構數據
 芳基正離子
芳基正離子表2部分長鏈芳烴與芳基正碳離子結構數據
 芳基正離子
芳基正離子表3小分子芳基正碳離子裂化能量數據
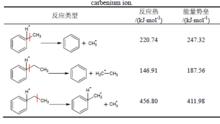 芳基正離子
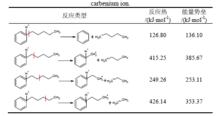
芳基正離子表4小分子芳基正碳離子裂化能量數據
 芳基正離子
芳基正離子從表1和表2中可以看出:當芳烴生成正碳離子以後,其結構發生了比較明顯的變化,由於芳基正碳離子的電荷集中於與苯環相連的H原子附近,使得芳環的α位C-C鍵鍵長增長,β位C-C鍵鍵長縮短,且α位C-C鍵成為烴分子中最長的C-C鍵,其反應活性有了非常顯著的提高。
從表3和表4中可以看出:受正電荷所在位置H原子的影響,芳基正碳離子芳環α位C-C鍵發生裂化需要的能量大為下降,其反應活性有了非常顯著的提高,最容易在該處發生斷裂。
芳烴自由基特點
 芳基正離子
芳基正離子從圖可以看出,芳基自由基整體形成一個大型的共軛結構,使得整個自由基的能量降低,其穩定性得到了提升。由於圖中所示的芳基自由基結構較為穩定,故芳烴在熱裂化條件下主要發生側鏈的斷裂,較少發生脫烷基反應。
芳基碳正離子與芳自由基
芳烴是裂化反應中一類非常重要的反應物,由於芳烴的結構與烷烴和烯烴相比較為複雜,其裂化反應規律也相對比較複雜。烷基芳烴在熱裂化中和在催化裂化中具有不同的反應特點,在熱裂化反應中,芳烴主要發生烷基的斷裂,生成低碳烷基芳烴和烯烴等反應產物[3-4]。而在催化裂化反應中,芳烴主要發生脫烷基反應,生成苯和烯烴等反應產物。
由於芳基自由基和芳基正碳離子的結構存在著非常明顯的不同,使得芳烴在熱裂化和催化裂化條件下的反應產物截然不同。在熱裂化反應中,由於芳環結構的影響,芳環α位C-C 鍵鍵長縮短,β位C-C 鍵鍵長增加,且α位C-C 鍵成為烴分子中最短的鍵,β位C-C 鍵鍵成為烴分子中最長的鍵;芳環β位C-C 鍵發生裂化需要的能量大為下降,其反應活性有了非常顯著的提高,最容易在該處發生斷裂。故芳烴主要在烷基側鏈發生斷裂,主要生成物為低碳烷基芳烴和烯烴。
在催化裂化反應中,芳烴首先生產芳基正碳離子,芳基正碳離子正電荷所在位置為H 原子上,其對於整個離子的結構具有非常明顯的影響,使得芳基正碳離子容易在芳環α位發生斷裂,主要生成物為苯和烯烴。

