親核芳香取代反應
芳香族親核取代反應(Nucleophilic Aromatic Substitution reaction,SNAr)是親核取代反應的一類,發生在芳香環上。當中一個親核體取代了一個好的離去基團,例如在芳香環上的鹵代烴。現有六種芳香環的親核取代反應機理。
正常的SN1和SN2難以發生,在芳環上可以進行的親核取代反應有以下幾種:
雙分子SNAr2機理
芳香親核取代最重要的機理;
分為兩步,與脂肪族親核取代四面體機理,以及芳香族親電取代芳基正離子機理類似,第一步進攻試劑與底物成鍵形成中間體,然後離去基團離去;通常第一步為決速步驟;
機理的證明:
1)二級動力學證明:
2)1902年,分離得到了穩定的Meisenheimer鹽;
3)取代基效應
鄰硝基氯苯和其對位吸電子基團取代衍生物在和甲醇鈉的反應中的相對速度:
4)當X分別為Cl, Br, I, SOPh時,反應速率差別很小,表明C-X的斷裂不是決速步驟;與SN1, SN2機理不同;速率並不完全一致,X的性質會影響Y的進攻速率,X電負性增加,被進攻位點上電子云密度減小,親核進攻速率加快;
單分子SNAr1機理
在芳環上按照SNAr1機理進行的反應很少 ,重氮鹽的水解被認為是按照SNAr1機理進行的,主要存在於芳基重氮化物的親核取代反應中。
苯炔機理
第一步,酸性最強的氫脫去,與Z的場效應有關,吸電子基團有利於鄰位氫脫去,給電子基團有利於對位氫脫去;第二步,能形成最穩定碳負離子中間體的位點是親核進攻的首選位點。
證明:如果芳基鹵化物具有兩個鄰位取代基,反應無法進行;Cilne取代,苯基上有取代基時,親核取代反應可能發生在不同位點上,由取代基定位效應導致;不是所有的Cilne取代都是此反應機理;鹵化物反應活性順序為Br>I>Cl>F,表明非SNAr機理;溫度8K時的氬基質中可分離出苯炔,可觀測到其紅外光譜,苯炔可以被捕獲;本卻具有芳香性,多出的一對電子僅覆蓋兩個碳原子的p軌道。
SRN1機理
自由基鏈式反應機理,需要電子給體引發;加入金屬鉀,更加有效提供溶劑化電子,Cline取代產物消失;加入自由基淬滅劑,9:10接近1.46:1。
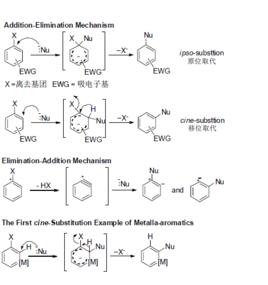
金屬苯的移位芳香親核取代反應
金屬雜芳香體系因其特殊的結構與性能而倍受關注。金屬苯作為金屬雜芳香體系中最重要的代表,由於其既能體現經典有機體系中苯的特性,也能反映金屬有機化合物的性質,而引起廣泛興趣。
SNAr 反應作為能夠證明金屬苯芳香性特徵的重要反應,是金屬雜芳香化學的研究熱點和難點。我們課題組2009 年將該反應拓展到金屬有機體系,報導了金屬苯的首例SNAr反應,隨後利用該反應合成了高穩定性的金屬苯。Wright 小組2011年報導了金屬苯的分子間SNAr反應。而這些已報導的金屬苯SNAr反應都是親核試劑進攻離去基團所連線的碳原子,並且離去的都是在經典有機SNAr 反應中很難脫去的氫負離子。