研究進展
1920年,俄國醫生甫洛諾夫(Serge Voronoff)為了給病人注入青春的活力,將黑猩猩的睪丸切片植入老年男子的陰囊內,10年後,已有數百人接受了這樣的手術,女性也接受猩猩卵巢組織移植以治療更年期症狀
2009年成果
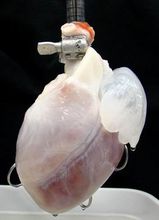 異種器官移植
異種器官移植2009年國明尼蘇達州立大學幹細胞科學家桃瑞絲-泰勒(Doris Taylor),在實驗室中實現了為新培育的微型心臟連線人造血液供給,人造心臟能夠像正常老鼠體內的心臟一樣跳動,但這種心臟看上去更加與眾不同:它復蓋著一層老鼠心臟去細胞組織的“腳手架”,而且新培育的老鼠心臟組織是基於另一隻老鼠的幹細胞培育而成。
桃瑞絲的方法非常簡單:從人體捐獻者或其他動物身體上提取器官,然後用溫性洗滌劑去除器官上的肌肉、細胞和DNA,只保留一種叫做“免疫惰性”蛋白質的內部“腳手架”蛋白質,從相關患者體內提取幹細胞附加在這個“裸體腳手架”上,來自患者體內的幹細胞在培育過程中,會對移植器官起到主體免疫功能,並避免主體遭受由於移植器官導致的新感染。
培育出簡單的器官
基於桃瑞絲的方法已成功培育出一些簡單的器官,2008年,患者克勞迪婭-卡斯蒂諾(Claudia Castillo)接受了一個來自死亡捐獻者的氣管移植器官,研究人員從捐獻者體內提取氣管,進行大小剪裁,然後放入從克勞迪婭體內提取的幹細胞培養環境腳手架中,最終發育形成相應的氣管組織。
她還基於這項老鼠實驗,重複性地試著培育豬的心臟和肝臟,對於豬器官的培育將更簡單一些,因為豬的體型更大,要比處理培育體型較小的老鼠器官更容易。預計去細胞化的移植肝臟器官將比心臟更早地培育出來。
其他研究小組也從事於移植肝臟培育研究,科學家史蒂文-巴迪拉克(Steven Badylak)稱,現已研究出如何在老鼠體內培育肝臟去細胞培育法,只是該技術尚未發布。此外,美國麻薩諸塞州總醫院的研究小組負責人馬丁-亞穆什(Martin Yarmush)培育了人造可移植老鼠肝臟器官,從而證明在實驗室內可以培育出具備肝功能的移植器官。據該研究小組成員科庫特-尤岡(Korkut Uygun)稱,研究小組的最終目標是培育出人體去細胞移植器官,並不僅是簡單的動物器官。
技術難點
桃瑞絲這種培育的複雜器官面臨的較大挑戰是如何確保所有的器官內細胞與患者的血液相溶合,如果沒有血液進入,移植器官中心的細胞則會嚴重缺氧,導致移植後細胞死亡。桃瑞絲稱,她有辦法能夠克服這種困難。2008年1月,她帶領的一支研究小組實現了較大的技術突破,他們基於新生老鼠心臟細胞培育出一個跳動中的心臟,這個心臟保持著3D外形,其內部充滿著所有血管。當他們植入一些新的細胞,會生長出血管組織。此外,桃瑞絲表示他們幾乎能夠重新培育出帶有細胞的完整血管系統,其中包括動脈、靜脈和毛細血管。她說:“由於我們培育出了血管,新的移植器官能夠與患者身體的血液供給系統自然地連線在一起。”在移植心臟器官的培育過程中,幹細胞轉換成為心室和心房的內皮細胞,還可形成血管和心臟平滑肌細胞。
匹茲堡大學醫學院的大衛-庫珀(David Cooper)是異種器官移植技術的主要研發人員,他指出,“裸體”豬心臟仍攜帶著alpha-Gal抗原體,人體免疫系統能夠識別,並遭受其攻擊。但是倫敦大學學院再生醫學教授克莉絲-梅森(Chris Mason)指出,許多培育的去細胞豬器官都沒有施用輔助免疫藥物,必須對豬器官內對人體免疫系統構成攻擊的物質徹底消除,否則未來數百萬名患者一旦接受豬心臟移植後將出現心臟瓣膜和相關組織的副作用。
排異反應
豬心臟經過去細胞化處理後,現成為培育人類移植心臟“腳手架”
 異種器官移植
異種器官移植動物器官異種移植排異過程在某些方面與同種排斥相似,可以借鑑。但異種移植又有其特性:細胞表面存在更多的“異物”,會與宿主產生強烈的反應,這種跨物種間的移植存在較大的分子差
異,包括天然抗體、補體、NK細胞和巨噬細胞等。常出現的超急性排異反應(HAR),排異反應在血液循環後幾分鐘或數小時發生,也可在24-48小時內發生不可逆轉體液排斥反應,較常見的發生在手術台上;急性血管性排斥反應(AVR),血管化臟器移植後數天到數周間發生,也是不可逆轉性體液排斥反應,常發生在手術後早期,病情進展迅速;加速性細胞排斥反應(TMR),受者循環血液中存在抗供者抗體並不一定引起HAR和AVR的情況下,可能出現加速性細胞排斥反應。該反應對免疫抑制劑抑制效果不良。受者抗供者抗體的存在可促進抗體依賴性細胞介導的細胞毒作用,促使發生細胞性排斥反應,病理表現以間質水腫和局限性炎性細胞浸潤為特徵,細胞浸潤的局部毛細血管內皮細胞變性和壞死。異種移植的免疫障礙也遠遠大於同種移植(Allografts)。
異種器官移植排斥反應類型
依據供、受者種族遺傳背景差異程度分為協調性(Concordant)和非協調性(Discordant)。協調性異種移植髮生在種屬較近的動物之間,如大鼠與小鼠之間;非協調性異種移植則在種系發生較遠的種屬間進行,排斥以分鐘或小時計,常導致HAR發生,如豬器官移植到人、豚鼠與大鼠之間的移植。有學者將協調性異種移植分為困難型和容易型;依據排斥反應發生機理將非協調性異種移植分為抗體型和非抗體型兩類。所不同的是在協調性異種移植中是誘生抗體,而在非協調性移植中則是預存天然抗體。
存在問題
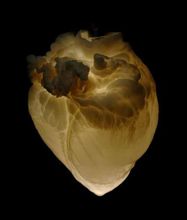 異種器官移植
異種器官移植雖然異種器官移植給人類移植器官的短缺帶來希望,但有些科學實驗表明還有令人擔心的問題存在。美國加州斯克里普斯研究所丹尼爾·沙羅門等人在實驗中發現,豬體內普遍存在的“豬內生逆轉錄酶病毒”能感染人體細胞。沙羅門等還發現,將豬胰腺細胞移植給免疫功能受到抑制的實驗鼠後,該病
毒會被激活,使鼠機體多種組織受到感染。
科學家尚未發現該病毒對豬有害,受感染的實驗鼠也未患上疾病。但是,人體被該病毒感染後會產生什麼後果,目前還不得而知。不同動物體內有不同的微生物群,對一種動物無害的病毒,在另一種動物身上可能造成嚴重危害,這並非沒有先例。1997年,英國倫敦大學學院的羅賓·韋斯等就曾報告說,他們在豬體內發現了兩種新型病毒。這兩種病毒不僅不損害豬的健康,而且一定程度上還能增強豬的機體功能。然而它們卻能使猴子、貓和某些鳥類患上白血病。從其結構推斷,科學家認為它們也可能會讓人類患上白血病。
科學家擔心,人類對豬體內的各種病毒還了解得太少,將豬器官移植給人存在風險,甚至有可能引發新型大規模傳染病,產生不堪構想的後果。
儘管病毒問題給異種器官移植的前景投下重重陰影,許多科學家仍贊成繼續這類研究。他們指出,異種器官移植具有極大醫療潛力,不應半途而廢。科學家們呼籲深入研究豬體內的病毒並尋求相應的對付方法,同時對移植試驗進行嚴格的審查與控制。
器官移植排斥的類型
宿主抗移植物反應
 異種器官移植
異種器官移植受者對供者組織器官產生的排斥反應稱為宿主抗移植物反應(host versus graft reaction,HVGR)根據移植物與宿主的組織相容程度,以及受者的免疫狀態,移植排斥反應主要表現為三種不同的類型。
(一)超急排斥
超急排斥(hyperacute rejection)反應一般在移植後24小時發生。目前認為,此種排斥主要由於ABO血型抗體或抗Ⅰ類主要組織相容性抗原的抗體引起的。受者反覆多次接受輸血,妊娠或既往曾做過某種同種移植,其體內就有可能存在這類抗體。在腎移植中,這種抗體可結合到移植腎的血管內皮細胞上,通過激活補體有直接破壞靶細胞,或通過補體活化過程中產生的多種補體裂解片段,導致血小板聚集,中性粒細胞浸潤並使凝血系統激活,最終導致嚴重的局部缺血及移植物壞死。超急排斥一旦發生,無有效方法治療,終將導致移植失敗。因此,通過移植前ABO及HLa 配型可篩除不合適的器官供體,以預防超急排斥的發生。
(二)急性排斥
急性排斥(acute rejection)是排斥反應中最常見的一種類型,一般於移植後數天到幾個月內發生,進行迅速。腎移植髮生急性排斥時,可表現為體溫度升高、局部脹痛、腎功能降低、少尿甚至無尿、尿中白細胞增多或出現淋巴細胞尿等臨床症狀。細胞免疫應答是急性移植排斥的主要原因,CD4+T(TH1)細胞和CD8+TC細胞是主要的效應細胞。即使進行移植前HLA配型及免疫抑制藥物的套用,仍有30%~50%的移植受者會發生急性排斥。大多數急性排斥可通過增加免疫抑制劑的用量而得到緩解。
(三)慢性排斥
慢性排斥(chronic rejection)一般在器官移植後數月至數年發生,主要病理特徵是移植器官的毛細血管床內皮細胞增生,使動脈腔狹窄,並逐漸纖維化。慢性免疫性炎症是導致上述組織病理變化的主要原因。目前對慢性排斥尚無理想的治療措施。
移植物抗宿主反應
如果免疫攻擊方向是由移植物針對宿主,即移植物中的免疫細胞對宿主的組織抗原產生免疫應答並引起組織損傷,則稱為移植物抗宿主反應(graft versus host reaction,GVHR)。GVHR的發生需要一些特定的條件:①宿主與移植物之間的組織相容性不合;②移植物中必需含有足夠數量的免疫細胞;③宿主處於免疫無能或免疫功能嚴重缺損狀態。GVHR主要見於骨髓移植後。此外,脾、胸腺移植時,以及免疫缺陷的新生兒接受輸血時,均可發生不同程度的GVHR。
急性GVHR一般發生於骨髓移植後10—70天內。如果去除骨髓中的T細胞,則可避免GVHR的發生,說明骨髓中T細胞是引起GVHR的主要效應細胞。但臨床觀察發現,去除骨髓中的T細胞後,骨髓植入的成功率也下降,白血病的復發率,病毒、真菌的感染率也都升高。這說明,骨髓中的T細胞有移植物抗白血病的作用,可以壓倒殘留的宿主免疫細胞,避免宿主對移植物的排斥作用;也可以在宿主免疫重建不全時,發揮抗微生物感染的作用。因此,選擇性地去針對宿主移植抗原的T細胞,而保留其餘的T細胞,不但可以避免GVHR,而且可以保存其保護性的細胞免疫功能。