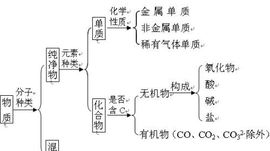
分類的方法
單一分類法
對對象使用一種標準的分類法(如氧化物按組成元素分為金屬氧化物、非金屬氧化物)
交叉分類法
對對象用多種不同的單一分類法進行分類(如將H2SO4按是否有氧元素、酸的強弱、酸的元數等不同標準進行分類,H2SO4分別屬於含氧酸、強酸和二元酸)
樹狀分類法
根據被分對象的整體與分支的類型之間的關係,以陳列式的形狀(樹)來定義。
純淨物
1.單質:由一種物質組成的純淨物
K、Ca、Na、Mg、Al、Zn、Fe、Sn、Pb、Cu、Hg、Ag、Au等
非金屬單質主要有:C、S、P、Si、O2、N2、H2、Cl2、He、Ne、Ar
2.化合物:
2.1有機物:烴、烴(烴的衍生物)、營養物質
烴:烷烴(甲烷),烯烴(乙烯),炔烴(乙炔),芳香烴(苯)
營養物質:葡萄糖、蛋白質、脂質
2.2.無機物:氧化物、氫化物、酸、鹼和鹽等
氧化物:由氧和另一種元素組成的純淨物(無機物)
酸性氧化物:SO2、CO2、P2O5、Mn2O7等
鹼性氧化物:MgO、CaO、Na2O(一定是金屬氧化物)等
兩性氧化物:Al2O3、ZnO等
不成鹽氧化物:CO、NO等
過氧化物:Na2O2、H2O2等
酸:指電離時產生的陽離子全部都是氫離子的化合物
含氧酸:HNO3等
無氧酸:HCl等
一元酸:HCl、HNO3,CH3COOH等
二元酸:H2CO3、H2SO4、H2S等
多元酸:H3PO4等
鹼:指電離時產生的陰離子全部都是氫氧根離子的化合物
強鹼:NaOH等
弱鹼:Fe(OH)3、NH3·H2O等
可溶性鹼:KOH、NaOH、Ba(OH)2、Ca(OH)2、NH3·H2O
不溶性鹼:Mg(OH)2、Cu(OH)2、Fe(OH)3等
鹽:指電離時能生成金屬陽離子(或NH4+)和酸根離子的化合物
正鹽:Na2CO3、NaCl、BaSO4等
酸式鹽:NaHCO3等
鹼式鹽:Cu2(OH)2CO3等
復鹽(又叫重鹽):KAl(SO4)2·12H2O,是指由兩種或兩種以上的陽離子與同一種酸根離子形成的鹽。
混鹽:是指同一種金屬陽離子與兩種或兩種以上的酸根陰離子形成的鹽。如CaOCl2等。
混合物
溶液、膠體、懸濁液、乳濁液等
氣態:例:空氣,N2,O2,CO2及稀有氣體等
固態:混凝土(水泥,砂子,碎石)等
液態:溶液:均一,穩定,透明
濁液:不均一,不穩定,不透明