簡介
要充分利用超臨界流體的獨特性質,必須了解純溶劑及其和溶質的混合物在超臨界條件下的相平衡行為。現用超臨界純溶劑的相圖來表明臨界點及其相平衡行為。
由於二氧化碳溶解、萃取物質的能力與二氧化碳本身的密度成正比,這就意味著只要通過改變壓力或溫度來改變溶劑二氧化碳的密度,就可以改變其對物質的溶解能力。利用不同密度下的二氧化碳對物質溶解能力的差異就可以實現萃取和分離的操作,而無需通過相變。
純二氧化碳p-T圖
壓力-溫度圖
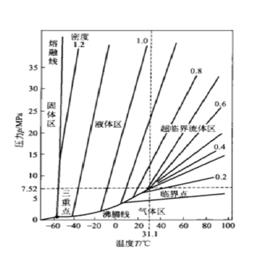
下圖為以純二氧化碳的密度為第三參數的壓力-溫度圖,圖中分別標註了氣、液、固相區和臨界點及其相應的超臨界流體區。
 圖1.二氧化碳的p_T_ρ圖
圖1.二氧化碳的p_T_ρ圖三條臨界線
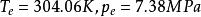 熔融線
熔融線(1)沸騰線(飽和蒸氣曲線)從三重點(T=216.58K,p=0.5185MPa)到臨界點( )為止。
(2)熔融線(熔解壓力曲線)從三重點出發隨壓力升高而陡直上升。
(3)升華壓力曲線對超臨界流體萃取無多大意義。
在二氧化碳的相圖中,升華線、熔融線和沸騰線將相圖分為固相區、液相區和氣相區。但當二氧化碳的壓力和溫度各自超過其臨界壓力、臨界溫度時,沸騰線消失,進入超臨界區。此時,已無液態和氣態的明確界線,對應點稱為臨界點,且在臨界點的附近,密度線聚集於臨界點周圍,壓力或溫度小範圍的變化,就會引起二氧化碳密度的大幅度變化。
臨界溫度和臨界壓力
這裡臨界點的概念可用臨界溫度和臨界壓力來解釋,這兩個名詞可定性地定義如下:
(1)臨界溫度是指高於此溫度時,無論加壓多大也不能使氣體液化;
(2)臨界壓力是指在臨界溫度下,液化為氣體所需的壓力。
操作範圍
從純二氧化碳的壓力-溫度圖(以密度為第三參數)還可以得到不同分離過程的操作範圍:
精餾操作
精餾操作通常接近於沸騰線。
液相萃取和吸收過程
液相萃取和吸收過程則在沸騰線與熔融線之間進行。
吸附分離操作
吸附分離操作則在熔融線的左側進行,氣相色譜中,二氧化碳為流動相,其操作範圍在高於室溫和壓力達2MPa的氣相區。
超臨界流體萃取和超臨界色譜操作
超臨界流體萃取和超臨界色譜操作則位於高於溶劑的臨界溫度和壓力的區域內。
超臨界流體萃取的實際操作範圍以及通過調節壓力或溫度改變溶劑密度從而改變溶劑萃取能力的操作條件,可以用二氧化碳的對比壓力一對比密度圖中得到。所謂對比壓力、對比密度或對比溫度,是指操作壓力、密度或溫度與臨界壓力、密度或溫度的比值,而超臨界流體萃取和超臨界色譜的實際操作區域為圖中虛線以上部分,大致在對比壓力大於1,對比溫度為0.9~1.2。