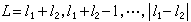氦原子光譜
正文
氦原子光譜有兩套線系,即兩個主線系,兩個銳線系,兩個漫線系等。從對這些線系的分析得知,氦原子有兩套能級,一套是單層的;另一套是三層的。這兩套能級之間沒有交叉的光譜躍遷。兩套能級各自內部的躍遷產生兩套光譜。單層能級之間躍遷產生單線結構的光譜,三層能級之間躍遷產生複雜多線結構的光譜。氦的著名黃色 D3線就是屬於後一種光譜。1868年8月18日在太陽日珥的光譜中觀察到這條譜線從而發現了氦。用高分辨本領的儀器可以分出它的三個成分是 5875.963┱、5875.643┱和5875.601┱,人們早年對氦有兩套能級尚無認識時,曾構想有兩種氦,產生單線光譜的稱為仲氦,而產生多線結構的稱為正氦。氦有兩個價電子,基態時處在(1s1s)電子組態。受激發時,通常是一個電子被激發到較高能態而另一個電子仍處在1s態。氦原子中兩電子角動量之間按LS 耦合,兩電子合成總自鏇量子數S=0,1;兩電子合成總軌道量子數
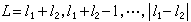 。可見氦原子能級有單層結構(S=0即兩電子自鏇反向)和三層結構(S=1,即兩電子自鏇同向)兩套能級。
。可見氦原子能級有單層結構(S=0即兩電子自鏇反向)和三層結構(S=1,即兩電子自鏇同向)兩套能級。 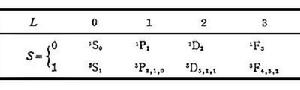 氦原子光譜
氦原子光譜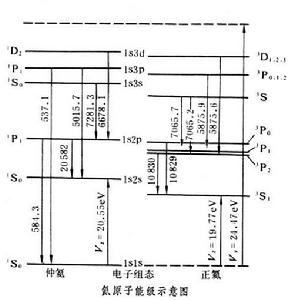 氦原子光譜
氦原子光譜根據光譜躍遷選擇定則:ΔS=0,說明單層與三層能級間不能交叉躍遷。此外 ΔL=±1;ΔJ=0,±1可以說明能級和光譜結構之間的關係。單層能級間躍遷產生的各線系都是單線結構;而三層能級間躍遷產生的主線系(3P2,1,0→3S1)和銳線系(3S1→3P2,1,0)都是由三條譜線組成,而漫線系(3D3,2,1→3P3,2,1)共有六種躍遷符合ΔJ=0,±1選擇定則,故漫線系譜線應是由六條靠得很近的譜線組成。若儀器分辨本領不夠高,不能觀察到分開的六條譜線,有時可見到三條, 其中的D3線即是漫線系中的第一條。
氦原子如激發到(1s2s) 電子組態, 由它形成的(1s2s)3S1比基態高19.77eV為第一激發態,(1s2s)1S0比基態高 20.55eV為第二激發態。從這兩狀態向基態的躍遷都是選擇定則所禁戒的,因此原子處在這兩激發態時不易自發向基態躍遷,原子處在這兩激發態的平均壽命比其他能級長五六個數量級。故把這種激發態稱亞穩態。氦原子的這兩個亞穩態在許多氣體放電管和氦氖雷射器的激發機理中起著十分重要的作用。