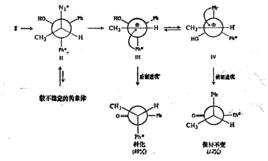
碳正離子的重排定義
重排的方向和推動力
碳正離子可以發生重排反應。在重排時,一個有機基團或一個氫原子帶其一對電子遷移到缺電子碳上,這樣就在基團轉移離去的碳原子上產生了一個新的碳正離子中心。通常,1,2一基團遷移是最常見的一類重排反應:
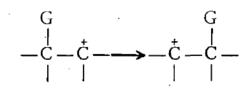 正離子轉移重排
正離子轉移重排這種重排反應的推動力是形成更為穩定的碳正離子。我們知道,帶電體系的穩定性隨著電荷的分散而增大。在簡單的烷基正離子中,由於烷基的誘導效應和超共軛效應可以使缺電子碳上的正電荷得到分散。所以,碳正離子的穩定性順序是:叔碳正離子>仲碳正離子>伯碳正離子。因此,在通常的1,2一遷移中,大多是由較低級的碳正離子重排成為更高級的碳正離子。
一些重要的觀點
首先,有未共用電子對的原子能使碳正離子的穩定性大為增加:
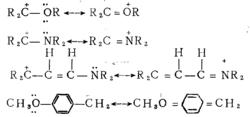 正離子轉移重排
正離子轉移重排這是通過雜原子的未共用電子對參與共軛來實現的。既然碳正離子重排的推動力是形成更為穩定的碳正離子,那么,當能量上有利時,也可以由高級的碳正離子重排成為較低級的碳正離子。經典的頻哪醇重排就屬此例·(由叔正離子重排為仲正離子):
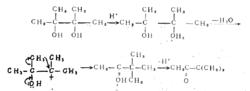 正離子轉移重排
正離子轉移重排在此例中,重排結果生成了質子化的酮,質子化的酮失去質子最後得到酮。其特徵在於分子中有第二個氧原子存在。正是這個氧原子和它的未共用電子對促進了重排反應的進行,任何能夠產生類似結構碳正離子的反應,正常情況下也將發生頻哪醇重排反應。例如β一氨基醇的去氨基反應;2一鹵代醇的脫鹵素反應;
其次,在分子水平上,穩定性沒有淨增益時也可以發生重排反應。曾用同位素標記法測定對甲苯磺酸2-丁醋在乙酸中溶劑解時產生的2-丁基正離子轉變成乙酸2-丁酯的情況:
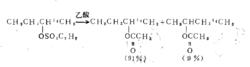 正離子轉移重排
正離子轉移重排這說明,2一丁基正離子在被溶劑截獲前,已經部分發生了同級重排,即由開始形成的仲碳正離子重排成為新的仲碳正離子。
再次,在有些重排反應進行過程中甚至包含由較穩定正離子變為較不穩定正離子的步驟。
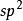 正離子轉移重排
正離子轉移重排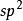 正離子轉移重排
正離子轉移重排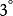 正離子轉移重排
正離子轉移重排最後,在碳正離子中,正性碳原子是雜化或接近雜化的,而且正性中心的幾何形狀是平面的,這在能量上比較有利。如果分子的特徵阻礙潛在的碳正離子成為平面結構,碳正離子的能量就會比較高,很難形成。Bartlett和Knox曾把1-氯-7,7-二甲基雙環(2.2.1)庚烷在硝酸銀乙醇溶液中回流48小時,但回收得到沒有變化的起始物。按理說碳正離子是容易形成的,此化合物對親核取代反應如此惰性,可歸因於在橋頭位置上形成碳正離子時所出現的張力。雙環體系的結構不允許圍繞正離子的碳採取平面構型。
重排的歷程和立體化學
在1,2一遷移中,遷移基團是帶著一對電子轉移到缺電子碳上,因此這類重排反應相當於是分子內的親核取代反應。親核取代反應有兩種歷程:SNI和SN2,重排反應也同樣有這兩種可能性。它可以類似SNI反應,遷移基團須等離去基團離開後才開始移動:
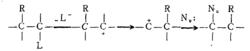 正離子轉移重排
正離子轉移重排它也可以類似於SN2反應,遷移基團在一步反應中幫著把離去基團推出,即以協同的方式發生重排。
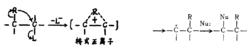 正離子轉移重排
正離子轉移重排這個橋式正離子結構,可能是中間體,也可能是過渡液態,這要取決於何種基團遷移。
遷移基團為芳基時,中間產物的結構可能為:(左下圖)
當遷移基團為烷基或氫時,中間橋式結構可能為:(中、右圖)
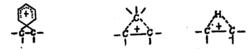 正離子轉移重排
正離子轉移重排虛線表示兩個電子在三個原子之間形成的鍵,這種離子與一般的碳正離子不同,叫做非經典碳正離子。
顯然,好的離去基團,穩定的叔或苄基型的正離子的生成和使用高度非親核性的介質,有利於反應按SNl歷程進行,反之,則很可能是按SN2歷程進行的。如果按SN2歷程進行,由於鄰基協助發生,常可觀察到反應速度的增加。從立體化學而言,當按SN2歷程進行重排時,遷移基團比較有利的幾何位置是跟離去基團處於反式共平面的位置。事實觀測到的情況確是如此。如順1,2-二甲基-1,2-環已二醇在稀硫酸作用下迅速重排,甲基迅速遷移得到環已酮。而其反式二醇在相同條件下,則發生環縮小反應:
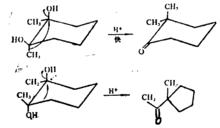 正離子轉移重排
正離子轉移重排在這種情況下,如果遷移基團是手性的,則其手征性中心的構型保持不變。而它所達到的原子則應發生構型轉化。
基團的遷移能力
在1,2一遷移中,究竟哪個基團遷移,這是個比較複雜的問題。但是,在由電子因素的內在遷移能力所控制的重排反應中,一般有以下規律:
1) 芳基比烷基有較大的遷移能力。
2)當其它情況相同時,各種芳基間的相對遷移能力,取決於芳環容納正電荷的能力,其容納正電荷的能力越強,則遷移傾向越大。
3)除此而外,結構改組時的能量變化也受分子張力的影響,能使分子張力降低的重排特別有利。構象效應在重排反應中也會控制基團的遷移方向。Collins在把一個苯基用碳-14標記後,對旋光性的2-氨基-1,1-二苯基-1-丙醇所進行的去氨基反應就證明了這一事實:
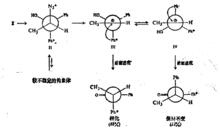 正離子轉移重排
正離子轉移重排顯然,構象效應主要地決定著重排反應的過程。最穩定,因而也是重氮離子的最豐富的構象是l,其中兩個龐大的苯基位於微小的氫的兩側,它脫去氮而生成碳正離子III。大部分重排就是由這種最初形成的正離子引起的,且重排的方式和這個正離子的構象是符合的。