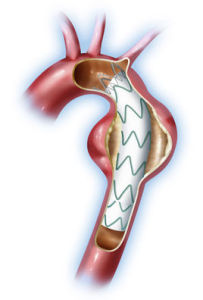
優點
血管、腔道狹窄、閉塞是介入支架植入技術的治療強項。具有創傷小、療效高、風險低、併發症少、住院時間短等優點,為血管、腔道狹窄、閉塞開創了一條新路。以儘可能小的創傷換取同樣甚至更高的療效是外科的發展方向,腹腔鏡、冠狀動脈擴張成形術在臨床的成功套用是典型事例。21世紀是微創醫學的世紀,介入放射技術是微創醫學主要組成部分,以微小創傷、更高療效、更低風險順應了醫學的發展方向。
套用
食管狹窄支架置入術
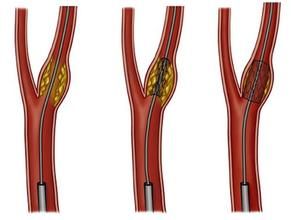 支架植入術
支架植入術1.適應證
①冠心病;②惡性腫瘤引起的食管-氣管瘺或食道縱隔瘺;③良性病變出現食道破裂瘺,如外傷、術後吻合口瘺、化學性灼傷破裂等,保守治療失敗或不能耐受外科手術治療;④食管良性狹窄反覆球囊擴張治療效果不佳者。
2.禁忌證
①凝血機制障礙未能糾正的;②嚴重心、肺功能衰竭;③嚴重惡病質狀態;④重度食道胃底靜脈曲張支架置入手術有引起出血可能。
3.介入治療技術
支架選擇極為重要。食管癌患者選擇覆膜防滑式支架能延緩腫瘤長入支架腔內的時間。治療食管氣管瘺或食道縱隔瘺必須用覆膜支架。良性狹窄置入支架後易移位,故以防滑、可回收支架為宜。直徑17~20mm為目前臨床常用支架,支架兩端均應超出病灶2cm左右,治療食道瘺時適當增加支架長度。
球囊預擴張後沿硬交換導絲送入支架準確定位後釋放。立即經導管注入對比劑,觀察支架位置、展開程度以及是否通暢、有無穿孔等並留存資料。預擴張球囊直徑的選擇應綜合考慮病變性質和範圍以及支架直徑、支撐力和順應性等特點。既要有利於支架的順利釋放,充分膨脹,又要兼顧支架釋放後的穩定。一般球囊直徑較欲置入的支架直徑小2~3mm,狹窄較輕的病人也可不用球囊預擴張。術後2~3天流質飲食,逐漸改為半流質、軟食,普食。忌吞咽粘稠、質硬大塊食物,如完整蛋黃、大塊雞骨等。應建議患者坐位進食,充分咀嚼,餐後多飲流質或水。嚴重嘔吐能導致支架移位。
下腔靜脈節段性閉塞
1、適應症
下腔靜脈膜性、節段性狹窄或閉塞;下腔靜脈狹窄或閉塞行球囊擴張後出現再狹窄;下腔靜脈狹窄或閉塞球囊擴張後彈性回縮>40%。
2、禁忌症
合併下腔靜脈新鮮血栓形成者。
未發育成熟的兒童布加綜合徵。
3、介入治療技術
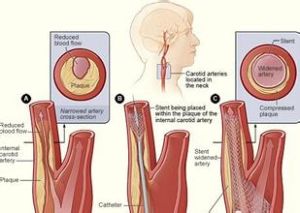 頸動脈支架植入術
頸動脈支架植入術注意事項:
①對良性狹窄置入支架必須慎重;②高位支架可能導致患者明顯不適,一般食管支架最高不能靠近環狀軟骨3cm處;③通過賁門的支架應是防返流支架。(2)下腔靜脈節段性閉塞(布、卡氏綜合症)。
一般肝後段下腔靜脈在側位觀多向前上方向走行進入右心房,其曲度通常為135°~160°,應按血管走行方向調整穿刺針角度,穿通病變時最好能正、側位交替造影觀察,使穿刺針進針方向始終對準閉塞段近心端的定位導管。2.放置支架瞬間囑病人閉住呼吸,因下腔靜脈可隨呼吸上下移動,影響支架定位。3.術中、術後均需肝素抗凝。
基於3D列印和微流控技術的體外支架植入手術
醫學上採用的心臟支架植入手術已經成為治療心血管疾病的重要手段之一。然而術後一年左右,病人的支
架植入部位會發生再狹窄病變現象(restenosis,圖1),尤其當支架植入位置不當時,再狹窄病變演化將加速,這已成為冠狀動脈疾病治療的一大難題。以往研究往往採用簡單的壁面光滑“Y”型流道進行數值模擬,計算支架放入後動脈分岔區域壁面剪下應力(wallshearstress,WSS)的影響。這類簡單模擬結果無法為實際臨床病例提供可靠信息。
為了針對真實病例解決這一問題,中國科學院物理研究所生物物理實驗室聯合中國科學院力學研究所LNM室微流動課題組、安貞醫院心臟病科及中國科學技術大學開展了臨床-實驗-模擬相結合的合作研究。首先由醫院提供實際臨床病例,採用血管造影術(angiography)掃描病變部位。然後引入3D列印及微流控技術,將真實血管病變部位模型“複製”加工到三維微流控晶片上。力學所LNM實驗室微流動課題組承擔了微流控晶片製作及流場測試工作,通過MicroPIV和共聚焦實驗系統,測量了實際病變部位附近的流場並計算了壁面剪下應力,給出了臨界壁面剪下應力約為0.4-0.5Pa,發現堵塞會發生在壁面剪下應力小於臨界值的部位,為臨床診斷提供了參考數據。
該研究首次提供了一種複製真實病例進行體外支架植入手術的實驗室研究方法(invitrovirtuestentimplantationsurgery),為今後與臨床病例緊密結合,提供最佳化的支架植入位置,以減小支架植入後再堵塞風險的體外實驗做了初步探索。相關結果發表在Scientificreports上(Vol.5:10945,May2015),力學所鄭旭為共同第一作者,李戰華為共同通訊作者。該研究得到了國家“973”項目(2013CB837200)、國家自然科學基金(11474345、11272322、11202219)及北京市自然科學基金(7154221)的支持。