成份
1.主要成份:
重組人促紅素,系從人類肝細胞獲取的人促紅素基因組DNA,經過基因重組而由中國倉鼠卵巢細胞產生的含有165個胺基酸(CHNOS:分子量18,235.96)的糖蛋白質(分子量:約30,000)。
2.輔料:
聚山梨酯80、鹽酸精氨酸、磷酸二氫鈉、氯化鈉、磷酸氫二鈉、注射用水
性狀
無色澄明液體,pH5.5-6.5。
適應症
施行透析時的腎性貧血。
規格
0.5ml:1500IU
0.5ml:3000IU
用法用量
在給藥初期,通常對成人給予Epoetin alfa(基因重組)每次3,000國際單位(IU),每周三次緩慢地靜脈注射。貧血情況改善後,將劑量改為每次1,500國際單位,每周兩至三次,或者每次3,000國際單位,每周兩次維持治療。以血紅蛋白濃度(Hb)約100mg/ml(紅細胞壓積值30%),作為貧血症狀改善與否的指標。另外,可依照患者的貧血症狀及年齡等在劑量上做適當的增減,但是最高維持劑量不可超過每周三次,每次3,000國際單位。
不良反應
 利血寶
利血寶1.一般不良反應
在4,435例中觀察到284例(6.4%)有不良反應。主要的不良反應有血壓上升166例(3.74%),頭痛43例(0.97%)等,主要的臨床檢查值異常有GPT上升13例(0.29%),GOT上升11例(0.25%),γ-GTP上升11例(0.25%)。
2.嚴重不良反應
1)休克:休克的發生是罕見的,但應注意觀察,如發現異常時,採取停藥等適當處置。
2)高血壓性腦病:因急劇的血壓上升有引起頭痛、意識障礙、痙攣等高血壓性腦病,甚至有腦出血症狀發生的可能,需密切注意血壓及紅細胞壓積值的變化給藥。
3)腦梗塞:有引起腦梗塞的可能,應密切注意觀察,如發現異常時,採取停藥等適當處置。
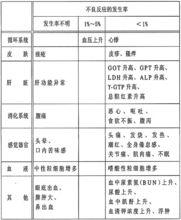
3.其他不良反應
禁忌
1.未控制的重度高血壓患者。
2.對本劑或對其他促紅素製劑過敏者。
3.合併感染者,宜控制感染後再使用本品。
注意事項
1.對下列患者應慎重給藥
(1)有心肌梗塞、肺梗塞、腦梗塞的患者,或者是有這些病史而可能引起血栓栓塞的患者(有報告指出,因給予本劑而引起血液粘稠度上升,所以必須充分地觀察是否有誘發血栓栓塞或使之惡化的因素)。
(2)高血壓的患者、高血壓性腦病
(3)有藥物過敏史的患者
(4)有過敏傾向的患者
2.重要注意事項
(1)本劑的用藥對象僅限於日常活動受到貧血干擾的腎性貧血病人。同時,用藥對象以血紅蛋白濃度低於100mg/ml(紅細胞壓積值小於30%)為指標。
(2)本劑用藥前應確認為腎性貧血,而對其他原因的貧血(如出血性貧血,各類血細胞減少症及鋁蓄積症等)不予給藥。
(3)用藥前須充分問診,以防止休克等反應的發生。初次用本劑或停藥後,再用本劑時,應先以少量行靜脈注射,確定無異常反應發生後再給予全量。
(4)本劑用藥期間應定期地檢查血紅蛋白濃度或者是紅細胞壓積值(用藥初期每周一次,維持給藥期每兩周一次)。應注意避免過度造血(確認血紅蛋白濃度不超過120mg/ml或紅細胞壓積值不超過36%),如果發現過度造血,應採取暫時停藥等適當的處置。
(5)本劑用藥後可能會觀察到血壓上升或者是高血壓性腦病,因此需注意血壓或紅細胞壓積值的變化而小心用藥,特別應注意使紅細胞壓積值緩慢上升。另外,停止用藥後紅細胞壓積值也有上升的可能,需注意觀察,當發現血壓上升時應採取停止用藥等適當處置。
(6)本劑的用藥可能會引起高鉀血症,適當的飲食調整是必要的。
(7)由於本劑的用藥可能會造成分流器的閉塞和血液透析裝置內留有殘血。所以,要充分留意分流器和血液透析裝置內的血流量。如有此情況發生,要重新設分流器或增加抗凝劑的劑量。
(8)鐵的存在對本劑的效果很重要,因此當鐵缺乏時(血清鐵蛋白低於100ng/ml,或轉鐵蛋白飽和度低於20%),應對病人給予鐵劑。
(9)葉酸或維生素B12不足會降低本品療效。嚴重鋁過多也會影響療效。
3.套用時的注意事項
(1)須遵照醫師的處方指示使用。
(2)注射本劑時請勿與其他藥物混合使用。
(3)本劑為單點易折式安瓿,建議用酒精棉等擦拭安瓿斷點割處後切割。
4.運動員慎用。
孕婦及哺乳期婦女用藥
對孕婦及哺乳婦女的用藥安全性尚未確立。
兒童用藥
對新生兒、嬰兒、幼兒和兒童使用本劑的安全性尚未確立。
老年用藥
高齡患者套用本品時,要注意監測血壓及紅細胞壓積,並適當調整用藥劑量及次數。
藥物相互作用
尚不清楚
藥物過量
可能會導致紅細胞壓積過高,引起各種致命的心血管系統併發症。
藥理毒理
1.藥理
促紅素(EPO)是由腎臟分泌的一種活性糖蛋白,作用於骨髓中紅系造血祖細胞,能促進其增殖,分化。本品為重組人促紅素(rhEPO)與天然產品相比,生物學作用在體內、外基本一致。藥效學試驗表明,本品可增加紅系造血祖細胞(CFU-E)的集落生成率,並對慢性腎功能衰竭性貧血有明顯的治療作用。
2.毒理
2.1 急性毒性
對小鼠、大白鼠及狗靜脈注射的LD和對出生後4天的大白鼠幼鼠注射的LD,均在20,000IU/kg以上。
2.2 亞急性毒性、慢性毒性
(1)大白鼠
雌、雄大白鼠分別在4周、13周及52周間施行靜脈注射或腹腔注射本劑所做的亞急性、慢性毒性試驗結果顯示,4周、13周及52周間分別以本劑80IU/kg/天、20IU/kg/天以上以及10IU/kg/天以上給藥時主要由於本劑的藥理作用過剩而引起了多血症,且長期給藥的結果會發生骨髓的纖維化。
(2)狗
雌、雄狗分別在4周、13周及52周間施行靜脈注射本劑所做的亞急性、慢性毒性試驗結果顯示,4周、13周及52周間分別以本劑200IU/kg/天以上、100IU/kg/天以上、20IU/kg/天以上給藥時主要由於本劑的藥理作用過剩而引起了多血症,且長期給藥的結果會出現骨髓的纖維化及腎臟的結構變化。
(3)大白鼠幼鼠
對於生後4天的雌、雄大白鼠,進行28天的皮下注射作亞急性毒性試驗,給藥80IU/kg/天以上時,即與成熟大白鼠一樣,引起多血症。
另外,400IU/kg/天以上時有骨髓纖維化、骨形成的結構變化發生。
2.3 對生殖方面的影響
評估大白鼠以本劑20IU/kg/天、100IU/kg/天及500IU/kg/天靜脈注射,在妊娠初期,器官形成期、圍產期及哺乳期對生殖方面的影響。發現有對胎兒的體重減輕、骨化及新生兒的發育抑制等作用,但是無致胎兒畸形作用。
同樣的對兔子以20IU/kg/天、100IU/kg/天及500IU/kg/天在器官形成期施行靜脈注射,結果沒有致胎兒畸形的作用及發育抑制作用。
2.4 抗原性
雖然在兔子、天竺鼠和小鼠顯示抗原性發生,但在臨床試驗中沒有顯示抗體的產生。
2.5 局部刺激性試驗
在兔子眼黏膜一次性刺激性試驗中,未發現有刺激性變化。在大白鼠皮下注射局部刺激性試驗中,發現在注射局部有一時性充血、出血。
2.6 其他
變異原性試驗(微生物、中國倉鼠卵巢細胞和小鼠小核試驗)及致熱性物質試驗(兔子、Limulus test)顯示無異常。
藥代動力學
1.血漿濃度
(1)健康成年男性
對7例健康成年男性,以靜脈注射本劑300IU後,血藥濃度在用藥後達到峰值(Cmax),之後以0.4和7小時的半衰期呈現雙相型減低。
(2)施行透析時的腎功能不全患者
施行透析時的腎功能不全患者11例,在接受本劑300IU的靜脈注射後,顯示出與健康志願者相似形態的血漿濃度變化,半衰期為6小時。
當劑量增加到1,500IU(8例)和3,000IU(12例)靜脈注射後,其半衰期分別是5.9和7.5小時。隨著劑量的增加,本劑在血漿中的消除會輕微減緩。
2.尿中排泄
給7例健康成人志願者靜脈注射本劑300IU後,其結果顯示給藥後24小時以內,給藥量的0.88%由尿中排泄。
貯藏
2℃~10℃避光保存,禁凍結。
包裝
10安瓿/盒
有效期
24個月
執行標準
WS-(S-027)-2004Z
批准文號
0.5ml:1500:國藥準字S20010075
0.5ml:3000:國藥準字S20010076
生產企業
日本國麒麟啤酒株式會社
包裝企業
麒麟鯤鵬(中國)生物藥業有限公司
核准日期
2006年11月8日
