中子分離能
從一原子核中分離出一個中子所需要的最少能量稱為中子分離能(neutron separation energy),用符號 S表示,亦稱“最後一個中子結合能”。
定義式為:
S( Z, A)=[ m( Z, A-1)+ m- m( Z, A)]c .
式中, Z為質子數, A為核子數, m為核素質量, m為中子靜質量, c為真空中光速。此式忽略了原子中電子的結合能。 SI單位為焦耳(J)。法定計量單位還有電子伏(eV)。
質子分離能
從一原子核中分離出一個質子所需要的最少能量稱為質子分離能(proton separation energy),用符號 S表示,亦稱“最後一個質子結合能”。
定義式為:
S( Z, A)=[ m( Z-1, A-1)+ m( H)- m( Z, A)]c .
式中, Z為質子數, A為核子數, m為核素質量, c為真空中光速。此式忽略了原子中電子的結合能。 SI單位為焦耳(J)。法定計量單位還有電子伏(eV)。
α粒子分離能
從一原子核中分離出一個α粒子所需要的最少能量稱為α粒子分離能,用符號 S表示。
定義式為:
S= B(A,Z)- B(A-4,B-2)
= M(A-4,B-2)- M(A,Z)+ M.
式中, M為α粒子的質量, B是結合能。
影響分離能的因素
分離能可以從吸收光譜實驗的數據算出,其大小與配體和中心原子的性質有關。
如果金屬離子一定,則分離能的大小隨晶體場的強弱而變;場強越大,分離能就越大。從八面體配合物的吸收光譜實驗得出,對於同一種常見氧化態的金屬離子生成同一構型的配合物,配體按場強的增大次序大體如下:
I <Br <SCN ~Cl <NO <F <OH ~ONO (亞硝酸根)~HCOO <CO <HO<NCS <NHCHCOO ~edta <NH<en<-NO(硝基)<CO~CN
這個次序叫做光譜化學次序。通常把I 、Br 、Cl 等稱為弱場配體,它們形成的配合物的分離能普遍地較小,而CN 、CO等則稱為強場配體,它們形成的配合物的分離能普遍地較大。
配體相同時,作為中心原子的同一金屬元素的高價態離子的分離能比低價態的要大。如第四周期過渡金屬的+2價離子的六水合配離子的 △值約在7500~14000cm 之間(參看以下圖表1)。
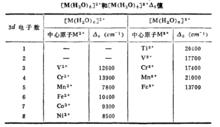 表1
表1同一副族(周期表中同一直行)中相同電荷的金屬離子從第四周期到第五周期, △值約增大40~50%,從第五周期到第六周期約增大20~30%。例如[MoCI] 的 △(=19200cm )比[CrCl] 中的 △(=13600cm )大;[IrCl] 的 △(=24900cm )比[RhCl] 的 △(=20300cm )大。

