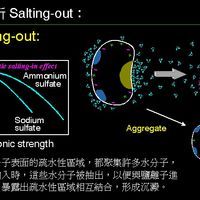
基本概念
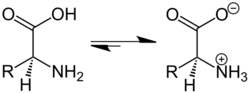 內鹽
內鹽兩性離子(英語:zwitterion)是總電荷為0,電中性的化合物,
又稱內鹽。但是帶正電和負電的原子不同。有些化學家將此術語限定為未具有相鄰正負電荷的化合物。此定義將諸如氧化胺的化合物排除。兩性離子為極性,通常易溶於水,難溶於大部分有機溶劑。
兩性電解質是具有酸性與鹼性基團的分子(因此具備兩性的特性),在特定pH值環境多半以兩性離子存在。平均電荷為0的pH值稱為該分子的等電點。
實際套用
兩性電解質用於建立穩定的pH梯度供等電位聚焦使用,。
典型的兩性離子有:
大部分胺基酸在生理pH值環境中為兩性離子
作為en:Good's buffers的緩衝劑
作為清潔劑:
自然產物如生物鹼en:Psilocybin與麥角酸
en:Betaine
較不常見的兩性離子有:
en:Quinonoid zwitterion
藥物,諸如en:Fexofenadine (Allegra) 與Cephaloridine
decaphenylferrocene [(η-C5Ph5)2Fe]已被證實具有兩性離子鍵合異構體[(η-C5Ph5)Fe(η-C6H5C5Ph4)]